Viết phương trình ion rút gọn và cân bằng:
6FeSO4 + K2Cr2O7 + 7H2SO4 -> K2SO4 + Cr2(SO4)3 + 3Fe2(SO4)3 + 7H2O
Cho phản ứng: 6 F e S O 4 + K 2 C r 2 O 7 + 7 H 2 S O 4 → 3 F e 2 ( S O 4 ) 3 + C r 2 ( S O 4 ) 3 + K 2 S O 4 + 7 H 2 O
Trong phản ứng trên, chất oxi hóa và chất khử lần lượt là
A. K2Cr2O7 và FeSO4
B. K2Cr2O7 và H2SO4
C. H2SO4 và FeSO4
D. FeSO4 và K2Cr2O7
Cho phản ứng
6 F e S O 4 + K 2 C r 2 O 7 + 7 H 2 S O 4 → 3 F e 2 ( S O 4 ) 3 + C r 2 ( S O 4 ) 3 + K 2 S O 4 + 7 H 2 O
Trong phản ứng trên, chất oxi hóa và chất khử lần lượt là
A. K2Cr2O7 và FeSO4.
B. K2Cr2O7 và H2SO4.
C. H2SO4 và FeSO4.
D. FeSO4 và K2Cr2O7.
Đáp án A.
6 F e S O 4 + K 2 C r 2 O 7 + 7 H 2 S O 4 → 3 F e 2 ( S O 4 ) 3 + C r 2 ( S O 4 ) 3 + K 2 S O 4 + 7 H 2 O
Số oxi hóa của Fe tăng → FeSO4 là chất khử.
Số oxi hóa của Cr giảm → K2Cr2O7 là chất oxi hóa
H2SO4 đóng vai trò là môi trường.
Cho phản ứng: 6FeSO4 + K2Cr2O7 + 7H2SO4 → 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O
Trong phản ứng trên, chất oxi hóa và chất khử lần lượt là
A. FeSO4 và K2Cr2O7
B. K2Cr2O7 và FeSO4
C. H2SO4 và FeSO4
D. K2Cr2O7 và H2SO4
Chọn đáp án B.
6 F e + 2 S O 4 + K 2 C r 2 + 6 O 7 + 7 H 2 S O 4 → 3 F e 2 + 3 S O 4 3 + C r 2 + 2 S O 4 3 + K 2 S O 4 + 7 H 2 O
Dựa vào phản ứng trên ta thấy, Fe tăng từ mức oxi hóa +2 lên +3 và Cr giảm từ mức oxi hóa +6 xuống +3 nên FeSO4 là chất khử, K2Cr2O7 là chất oxi hóa.
Cho phản ứng
6 F e S O 4 + K 2 C r 2 O 7 + 7 H 2 S O 4 → 3 F e 2 ( S O 4 ) 3 + C r 2 ( S O 4 ) 3 + K 2 S O 4 + 7 H 2 O
Trong phản ứng trên, chất oxi hóa và chất khử lần lượt là
A. K2Cr2O7 và FeSO4.
B. K2Cr2O7 và H2SO4.
C. H2SO4 và FeSO4.
D. FeSO4 và K2Cr2O7.
Đáp án A.
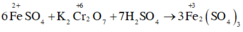
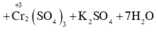
Số oxi hóa của Fe tăng → FeSO4 là chất khử.
Số oxi hóa của Cr giảm → K2Cr2O7 là chất oxi hóa
H2SO4 đóng vai trò là môi trường.
Cho phản ứng :
6FeSO4 + K2Cr2O7 + 7H2SO4 → 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 +7H2O
Trong phản ứng trên, chất oxi hóa và chất khử lần lượt là
A. FeSO4 và K2Cr2O7
B. H2SO4 và FeSO4.
C. K2Cr2O7 và FeSO4.
D. K2Cr2O7 và H2SO4.
Ta có Fe2+ lên F3+ và Cr6+ xuống Cr3+ nên chất oxi hóa (giảm số oxi hóa) là K2Cr2O7 và chất khử (tăng số oxi hóa) là FeSO4
=> Đáp án C
Cho phản ứng
6FeSO4 + K2Cr2O7 + 7H2SO4 ® 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O
Trong phản ứng trên, chất oxi hóa và chất khử lần lượt là:
A. FeSO4 và K2Cr2O7
B. K2Cr2O7 và FeSO4
C. H2SO4 và FeSO4
D. K2Cr2O7 và H2SO4
Cho phuong trình phản ứng:
K 2 C r 2 O 7 + C u F e S 2 + H B r + H 2 S O 4 → K 2 S O 4 + B r 2 + C u S O 4 + F e 2 ( S O 4 ) 3 + H 2 O + C r 2 ( S O 4 ) 3
Tổng các hệ số cân bằng (nguyên, tối giản) trong phương trình trên là:
A. 180
B. 327
C. 88
D. 231
Để cho đơn giản, ta tách thành 2 phản ứng oxi hóa - khử và cân bằng như sau:
![]()
![]()
![]()
![]()
Kết hợp hai phương trình ta được:
![]()
![]()
Khi đó tổng các hệ số cân bằng (nguyên, tối giản) của các chất trong phản ứng là: 18+6+66+75+18+18+6+3+3+78=231
Đáp án D
Cân bằng các phản ứng sau bằng phương pháp thăng bằng electron
1. 3K2S + K2Cr2O7 + 7H2SO4 → 3S + Cr2 (SO4) 3 + 4K2SO4 + 7H2O
2. Fe3O4 + HNO3 → Fe(NO3) 3 + NO + H2O
3. K2SO3 + KMnO4 + KHSO4 → K2SO4 + MnSO4 + H2O
4. SO2 + KMnO4 + H2O → K2SO4 + MnSO4 + H2SO4
5. K2S + KMnO4 + H2SO4 → S + MnSO4 + K2SO4 + H2O
6. Mg + HNO3 → Mg(NO3) 2 + NH4NO3 + H2O
7. CuS2 + HNO3 → Cu(NO3) 2 + H2SO4 + N2O + H2O
8. K2Cr2O7 + KI + H2SO4 → Cr2(SO4) 3 + I2 + K2SO4 + H2O
9. FeSO4 + Cl2 + H2SO4 → Fe2(SO4) 3 + HCl
10. KI + KClO3 + H2SO4 → K2SO4 + I2 + KCl + H2O
11. Cu2S + HNO3 (l) → Cu(NO3)2 + CuSO4 + NO + H2O
Cho phản ứng:
6 F e S O 4 + K 2 C r 2 O 7 + 7 H 2 S O 4 → 3 F e 2 S O 4 3 + C r 2 S O 4 3 + K 2 S O 4 + 7 H 2 O
Trong phản ứng trên, chất oxi hóa và chất khử lần lượt là:
A. K2Cr2O7 và FeSO4.
B. K2Cr2O7 và H2SO4.
C. H2SO4 và FeSO4.
D. FeSO4 và K2Cr2O7.
Chọn A.
Trong phản ứng trên Fe trong FeSO4 có số oxi hóa tăng từ +2 lên +3 nên FeSO4 đóng vai trò chất khử, Cr trong K2Cr2O7 có số oxi hóa giảm từ +6 xuống +3 nên K2Cr207 đóng vai trò chất oxi hóa.