hãy nhận biết các dung dịch sau: NaOH, HNO3, CaCl2, H2SO4, bằng phương pháp hoá học. Viết PTHH xảy ra (nếu có)

Những câu hỏi liên quan
Bài 1: Bằng phương pháp hoá học nhận biết các dung dịch mất nhãn sau, viết PTHH xảy ra nếu có:a.Ba(OH)2, NaCl, HCl, K2SO4b.NaOH, H2SO4, NaNO3, K2SO4Bài 2: Em hãy tự viết các PTHH theo mẫu sau:1.Sodium hydroxide NaOH: có đầy đủ tính chất của 1 base tan2. Calcium hydroxide Ca(OH)2: có đầy đủ tính chất của 1 base tan
Đọc tiếp
Bài 1: Bằng phương pháp hoá học nhận biết các dung dịch mất nhãn sau, viết PTHH xảy ra nếu có:
a.Ba(OH)2, NaCl, HCl, K2SO4
b.NaOH, H2SO4, NaNO3, K2SO4
Bài 2: Em hãy tự viết các PTHH theo mẫu sau:
1.Sodium hydroxide NaOH: có đầy đủ tính chất của 1 base tan
2. Calcium hydroxide Ca(OH)2: có đầy đủ tính chất của 1 base tan
Nhận biết các dung dịch mất nhãn sau bằng phương pháp hoá học: NaCl, NaOH, H2SO4, HCl. Viết phương trình hóa học xảy ra (nếu có).
- Cho các dd tác dụng với quỳ tím
+ QT chuyển đỏ: H2SO4, HCl (1)
+ QT chuyển xanh: NaOH
+ QT không chuyển màu: NaCl
- Cho các dd ở (1) tác dụng với dd BaCl2
+ Không hiện tượng: HCl
+ Kết tủa trắng: H2SO4
\(BaCl_2+H_2SO_4\rightarrow BaSO_4\downarrow+2HCl\)
Đúng 1
Bình luận (0)
Hãy nhận biết các dung dịch: NaOH; Na2SO4; HCl, H2SO4 bị mất nhãn đựng trong mỗi lọ bằng phương pháp hoá học. Viết các PTHH (nếu có).
Xem chi tiết
\(NaOH\left(B\right);Na_2SO_4\left(M\right);HCl\left(A\right);H_2SO_4\left(A\right)\)
`-` Trích mẫu thử
`-` Nhỏ lần lượt các mẫu thử lên giấy quỳ tím:
`+` Quỳ tím hóa đỏ `-> HCl,H_2SO_4` `(1)`
`+` Quỳ tím hóa xanh `-> NaOH` (nhận)
`+` Quỳ tím không đổi màu `-> Na_2SO_4` (nhận)
`-` Lần lượt cho dung dịch `BaCl_2` vào `2` mẫu thử ở nhóm `(1)`
`+` Xuất hiện kết tủa màu trắng `->H_2SO_4`
`PT:BaCl_2 + H_2SO_4 -> BaSO_4 + 2HCl`
`+` Không có dấu hiệu phản ứng `-> HCl`.
Đúng 5
Bình luận (0)
Bằng phương pháp hoá học hãy nhận biết các dung dịch sau đây: dung dịch NAOH, H2SO4,HNO3,KCL
Trích mẫu thử
Cho quỳ tím vào các mẫu thử
- mẫu thử nào làm quỳ tím hoá đỏ là $H_2SO_4,HNO_3$
- mẫu thử nào làm quỳ tím hoá xanh là $NaOH$
- mẫu thử nào không đổi màu quỳ tím là $KCl$
Cho dung dịch $BaCl_2$ vào hai mẫu thử còn :
- mẫu thử nào tạo kết tủa trắng là $H_2SO_4$
$BaCl_2 + H_2SO_4 \to BaSO_4 + 2HCl$
- mẫu thử nào không hiện tượng gì là $KCl$
Đúng 1
Bình luận (0)
bằng phương pháp hóa học em hãy nhận biết 3 dung dịch không màu sau là: CaCl2,NaNO3, KOH. Viết các PTHH xảy ra?
- Trích mẫu thử.
- Nhỏ vài giọt từng mẫu thử vào giấy quỳ tím.
+ Quỳ hóa xanh: KOH.
+ Quỳ không đổi màu: CaCl2, NaNO3. (1)
- Cho mẫu thử nhóm (1) pư với dd AgNO3.
+ Xuất hiện kết tủa trắng: CaCl2.
PT: \(CaCl_2+2AgNO_3\rightarrow Ca\left(NO_3\right)_2+2AgCl_{\downarrow}\)
+ Không hiện tượng: NaNO3.
- Dán nhãn.
Đúng 2
Bình luận (0)
1/ hãy nêu phương pháp nhận biết các lọ đựng riêng biệt các dung dịch mất nhãn: HCl; H2SO4 ;HNO3 Viết các phương trình hoá học xảy ra.
2/ bằng phương pháp hóa học ,chỉ dùng thêm một kim loại Cu phân biệt các chất sau đây đựng trong các lọ không nhãn : HCl; HNO3;NaOH ; AgNO3;NaNO3; HgCl2.
2.-Trích mỗi lọ một ít làm mẫu thử
-cho Cu tác dụng từng chất, nhận ra HNO3 có khí không màu hóa nâu trong không khí(NO).Nhận ra AgNO3 và HgCl2 vì pư tạo dung dịch màu xanh.
-Dùng dung dịch muối Cu tạo ra, nhận ra được NaOH có kết tủa xanh lơ.
Dùng Cu(OH)2 để nhận ra HCl làm tan kết tủa.
-Dùng dd HCl để phân biệt AgNO3 và HgCl2 ( có kết tủa trắng là AgNO3 )
PTHH:3Cu + 8HNO3 -->3Cu(NO3)2 + 4H2O + 8NO
2AgNO3 + Cu --> 2Ag + Cu(NO3)2
Cu + HgCl2 --> CuCl2 + Hg
NaOH + Cu(NO3)--> Cu(OH) + NaNO3
Cu(OH)2 + 2HCl--> CuCl2 + 2H2O
AgNO3 +HCl--> AgCl+ HNO3
Đúng 2
Bình luận (0)
1) * Trích mỗi ống nghiệm một ít hóa chất đánh dấu làm mẫu thử
- Cho một mẩu quỳ tím vào 3 mẫu thử
+ Nếu dung dịch nào làm quỳ tím ngả màu xanh là dung dich HCl
+ Nếu mẫu thử làm cho quỳ tím ngả màu đỏ là dung dịch H2SO4
- Còn lại là HNO3
Đúng 1
Bình luận (1)
Câu 3: a. Có 4 lọ không nhân mỗi lọ đựng các dung dịch sau: KOH, Na2SO4 Nacl, H2SO4 làm thế nào để nhận biết dung dịch đựng trong mỗi lọ bằng phương pháp hoá học. Viết PTHH xảy ra( nếu có). b/ Nhận biết các dung dịch mất nhãn sau: Ba(OH)2 ; KOH ; H2SO4 ; HNO3 ; Nacl ; NaNO3
a)
- Cho các dd tác dụng với quỳ tím:
+ Quỳ tím chuyển đỏ: H2SO4
+ Quỳ tím chuyển xanh: KOH
+ Quỳ tím không chuyển màu: Na2SO4, NaCl
- Cho 2 dd còn lại tác dụng với dd BaCl2
+ Kết tủa trắng: Na2SO4
\(Na_2SO_4+BaCl_2\rightarrow BaSO_4\downarrow+2NaCl\)
+ Không hiện tượng: NaCl
b)
- Cho các dd tác dụng với quỳ tím:
+ Quỳ tím chuyển xanh: Ba(OH)2, KOH (1)
+ Quỳ tím chuyển đỏ: H2SO4, HNO3 (2)
+ Quỳ tím không chuyển màu: NaCl, NaNO3 (3)
- Cho dd ở (1) tác dụng với dd Na2SO4:
+ Kết tủa trắng: Ba(OH)2
\(Ba\left(OH\right)_2+Na_2SO_4\rightarrow BaSO_4\downarrow+2NaOH\)
+ Không hiện tượng: KOH
- Cho 2 dd ở (2) tác dụng với dd BaCl2
+ Kết tủa trắng: H2SO4
\(BaCl_2+H_2SO_4\rightarrow BaSO_4\downarrow+2HCl\)
+ Không hiện tượng: HNO3
- Cho 2 dd ở (3) tác dụng với dd AgNO3
+ Kết tủa trắng: NaCl
\(NaCl+AgNO_3\rightarrow AgCl\downarrow+NaNO_3\)
+ Không hiện tượng: NaNO3
Đúng 0
Bình luận (0)
Bằng phương pháp hoá học hãy nhận biết dung dịch sau: NaCl,H2SO4,Na2SO4,NaOH. Viết phương trình hóa học (nếu có)
Trích mẫu thử
Nhúng quỳ tím vào các mẫu thử
+Nếu mẫu thử nào làm quỳ tím hóa đỏ-->H2SO4
+Nếu mẫu thử nào làm quỳ tím hóa xanh-->NaOH
+Còn lại ko hiện tượng
*Nhận biết các mẫu thử còn lại
-Cho dd BaCl2 vào các mẫu thử còn lại
+Nếu xuất hiện kết tủa trắng-->Na2SO4
+Còn lại NaCl ko hiện tượng
*PTHH:
Na2SO4+BaCl2--->BaSO4+2NaCl
Đúng 1
Bình luận (0)
Lấy mỗi chất ra một ít và làm thí nghiệm sau:
- Nhỏ quỳ tím vào các mẫu thử:
+ Mẫu thử làm quỳ chuyển màu đỏ: \(H_2SO_4\) (1)
+ Mẫu thử làm quỳ chuyển xanh: \(NaOH\)
+ Quỳ không chuyển màu: NaCl, \(Na_2SO_4\)
- Tiếp tục cho các mẫu thử còn lại td với dd \(BaCl_2\):
+ Mẫu có hiện tượng kt trắng: \(Na_2SO_4\)
\(Na_2SO_4+BaCl_2\rightarrow BaSO_4+2NaCl\)
+ Mẫu không hiện tượng: NaCl
Đúng 0
Bình luận (0)
Bằng phương pháp hóa học hãy nhận biết các dung dịch sau: Na2SO4, HCL, NaOH , NaCL. Viết các pthh xảy ra
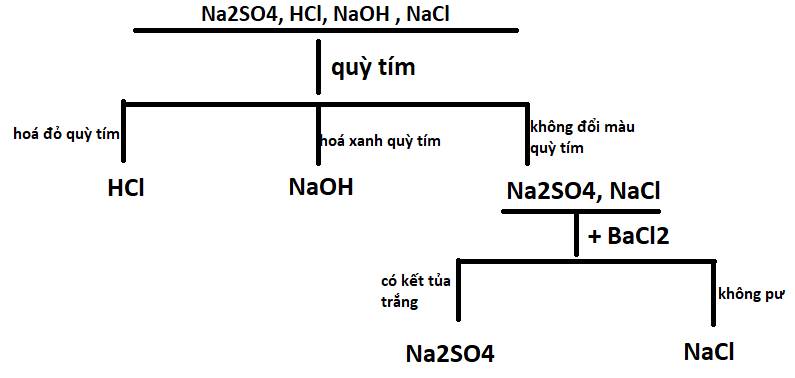
PTHH:
Na2SO4 + BaCl2 ----> BaSO4\(\downarrow\) + 2NaCl
**P/s: Có thể thay BaCl2 bằng Ba(OH)2, phản ứng vẫn xảy ra tương tự.
Na2SO4 + Ba(OH)2 ---> BaSO4\(\downarrow\) + 2NaOH
Chúc em học tốt!
Đúng 2
Bình luận (0)

























