Cho A gam hỗn hợp Bari Cacbonat và Canxi Cacbonat tác dụng với V lít dd HCL 0,4M thấy giải phóng 4,48 lít CO2 (đktc), dẫn khí thu được vào dung dịch Ca(OH)2 dư. Tính
a/ Khối lượng kết tủa thu được
b/ Thể tích dd HCL cần dùng
Cho a g hỗn hợp BaCO3, CaCO3 tác dụng hết với V lít dd HCl 0,4 M thấy giải phóng 4,48 lít CO2 (đktc). Dẫn khí thu được vào dd Ca(OH)2 dư.
a. Khối lượng kết tủa thu được là B. 15 gam C. 20g A. 10g D. 25 gam
b. Thể tích dd HCI cần dùng là C. 1,6 lít B. 1,5 lít A. 1 lít D. 1,7 lít
c. Giá trị của a nằm trong khoảng nào? A. 10 gam <a <20 gam B. 20 gam <a <35,4 gam C. 20g <a <39,4g D. 20g < a <40g
a) \(n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
0,2----->0,2
=> mCaCO3 = 0,2.100 = 20 (g)
=> C
b)
PTHH: BaCO3 + 2HCl --> BaCl2 + CO2 + H2O
CaCO3 + 2HCl --> CaCl2 + CO2 + H2O
=> nHCl = 2.nCO2 = 2.0,2 = 0,4 (mol)
=> \(V_{dd.HCl}=\dfrac{0,4}{0,4}=1\left(l\right)\)
=> A
c)
nmuối = 0,2 (mol)
Có: 100.0,2 < a < 197.0,2
=> 20 < a < 39,4
=> C
. PTHH: C O 2 + C a ( O H ) 2 → C a C O 3 + H 2 O n C O 2 = 4 , 48 22 , 4 = 0 , 2 m o l → n C a C O 3 = n C O 2 = 0 , 2 m o l → m C a C O 3 = 0 , 2.100 = 20 g a m → Chọn C. b. PTHH: B a C O 3 + 2 H C l → B a C l 2 + C O 2 + H 2 O C a C O 3 + 2 H C l → C a C l 2 + C O 2 + H 2 O Nhận xét: Từ PTHH ta thấy n H C l = 2 n C O 2 = 0 , 4 m o l → V H C l = 0 , 4 0 , 4 = 1 , 0 l í t → Chọn A. c. Giả sử hỗn hợp ban đầu chỉ có BaCO3 n B a C O 3 = n C O 2 = 0 , 2 m o l → m B a C O 3 = 0 , 2.197 = 39 , 4 g a m Giả sử hỗn hợp ban đầu chỉ có CaCO3 n C a C O 3 = n C O 2 = 0 , 2 m o l → m C a C O 3 = 0 , 2.100 = 20 g a m Thực tế, hỗn hợp ban đầu chứa cả BaCO3 và CaCO3 nên giá trị của a nằm trong khoảng 20 gam < a < 39,4 gam
Hấp thụ hoàn toàn V lít khí CO2 (đktc) vào 250 ml dung dịch hỗn hợp gồm NaOH 0,4M và KOH aM thì thu được dung dịch X. Cho từ từ 250 ml dung dịch H2SO4 0,5M vào X thu được dung dịch Y và 1,68 lít khí CO2 (đktc). Cho Y tác dụng với dung dịch Ba(OH)2 dư thấy xuất hiện 34,05 gam kết tủa trắng. Giá trị của a là
A. 0,9
B. 0,7
C. 0,5
D. 0,6
Hấp thụ hoàn toàn V lít khí CO2 (đktc) vào 250 ml dung dịch hỗn hợp gồm NaOH 0,4M và KOH aM thì thu được dung dịch X. Cho từ từ 250 ml dung dịch H2SO4 0,5M vào X thu được dung dịch Y và 1,68 lít khí CO2 (đktc). Cho Y tác dụng với dung dịch Ba(OH)2 dư thấy xuất hiện 34,05 gam kết tủa trắng. Giá trị của a là
A. 0,9
B. 0,7
C. 0,5
D. 0,6
Câu 4. Dẫn 672 ml đktc khí CO2 vào dung dịch Ca(OH)2 dư có nồng độ 1,5M, sau phản ứng hoàn toàn thu được kết tủa canxi cacbonat. Tính a. Khối lượng khối lượng kết tủa thu được. b. Thể tích dung dịch Ca(OH)2 cần dùng cho phản ứng.
\(a.n_{CO_2}=\dfrac{0,672}{22,4}=0,03mol\\ CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
\(n_{CO_2}=n_{Ca\left(OH\right)_2}=n_{CaCO_3}=0,03mol\\ m_{CaCO_3}=0,03.100=3g\\ b.V_{ddCa\left(OH\right)_2}=\dfrac{0,03}{1,5}=0,02l\)
Đốt cháy hoàn toàn 4,3 gam một chất hữu cơ X thu được hỗn hợp khí CO2, H2O, HCl. Dẫn hỗn hợp này vào bình đựng dung dịch AgNO3 dư, thu được 5,74 gam kết tủa và khối lượng bình dung dịch AgNO3 tăng thêm 2,54 gam. Khí thoát ra khỏi bình dung dịch AgNO3 dẫn vào 5 lít dung dịch Ca(OH)2 0,02M (TN1) thấy xuất hiện kết tủa, lọc tách kết tủa, dung dịch còn lại cho tác dụng với dung dịch Ba(OH)2 dư (TN2) lại thấy xuất hiện thêm kết tủa, tổng khối lượng kết tủa ở 2 thí nghiệm là 13,94 gam. Biết Mx < 230 gam/mol. Số nguyên tử O trong một phân tử của X là
A. 2
B. 4
C. 1
D. 3.
Cho 0,5 mol hỗn hợp hai muối cacbonat của kim loại hoá trị II tác dụng hết với dd HCl. Dẫn khí thoát ra vào dd Ca(OH)2 dư thì khối lượng kết tủa thu được là: D. 60 gam C. 55 gam A. 50g B. 45 gam
Gọi công thức chung 2 muối là ACO3
PTHH: ACO3 + 2HCl --> ACl2 + CO2 + H2O
0,5-------------------->0,5
Ca(OH)2 + CO2 --> CaCO3 + H2O
0,5---->0,5
=> mCaCO3 = 0,5.100 = 50 (g)
=> A
Gọi 2 kim loại đó lần lượt là M và N (II):
PTHH:
MCO3 + 2HCl ---> MCl2 + CO2 + H2O
NCO3 + 2HCl ---> NCl2 + CO2 + H2O
Theo pt: nCO2 = nmuối = 0,5 (mol)
Ca(OH)2 + CO2 ---> CaCO3 + H2O
0,5--------->0,5
=> m = 0,5.100 = 50 (g)
=> A
Nung m gam hỗn hợp X gồm hai muối cacbonat trung tính của 2 kim loại A và B đều có hóa trị 2. Sau một thời gian thu được 3,36 lít CO2 đktc và còn lại hỗn hợp rắn Y. Cho Y tác dụng hết với dung dịch HCl dư rồi cho khí thoát ra hấp thụ hết bởi dung dịch Ca(OH)2 dư thu được 15 gam kết tủa, phần dung dịch đem cô cạn thu được 32,5 gam hỗn hợp muối khan. Giá trị của m là:
A. 30,8 gam
B. 29,2 gam
C. 29,8 gam
D. 30,2 gam
Đáp án B
Gọi công thức trung bình của hai muối ACO3 và BCO3 là MCO3
MCO3 → MO + CO2
n C O 2 = 3,36 /22,4 = 0,15 mol → n M C O 3 = 0,15 mol
Hỗn hợp Y gồm MCO3 dư và MO
MCO3 + 2HCl → MCl2 + CO2 + H2O
MO + 2HCl → MCl2 + H2O
CO2 + Ca(OH)2 dư → CaCO3 ↓ + H2O
n C a C O 3 = 15/100 = 0,15 mol
→ n M C O 3 dư = 0,15 mol
n M C O 3 ban đầu = 0,15 + 0,15 = 0,3 mol
Bảo toàn kim loại M có:
n M C O 3 = n M C l 2 = 0,3 (mol)
Bảo toàn khối lượng có:
m M C O 3 = m M C l 2 - 0,3.(71- 60) = 29,2 (gam)
Cho 29,2 gam hỗn hợp khí X gồm Fe3O4 và CuO phản ứng với CO nung nóng, sau một thời gian thu được hỗn hợp rắn Y và hỗn hợp khí Z. Cho Z tác dụng với dd Ba(OH)2 dư thu được 9,85 gam kết tủa. Hòa tan hết Y trong 150 gam dung dịch HNO3 63% đun nóng thu được dung dịch T và 4,48 lít NO2 (đktc) ( là sản phẩm khử duy nhất). Cho V (lít) dung dịch NaOH 1M vào dung dịch T, phản ứng hoàn toàn tạo ra kết tủa với khối lượng lớn nhất. Phần trăm khối lượng Fe3O4 và giá trị V là
A. 20,54% và 1,300 lít
B. 20,54% và 0,525 lít
C. 79,45 % và 1,300 lít
D. 19,45% và 0,525 lít
Đáp án C
nHNO3 bđ = 1,5 ; nNO2 = 0,2 (mol)
Khi thêm nước lọc vào T và thu được lượng kết tủa max thì phần dung dịch nước lọc chỉ chứa NaNO3.
Bảo toàn N => nNaNO3 = nHNO3 – nNO2 = 1,3 (mol)
=> nNaOH = 1,3 => Vdd NaOH = 1,3 (lít)
Đặt a, b là số mol Fe3O4 và CuO
mhh = 232a + 80b = 29,2 (1)
Có: nCO2 = nBaCO3 = 0,05 (mol) = nO( trong oxit pư)
Bảo toàn e cả quá trình: nNO2 = nFe3O4 + 2nO (mất đi khi + CO)
=> nFe3O4 = nNO2 - 2nO (mất đi khi + CO) = 0,2 – 2.0,05 = 0,1 (mol)
=> %mFe3O4 = [0,1. 232: 29,2].100% = 79,45%
Đốt cháy hoàn toàn 4,3 gam một chất hữu cơ X thu được hỗn hợp khí CO2, H2O, HCl. Dẫn hỗn hợp này vào bình đựng dung dịch AgNO3 dư thu được 5,74 gam kết tủa và khối lượng bình dung dịch AgNO3 tăng thêm 2,54 gam. Khí thoát ra khỏi bình dung dịch AgNO3 dẫn vào 5 lít dung dịch Ca(OH)2 0,02M thấy xuất hiện kết tủa, lọc tách kết tủa, dung dịch còn lại cho tác dụng Ba(OH)2 dư lại thấy xuất hiện thêm kết tủa, tổng khối lượng kết tủa ở 2 thí nghiệm là 13,94 gam. Biết Mx < 230 g/mol. Số nguyên tử O trong một phân tử của X là
A. 4
B. 1
C. 2
D. 3
Đáp án A
Có
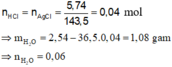
Khí thoát ra khỏi bình là CO2.
CO2 + 0,1 mol Ca(OH)2 → CaCO3 + dung dịch
Dung dịch thu được + Ba(OH)2 dư → BaCO3
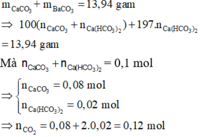
Áp dụng định luật bảo toàn khối lượng có:
mO(X) = 4,3 – 12.0,12 – 1.(2.0,06 + 0,04) – 35,5.0,04 = 1,28 gam
nO(X) = 0,08 mol
nC : nH : nO : nCl = 0,12 : 0,16 : 0,08 : 0,04 = 3:4:2:1
X có dạng C3nH4nO2nCln 107,5n < 230 n < 2,13 mà tổng số nguyên tử H và Cl phải là số chẵn n = 2
Trong phân tử X chứa 4 nguyên tử O