C1: Cho 100ml dung dịch NaOH 1M vào 100 mol dung dịch HCLcm=> dung dịch X tính Cm của HCL
C2 : Cho 6,2(g) Na2O vào 100g H2O=>Dung dịch X tính C%
1,hòa tan 6,2 gam Sodium oxide (Na2O)vào nước (H2O) được 2 lít dung dịch Sodium Hydroxide (NaOH).Tính nồng độ mol/L của dung dịch X
\(n_{Na_2O}=\dfrac{6,2}{62}=0,1mol\\ Na_2O+H_2O\rightarrow2NaOH\\ n_{NaOH}=0,1.2=0,2mol\\ C_{M_X}=C_{M_{NaOH}}=\dfrac{0,2}{2}=0,1M\)
\(n_{Na_2O}=\dfrac{6,2}{62}=0,1\left(mol\right)\)
PT: \(Na_2O+H_2O\rightarrow2NaOH\)
Theo PT: \(n_{NaOH}=2n_{Na_2O}=0,2\left(mol\right)\)
\(\Rightarrow C_{M_{NaOH}}=\dfrac{0,2}{2}=0,1\left(m\right)\)
Hoà tan hoàn toàn 19,5 gam hỗn hợp Na2O, Al2O3 vào nước được 500ml dung dịch trong suốt X. Thêm dần dần dung dịch HCl 1M vào dung dịch X đến khi bắt đầu thấy xuất hiện kết tủa thì dừng lại nhận thấy thể tích dung dịch HCl 1M đã cho vào là 100ml. Tính nồng độ mol của các chất tan trong dung dịch
A. [Na[Al(OH)4]] = 0,2M; [NaOH] = 0,4M
B. [Na[Al(OH)4]] = 0,2M; [NaOH] = 0,2M
C. [Na[Al(OH)4]] = 0,4M; [NaOH] = 0,2M
D. [Na[Al(OH)4]] = 0,2M
Gọi số mol Na2O và Al2O3 lần lượt là x, y
Nhận thấy khi thêm 0,1 mol HCl vào dung dịch X thì thấy xuất hiện kết tủa
→ Trong dung dịch X chứa NaAlO2 a mol và NaOH :0,1 mol
Bảo toàn nguyên tố → nNa2O = (nNaOH + nNaAlO2):2 = (0,1 + a): 2
nAl2O3 = nNaAlO2 : 2 = a:2
Ta có phương trình : [(0,1 + a): 2 ]×62 + (a:2)×102 = 19,5→ → a= 0,2 mol
CMNaOH = 0,2M, CMNaAlO2 = 0,4M
Đáp án C
cho 12.4 g na2o vào 500 ml nước thu được dung dịch x a) viết pthh tính nồng độ mol của dung dịch X b) để trung hìa dung dịch X người ta cần Vml dung dịch H2So4 1M ( vừa đủ ) tính V
\(n_{Na_2O}=\dfrac{12,4}{62}=0,2\left(mol\right)\)
PTHH:
\(Na_2O+H_2O\rightarrow2NaOH\)
0,2 0,2 0,4
\(C_{M\left(NaOH\right)}=\dfrac{0,4}{0,5}=0,8\left(M\right)\)
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
0,4 0,2
\(V_{H_2SO_4}=\dfrac{0,2}{1}=0,2\left(l\right)=200\left(ml\right)\)
\(a)Na_2O+H_2O\rightarrow2NaOH\\ n_{Na_2O}=\dfrac{12,4}{62}=0,2mol\\ n_{NaOH}=0,2.2=0,4mol\\ C_{M_{NaOH}}=\dfrac{0,4}{0,5}=0,8M\\ b)2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\\ n_{H_2SO_4}=0,4:2=0,2mol\\ V_{ddH_2SO_4}=\dfrac{0,2}{1}=0,2l=200ml\)
Cho từ từ 100 ml dung dịch chứa hỗn hợp NaHCO3 2M, Na2CO3 1M vào 100 ml dung dịch chứa HCl 1M và H2SO4 0,5M thu được V lít khí (đktc) và dung dịch X. Cho 100ml dung dịch Ba(OH)2 2M và NaOH 0,75M vào dung dịch X thu được m (g) kết tủa. Giá trị của m, V là:
A. 45 gam và 2,24 lít
B. 43 gam và 2,24 lít
C. 41,2 gam và 3,36 lít
D. 43 gam và 3,36 lít
Đáp án C
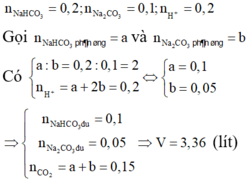
n Ba ( OH ) 2 = 0 , 2 ; n NaOH = 0 , 075
![]()
Hòa tan 100ml dung dịch NaOH 1M vào 100ml dung dịch Ca(OH)2 0,3 M . Tính nồng độ mol của ion trong dung dịch thu được?
Khi cho 100ml dung dịch NaOH 1M vào 100 ml dung dịch HNO 3 xM, thu được dung dịch có chứa 7,6 gam chất tan. Giá trị của x là
A. 1,2.
B.0,8.
C. 0,6
D. 0,5.
a,tính khối lượng NaOH có trong 200ml dung dịch NaOh 1M b,tính số mol H2SO4 có trong 100ml dung dịch H2SO4 2M c,hoà tan 6g NaCl vào nước thu được 200g dung dịch tính nồng độ phần trăm của dung dịch d,tính khối lượng NaCl có trong 200g dung dịch NaCl 8%
a, \(n_{NaOH}=0,2.1=0,2\left(mol\right)\)
\(m_{NaOH}=0,2.40=8\left(g\right)\)
b, \(n_{H_2SO_4}=2.0,1=0,2\left(mol\right)\)
\(c,C\%=\dfrac{6}{200}.100\%=3\%\)
\(m_{NaCl}=\dfrac{200.8}{100}=16\left(g\right)\)
X là dung dịch AlCl3, Y là dung dịch NaOH 1M. Cho 240ml dung dịch Y vào cốc chứa 100ml dung dịch X, khuấy đều tới phản ứng hoàn toàn thấy trong cốc có 6,24 gam kết tủa. Thêm tiếp vào cốc 100ml dung dịch Y, khuấy đều đến khi kết thúc phản ứng thấy trong cốc có 4,68 gam kết tủa. Nồng độ mol của dung dịch X là
A. 1,0M
B. 1,2M
C. 1,5M
D. 1,6M
Nhận thấy, ở lần 1 thì chưa có kết tủa tan còn lần 2 đã có kết tủa tan (nếu ở trường hợp cả 2 lần đều có kết tủa tan thì chênh lệch số mol kết tủa sẽ bằng chênh lệch số mol NaOH cho vào)
Lần 2:

Hòa tan m(g) hỗn hợp Na2CO3 và KHCO3 vào H2O được 200ml dung dịch A. Cho từ từ vào dung dịch trên 100ml dung dịch HCl 1M thu được dung dịch B và thoát ra 1.12 l khí (đktc). Cho dung dịch B phản ứng với Ca(OH)2 thì thu được 20g chất rắn. Tính nồng độ mol các chất trong dung dịch
Na2CO3 + HCl = NaCl + NaHCO3
KHCO3 + HCl = KCl +CO2 + H2O
n HCl = 0,1 * 1,5=0,15 mol
n CO2 = 1,008 / 22,4 =0,045 mol => n KHCO3 = 0,045 mol = n iôn K+ = n iôn HCO3 -=> nồng độ MOl
dd B tác dụng với Ba(OH)2 dư : Ba(OH)2 (dư) + NaHCO3 = BaCO3 + NaOH +H2O
n kết tủa= n BaCO3 = 29,55/197=0,15 mol => n NaHCO3 = 0,15 mol = nNa2CO3 => n Na + trong ddA = 0,15 *2 = 0,3 mol => nồng độ mol
nHCO3 - = 0,15 mol => nồng độ mol
Có n Na2CO3 và nKHCO3 dễ dàng tính được a(g)
**** Cho từ từ DD A gồm Na2CO3 và NaHCO3 va ddHCl thì sẽ có 2 trường hợp
TH1: Na2CO3 phản ứng trước:
Na2CO3 +2 HCl =2NaCl + H2O +CO2
.................0,15
n Na2CO3 ở câu trên tính dc là 0,15 mol => n HCl phản ứng ở đây là 0,15 * 2 = 0,3 mol
goi x , y lan luot la nong do cua na2co3 va khco3
theo de bai : n(co3)2-=(nh+)-nco2=0,1-0,05=0,05 mol
=>x=0,05:0,2=0,25m
hco3-)+ca2+=>caco3
0,2
=>số mol hno3 ban đầu =so mol ket tua +nco2-nco3)2-=0,2mol=>y=1m