X là hỗn hợp Al và Zn, Y là dung dịch HCL chưa rõ nồng độ.
- Thí nghiệm 1: Cho 21,65 gam X vào 2 lít Y được 10,08 lít H2 (đktc).
- Thí nghiệm 2: Cho 21,65gam X vào 3 lít Y được 12,32 lít H2 (đktc).
Tính nồng độ mol của dung dịch Y và khối lượng Al, Zn có trong hỗn hợp.

Những câu hỏi liên quan
X là hỗn hợp Mg và Zn, Y là dung dịch H2SO4 chưa rõ nồng độ.
- Thí nghiệm 1: Cho 24,3 gam X vào 2 lít Y được 8,96 lít H2 (đktc).
- Thí nghiệm 2: Cho 24,3 gam X vào 3 lít Y được 11,2 lít H2 (đktc).
Tính nồng độ mol của dung dịch Y và khối lượng Mg, Zn có trong hỗn hợp.
PTHH:
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
Thí nghiệm 1:
Ta có:
\(n_{H_2SO_4}=n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
\(\Rightarrow C_{M\left(H_2SO_4\right)}=\dfrac{0,4}{2}=0,2M\)
\(n_{Mg}+n_{Zn}=n_{H_2SO_4}=0,4\left(mol\right)\left(1\right)\)
Lại có: \(24n_{Mg}+65n_{Zn}=24,3\left(2\right)\)
Giải hệ hai phương trình (1) và (2) ta được:
\(\left\{{}\begin{matrix}n_{Mg}=0,04\left(mol\right)\\n_{Zn}=0,36\left(mol\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}m_{Mg}=0,96\left(g\right)\\n_{Zn}=23,4\left(g\right)\end{matrix}\right.\)
Thí nghiệm 2:
Ta có:
\(n_{H_2SO_4}=n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(\Rightarrow C_{M\left(H_2SO_4\right)}=\dfrac{0,5}{2}=0,25M\)
\(n_{Mg}+n_{Zn}=n_{H_2SO_4}=0,5\left(mol\right)\left(3\right)\)
Lại có: \(24n_{Mg}+65n_{Zn}=24,3\left(4\right)\)
Giải hệ hai phương trình (3) và (4) ta được:
\(\left\{{}\begin{matrix}n_{Mg}=0,2\left(mol\right)\\n_{Zn}=0,3\left(mol\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}m_{Mg}=4,8\left(g\right)\\n_{Zn}=19,5\left(g\right)\end{matrix}\right.\)
Đúng 1
Bình luận (11)
Hỗn hợp A gồm hai kim loại Mg và Zn. Dung dịch B là dung dịch HCl nồng độ a mol/lít. Thí nghiệm 1: Cho 8,9 gam hỗn hợp A vào 2 lít dung dịch B, kết thúc phản ứng thu được 4,48 lít H2 (đktc). Thí nghiệm 2: Cho 8,9 gam hỗn hợp A vào 3 lít dung dịch B, kết thúc phản ứng cũng thu được 4,48 lít H2 (đktc). Giá trị của a là: A. 0,1 B. 0,15 C. 0,05 D. 0,3
Đọc tiếp
Hỗn hợp A gồm hai kim loại Mg và Zn. Dung dịch B là dung dịch HCl nồng độ a mol/lít.
Thí nghiệm 1: Cho 8,9 gam hỗn hợp A vào 2 lít dung dịch B, kết thúc phản ứng thu được 4,48 lít H2 (đktc).
Thí nghiệm 2: Cho 8,9 gam hỗn hợp A vào 3 lít dung dịch B, kết thúc phản ứng cũng thu được 4,48 lít H2 (đktc).
Giá trị của a là:
A. 0,1
B. 0,15
C. 0,05
D. 0,3
Đáp án D
Nhận thấy ở hai thí nghiệm có lượng kim loại tham gia phản ứng như nhau, lượng HCl sử dụng lớn hơn lượng HCl sử dụng ở thí nghiệm 1 nhưng lượng H2 ở hai thí nghiệm thu được như nhau.
Do đó ở thí nghiệm 2 HCl phản ứng dư, thí nghiệm 1 có HCl phản ứng đủ hoặc dư.
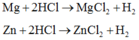
Có
![]()
Quan sát 4 đáp án nhận thấy chỉ có giá trị 0,3 là phù hợp.
Đúng 0
Bình luận (0)
1. Cho 5.1 gam hỗn hợp X gồm Al và Mg tác dụng vừa đủ với dung dịch HCl thấy khối lượng tăng lên 4.6 gam. Xác định số mol HCl tham gia phản ứng.2. Hòa tan a gam hỗn hợp bột Mg, Al bằng dung dịch HCl thu được 17.92 lít khí H2 (đktc). Cùng lượng hỗn hợp trên hòa tan trong dung dịch NaOH dư thu được 13.44 lít khí H2 (đktc). Giá trị của a ?.3. Cho hỗn hợp X gồm 2 kim loại Al và Ba. Tiến hành 2 thí nghiệm : *Thí nghiệm 1 : Cho m gam X vào nước dư thu được 1.344 lít H2 (đktc). *Thí nghiệm 2 : Ch...
Đọc tiếp
1. Cho 5.1 gam hỗn hợp X gồm Al và Mg tác dụng vừa đủ với dung dịch HCl thấy khối lượng tăng lên 4.6 gam. Xác định số mol HCl tham gia phản ứng.
2. Hòa tan a gam hỗn hợp bột Mg, Al bằng dung dịch HCl thu được 17.92 lít khí H2 (đktc). Cùng lượng hỗn hợp trên hòa tan trong dung dịch NaOH dư thu được 13.44 lít khí H2 (đktc). Giá trị của a = ?.
3. Cho hỗn hợp X gồm 2 kim loại Al và Ba. Tiến hành 2 thí nghiệm :
*Thí nghiệm 1 : Cho m gam X vào nước dư thu được 1.344 lít H2 (đktc).
*Thí nghiệm 2 : Cho 2m gam X vào dung dịch Ba(OH)2 dư thu được 20.832 lít khí H2 (đktc).
Tìm giá trị của m.
4. X là hỗn hợp Ba và Al. Hòa tan m gam X vào lượng dư nước thu được 8.96 lít H2 (đktc). Cũng hòa tan m gam X vào dung dịch NaOH dư thì thu được 12.32 lít khí H2 (đktc). Xác định giá trị của m.
1. Cho 5.1 gam hỗn hợp X gồm Al và Mg tác dụng vừa đủ với dung dịch HCl thấy khối lượng tăng lên 4.6 gam. Xác định số mol HCl tham gia phản ứng.2. Hòa tan a gam hỗn hợp bột Mg, Al bằng dung dịch HCl thu được 17.92 lít khí H2 (đktc). Cùng lượng hỗn hợp trên hòa tan trong dung dịch NaOH dư thu được 13.44 lít khí H2 (đktc). Giá trị của a ?.3. Cho hỗn hợp X gồm 2 kim loại Al và Ba. Tiến hành 2 thí nghiệm : *Thí nghiệm 1 : Cho m gam X vào nước dư thu được 1.344 lít H2 (đktc). *Thí nghiệm 2 : Ch...
Đọc tiếp
1. Cho 5.1 gam hỗn hợp X gồm Al và Mg tác dụng vừa đủ với dung dịch HCl thấy khối lượng tăng lên 4.6 gam. Xác định số mol HCl tham gia phản ứng.
2. Hòa tan a gam hỗn hợp bột Mg, Al bằng dung dịch HCl thu được 17.92 lít khí H2 (đktc). Cùng lượng hỗn hợp trên hòa tan trong dung dịch NaOH dư thu được 13.44 lít khí H2 (đktc). Giá trị của a = ?.
3. Cho hỗn hợp X gồm 2 kim loại Al và Ba. Tiến hành 2 thí nghiệm :
*Thí nghiệm 1 : Cho m gam X vào nước dư thu được 1.344 lít H2 (đktc).
*Thí nghiệm 2 : Cho 2m gam X vào dung dịch Ba(OH)2 dư thu được 20.832 lít khí H2 (đktc).
Tìm giá trị của m.
4. X là hỗn hợp Ba và Al. Hòa tan m gam X vào lượng dư nước thu được 8.96 lít H2 (đktc). Cũng hòa tan m gam X vào dung dịch NaOH dư thì thu được 12.32 lít khí H2 (đktc). Xác định giá trị của m.
Chia hỗn hợp X gồm K, Al và Fe thành hai phần bằng nhau. - Cho phần 1 vào dung dịch KOH (dư) thu được 0,784 lít khí H2 (đktc). - Cho phần 2 vào một lượng dư H2O, thu được 0,448 lít khí H2 (đktc) và m gam hỗn hợp kim loại Y. Hoà tan hoàn toàn Y vào dung dịch HCl (dư) thu được 0,56 lít khí H2 (đktc). Khối lượng (tính theo gam) của K, Al, Fe trong mỗi phần hỗn hợp X lần lượt là A. 0,78; 0,54; 1,12 B. 0,39; 0,54; 1,40 C. 0,39; 0,54; 0,56 D. 0,78; 1,08; 0,56
Đọc tiếp
Chia hỗn hợp X gồm K, Al và Fe thành hai phần bằng nhau.
- Cho phần 1 vào dung dịch KOH (dư) thu được 0,784 lít khí H2 (đktc).
- Cho phần 2 vào một lượng dư H2O, thu được 0,448 lít khí H2 (đktc) và m gam hỗn hợp kim loại Y. Hoà tan hoàn toàn Y vào dung dịch HCl (dư) thu được 0,56 lít khí H2 (đktc).
Khối lượng (tính theo gam) của K, Al, Fe trong mỗi phần hỗn hợp X lần lượt là
A. 0,78; 0,54; 1,12
B. 0,39; 0,54; 1,40
C. 0,39; 0,54; 0,56
D. 0,78; 1,08; 0,56
Chia hỗn hợp X gồm K, Al, Fe thành hai phần bằng nhau. Cho phần 1 vào dung dịch KOH dư thu được 0,784 lít khí H2 (đktc). Cho phần 2 vào một lượng dư H2O, thu được 0,448 lít khí H2 (đktc) và m gam hỗn hợp kim loại Y. Hòa tan hoàn toàn Y vào dung dịch HCl dư, thu được 0,56 lít khí H2 (đktc). Khối lượng (tính theo gam) của K, Al, Fe trong mỗi phần hỗn hợp X lần lượt là A. 0,39; 0,54; 0,56 B. 0,39; 0,54; 1,40 C. 0,78; 1,08; 0,56. D. 0,78; 0,54; 1,12
Đọc tiếp
Chia hỗn hợp X gồm K, Al, Fe thành hai phần bằng nhau.
Cho phần 1 vào dung dịch KOH dư thu được 0,784 lít khí H2 (đktc).
Cho phần 2 vào một lượng dư H2O, thu được 0,448 lít khí H2 (đktc) và m gam hỗn hợp kim loại Y. Hòa tan hoàn toàn Y vào dung dịch HCl dư, thu được 0,56 lít khí H2 (đktc). Khối lượng (tính theo gam) của K, Al, Fe trong mỗi phần hỗn hợp X lần lượt là
A. 0,39; 0,54; 0,56
B. 0,39; 0,54; 1,40
C. 0,78; 1,08; 0,56.
D. 0,78; 0,54; 1,12
Hỗn hợp X gồm a mol Al và b mol Na. Hỗn hợp Y gồm b mol Al và a mol Na. Thực hiện 2 thí nghiệm sau:- Thí nghiệm 1: Hòa tan hỗn hợp X vào nước dư, thu được 5,376 lít khí
H
2
, dung dịch X1 và m gam chất rắn không tan. - Thí nghiệm 2: Hòa tan hỗn hợp Y vào nước dư, thu được dung dịch
Y
1
trong đó khối lượng NaOH là 1,2 gam. Biết thể tích khí đo ở đktc. Tổng khối lượng Al trong hỗn hợp X và Y là A. 6,75 gam. B...
Đọc tiếp
Hỗn hợp X gồm a mol Al và b mol Na. Hỗn hợp Y gồm b mol Al và a mol Na. Thực hiện 2 thí nghiệm sau:
- Thí nghiệm 1: Hòa tan hỗn hợp X vào nước dư, thu được 5,376 lít khí H 2 , dung dịch X1 và m gam chất rắn không tan.
- Thí nghiệm 2: Hòa tan hỗn hợp Y vào nước dư, thu được dung dịch Y 1 trong đó khối lượng NaOH là 1,2 gam. Biết thể tích khí đo ở đktc. Tổng khối lượng Al trong hỗn hợp X và Y là
A. 6,75 gam.
B. 7,02 gam.
C. 7,29 gam
D. 7,56 gam.
* T N 1 : A l : a m o l N a : b m o l → H 2 O N a A l O 2 : b m o l H 2 A l B T e : n N a + 3 . n P b = b + 3 b = 2 . n H 2 = 0 , 48 → b = 0 , 12 * T N 2 : A l : 0 , 12 m o l N a : a m o l → H 2 O N a A l O 2 : 0 , 12 m o l N a O H : 0 , 03 m o l + . . . a = n N a = n N a O H + n N a A l O 2 = 0 , 15 → n A l ( T N 1 , T N 2 ) = 0 , 27 m o l → m A l = 7 , 29 g
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Na, Al, Mg. Tiến hành 3 thí nghiệm sau: Thí nghiệm 1: Cho m gam X vào nước dư thu được V lít khí. Thí nghiệm 2: Cho 2m gam X vào dung dịch NaOH dư thu được 3,5V lít khí. Thí nghiệm 3: Hòa tan 4m gam X vào dung dịch HCl dư thu được 9V lít khí. Các thể tích đều đo ở đktc và coi như Mg không tác dụng với nước và kiềm. Phát biểu nào sau đây là đúng ? A. Số mol Al gấp 1,5 lần số mol Mg B. Trong X có 2 kim loại có số mol bằng nhau. C. Ở thí nghiệm 1, Al bị hòa tan hoàn toàn D. Phần t...
Đọc tiếp
Hỗn hợp X gồm Na, Al, Mg. Tiến hành 3 thí nghiệm sau:
Thí nghiệm 1: Cho m gam X vào nước dư thu được V lít khí.
Thí nghiệm 2: Cho 2m gam X vào dung dịch NaOH dư thu được 3,5V lít khí.
Thí nghiệm 3: Hòa tan 4m gam X vào dung dịch HCl dư thu được 9V lít khí.
Các thể tích đều đo ở đktc và coi như Mg không tác dụng với nước và kiềm. Phát biểu nào sau đây là đúng ?
A. Số mol Al gấp 1,5 lần số mol Mg
B. Trong X có 2 kim loại có số mol bằng nhau.
C. Ở thí nghiệm 1, Al bị hòa tan hoàn toàn
D. Phần trăm khối lượng của Na là 23,76%.
Đáp án B
Thí nghiệm 1 cho m gam X vào H2O thu được V lít khí còn khí cho 2m gam vào NaOH thì thu được 3,5V lít tương đương khi cho m gam X vào NaOH thu được 1,75V lít.Do vậy trong X số mol Al nhiều hơn Na.
Gọi số mol của Na trong m gam X là x, suy ra khi cho m gam X vào H2O thì Al dư, nên Al phản ứng theo Na.
→ n H 2 = x + 3 x 2 = 2 x
Khi cho m gam X tác dụng với NaOH thu được 1,75V lít khí tức 3,5x mol khí. Lúc này cả Al và Na đều hết.
→ n A l = 3 , 5 x . 2 - x 3 = 2 x
Mặt khác cho 4m gam X vào HCl thu được 9V lít hay cho m gam X vào HCl thì thu được 2,25V lít hay 4,5x mol khí.
→ n M g = 4 , 5 x . 2 - x - 2 x . 3 2 = x
Vậy số mol Mg và Na bằng nhau
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Na, Al, Mg. Tiến hành 3 thí nghiệm sau: Thí nghiệm 1: Cho m gam X vào nước dư thu được V lít khí. Thí nghiệm 2: Cho 2m gam X vào dung dịch NaOH dư thu được 3,5V lít khí. Thí nghiệm 3: Hòa tan 4m gam X vào dung dịch HCl dư thu được 9V lít khí. Các thể tích đều đo ở đktc và coi như Mg không tác dụng với nước và kiềm. Phát biểu nào sau đây là đúng? A. Số mol Al gấp 1,5 lần số mol Mg. B. Trong X có 2 kim loại có số mol bằng nhau. C. Ở thí nghiệm 1, Al bị hòa tan hoàn toàn D. Phần tr...
Đọc tiếp
Hỗn hợp X gồm Na, Al, Mg. Tiến hành 3 thí nghiệm sau:
Thí nghiệm 1: Cho m gam X vào nước dư thu được V lít khí.
Thí nghiệm 2: Cho 2m gam X vào dung dịch NaOH dư thu được 3,5V lít khí.
Thí nghiệm 3: Hòa tan 4m gam X vào dung dịch HCl dư thu được 9V lít khí.
Các thể tích đều đo ở đktc và coi như Mg không tác dụng với nước và kiềm. Phát biểu nào sau đây là đúng?
A. Số mol Al gấp 1,5 lần số mol Mg.
B. Trong X có 2 kim loại có số mol bằng nhau.
C. Ở thí nghiệm 1, Al bị hòa tan hoàn toàn
D. Phần trăm khối lượng của Na là 23,76%.
Đáp án B
Thí nghiệm 1 cho m gam X vào H2O thu được V lít khí còn khí cho 2m gam vào NaOH thì thu được 3,5V lít tương đương khi cho m gam X vào NaOH thu được 1,75V lít. Do vậy trong X số mol Al nhiều hơn Na.
Gọi số mol của Na trong m gam X là x, suy ra khi cho m gam X vào H2O thì Al dư, nên Al phản ứng theo Na.
→ n H 2 = x + 3 x 2 = 2 x
Khi cho m gam X tác dụng với NaOH thu được 1,75V lít khí tức 3,5x mol khí. Lúc này cả Al và Na đều hết.
→ n A l = 3 , 5 x . 2 - x 3 = 2 x
Mặt khác cho 4m gam X vào HCl thu được 9V lít hay cho m gam X vào HCl thì thu được 2,25V lít hay 4,5x mol khí
→ n M g = 4 , 5 x . 2 - x - 2 x . 3 2 = x
Vậy số mol Mg và Na bằng nhau.
Đúng 0
Bình luận (0)









