a) Nước cất có nồng độ H+ là \({10^{ - 7}}\) mol/L. Tính độ pH của nước cất.
b) Một dung dịch có nồng độ H+ gấp 20 lần nồng độ H+ của nước cất. Tính độ pH của dung dịch đó.
Nhắc lại rằng, độ pH của một dung dịch được tính theo công thức \(pH = - \log \left[ {{H^ + }} \right]\), trong đó [H+] là nồng độ H+ của dung dịch đó tính bằng mol/L. Nồng độ H+ trong dung dịch cho biết độ acid của dung dịch đó.
a) Dung dịch acid A có độ pH bằng 1,9; dung dịch acid B có độ pH bằng 25. Dung dịch nào có độ acid cao hơn và cao hơn bao nhiêu lần?
b) Nước cất có nồng độ H+ là 10 mol/L. Nước chảy ra từ một vòi nước có độ pH từ 6,5 đến 6,7 thì có độ acid cao hay thập hơn nước cất?
\(a,pH_A=1,9\Leftrightarrow-log\left[H^+\right]=1,9\Leftrightarrow H^+=10^{-1,9}\)
Vậy độ acid của dung dịch A là \(10^{-1,9}mol/L\)
\(pH_B=2,5\Leftrightarrow-log\left[H^+\right]=2,5\Leftrightarrow H^+=10^{-2,5}\)
Vậy độ acid của dung dịch B là \(10^{-2,5}mol/L\)
Ta có: \(\dfrac{H^+_A}{H_B^+}=\dfrac{10^{-1,9}}{10^{-2,5}}\approx398\)
Vậy độ acid của dung dịch A cao hơn độ acid của dung dịch B 3,98 lần.
b, Ta có:
\(6,5< pH< 6,7\\ \Leftrightarrow6,5< -log\left[H^+\right]< 6,7\\ \Leftrightarrow-6,7< log\left[H^+\right]< -6,5\\ \Leftrightarrow10^{-6,7}< H^+< 10^{-6,5}\)
Vậy nước chảy từ vòi nước có độ acid từ \(10^{-6,7}mol/L\) đến \(10^{-6,5}mol/L\)
Như vậy, nước đó có độ acid cao hơn nước cất.
Độ pH của một dung dịch được tính theo công thức pH=-log[H+] với [H+] là nồng độ ion H+ trong dung dịch đó. Cho dung dịch A có độ pH ban đầu bằng 6. Nếu nồng độ ion H+ trong dung dịch A tăng lên 4 lần thì độ pH trong dung dịch mới gần bằng giá trị nào dưới đây?
A. 5,2
B. 6,6
C. 5,7
D. 5,4
Độ pH của một dung dịch được tính theo công thức p H = - log H + với H + là nồng độ ion H + trong dung dịch đó. Cho dung dịch A có độ pH ban đầu bằng 6. Nếu nồng độ ion H + trong dung dịch A tăng lên 4 lần thì độ pH trong dung dịch mới gần bằng giá trị nào dưới đây?
A. 5,2
B. 6,6
C. 5,7
D. 5,4
Nhắc lại rằng, độ pH của một dung dịch được tính theo công thức \(pH = - \log x\), trong đó \(x\) là nồng độ ion H+ tính bằng mol/L.
Biết sữa có độ pH là 6,5. Nồng độ H+ của sữa bằng bao nhiêu?
tham khảo
Ta có:
\(pH=-logx\Leftrightarrow6,5=-logx\Leftrightarrow logx=-6,5\Leftrightarrow x=10^{-6,5}\approx3,16.10^{-77}\)
Vậy nồng độ \(H^+\) của sữa bằng \(3,16.10^{-7}\) mol/L.
Ta đã biết, độ pH của một dung dịch được xác định bởi \(pH = - \log \left[ {{H^ + }} \right],\) ở đó \(\left[ {{H^ + }} \right]\) là nồng độ (mol/l) của hydrogen. Tính tốc độ thay đổi của pH với nồng độ \(\left[ {{H^ + }} \right]\).
Với \(pH=-log\left[H^+\right]\),ta có:
\(\dfrac{dpH}{d\left[H^+\right]}=\dfrac{d}{d\left[H^+\right]}\left(-log\left[H^+\right]\right)\)
Sử dụng quy tắc tính đạo hàm của hàm hợp, ta có:
\(\dfrac{dpH}{d\left[H^+\right]}=-1.\dfrac{d}{d\left[H^+\right]}\left(log\left[H^+\right]\right)\)
Áp dụng công thức đạo hàm của hàm số logarit tổng quát, ta có:
\(\dfrac{dpH}{d\left[H^+\right]}=-1.\dfrac{1}{\left[H^+\right]ln10}\)
Vậy tốc độ thay đổi của \(pH\) đối với nồng độ \(\left[H^+\right]\) là:
\(\dfrac{dpH}{d\left[H^+\right]}=-\dfrac{1}{\left[H^+\right]ln10}\)
Có 16ml dung dịch HCl nồng độ a mol/l( gọi là dung dịch A). Thêm nước cất vào dung dịch A cho đến khi thể tích dung dịch là 200ml, lúc này CM của dung dịch là 0,1M. Tính A?
nHCl = 0,2 . 0,1 = 0,02 (mol)
\(a=\dfrac{nHCl}{C_MHCl}=\dfrac{0,02}{0,016}=1,25M\)
Cân 10,6g muối N a 2 C O 3 cho vào cốc chia độ. Rót vào cốc khoảng vài chục ml nước cất, khuấy cho muối tan hết. Sau đó rót thêm nước vào cốc cho đủ 200ml. Ta được dung dịch N a 2 C O 3 có khối lượng riêng là 1,05g/ml. Hãy tính nồng độ phần trăm và nồng độ mol của dung dịch vừa pha chế.
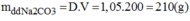
Nồng độ phần trăm của dung dịch pha chế:
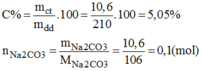
Nồng độ mol của dung dịch:
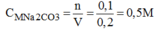
Chỉ số hay độ pH của một dung dịch được tính theo công thức: \(pH = - \log [{H^ + }]\) (Trong đó \([{H^ + }]\) chỉ nống độ hydrogen). Đo chỉ số pH của một mẫu nước sông, ta có kết quả là pH = 6,1.
a) Viết phương trình thể hiện nồng độ x của ion hydrogen \([{H^ + }]\) trong mẫu nước sông đó.
b) Phương trình vừa tìm được có ẩn là gì và nằm ở vị trí nào của lôgarit?
a) Ta có:\(-\log\left[H^+\right]=6.1\Leftrightarrow-\log x=6,1\)
b) Phương trình vừa tìm được có ẩn là x và nằm ở vị trí hệ số của logarit
a) Lấy chính xác 100ml dd H2SO4 0,2M và cho nước cất đến vạch 250ml. Tính nồng độ đương lượng của dung dịch mới và số gam H2SO4 có trong 10 ml dung dịch này. b) Tính nồng độ dung dịch HNO3 thu được khi trộn: • 500 g HNO3 10 % với 300 g HNO3 20% • 600 ml HNO3 2 N với 200 ml HNO3 4 N