Enthalpy tạo thành của H2O2 là -133 kJ mol-1, năng lượng liên kết O![]() H là 463 kJ mol-1 và năng lượng phân ly H2, O2 lần lượt là 436 và 495 kJ mol-1. Tính năng lượng liên kết O
H là 463 kJ mol-1 và năng lượng phân ly H2, O2 lần lượt là 436 và 495 kJ mol-1. Tính năng lượng liên kết O![]() O trong H2O2
O trong H2O2

Những câu hỏi liên quan
d) Cho biết năng lượng liên kết trong các phân tử O2, N2 và NO lần lượt là 494 kJ/mol, 945
kJ/mol và 607 kJ/mol. Biến thiên enthalpy chuẩn của phản ứng dưới đây bằng bao nhiêu?
N2(g) + O2(g) 2NO(g)
A. -832 kJ. B. +832 kJ. C. -225 kJ. D. +225 kJ.
\(\Delta_rH^{^o}_{298}=945+494-2\cdot607=+225kJ\\ \Rightarrow D\)
Đúng 1
Bình luận (0)
Biết năng lượng liên kết của phân tửCl2là 243 kJ mol-1, năng lượng ion hoá thứ nhất của nguyên tử Cl và phân tử Cl2 lần lượt là 1 250 và 1 085 kJ mol-1. Tính năng lượng liên kết của Cl2 + và thảo luận tiểu phân nào (Cl2, Cl2 +) có liên kết dài hơn. Giải thích.
Đọc tiếp
Biết năng lượng liên kết của phân tửCl2là 243 kJ mol-1, năng lượng ion hoá thứ nhất của nguyên tử Cl và phân tử Cl2 lần lượt là 1 250 và 1 085 kJ mol-1. Tính năng lượng liên kết của Cl2 + và thảo luận tiểu phân nào (Cl2, Cl2 +) có liên kết dài hơn. Giải thích.
Ta có hai sơ đồ ứng với quá trình:
\(Cl_2->2Cl->Cl^+,Cl\\ Cl_2->Cl_2^+->Cl^+,Cl\)
Theo nguyên lý I của nhiệt động học:
\(E_{b\left(Cl_2\right)}+IE_{Cl}=IE_{Cl_2}+E_{b\left(Cl_2^+\right)}\\ E_{b\left(Cl_2^+\right)}=243+1250-1085=408kJ\cdot mol^{-1}\\ E_{b\left(Cl_2^+\right)}>E_{b\left(Cl_2\right)}\)
Vì \(Cl_2^+\) có ít hơn một e phản liên kết so với Cl2, bậc liên kết cao hơn (1.5), do đó tiểu phân \(Cl_2\) có liên kết dài hơn.
Đúng 1
Bình luận (0)
Năng lượng liên kết của liên kết C – C (trong phân tử ethane) là 368 kJ mol-1 và năng lượng liên kết của liên kết C = C (trong phân tử ethene) là 636 kJ mol-1. Hãy cho biết liên kết nào (σ hay π) dễ bị bẻ gãy hơn khi phân tử tham gia phản ứng.
Liên kết đơn C – C có gồm 1 liên kết σ có năng lượng là 368 kJ mol-1.
Liên kết đôi C = C gồm 1 liên kết σ và liên kết π có năng lượng là 636 kJ mol-1.
=> Năng lượng của liên kết π là: 636 – 368 = 268 (kJ mol-1)
Vì năng lượng của liên kết σ (368 kJ mol-1) lớn hơn năng của liên kết π (268 kJ mol-1) nên khi phân tử tham gia phản ứng, liên kết π dễ bị bẻ gãy hơn.
Đúng 0
Bình luận (0)
c) Tính biến thiên enthanpy của phản ứng tạo thành ammonia (sử dụng năng lượng liên kết).
Cho biết phản ứng thu nhiệt hay toả nhiệt và vẽ sơ đồ biểu diễn biến thiên enthalpy của phản
ứng 3H2 (g) + N2 (g) → 2NH3 (g)
Liên kết Eb (kJ/ mol)
H – N 386
H – H 436
N ≡ N 945
\(\Delta_rH^{^{ }o}_{298}=3\cdot436+945-2\left(3\cdot386\right)=-63kJ\cdot mol^{-1}\)
Sơ đồ:
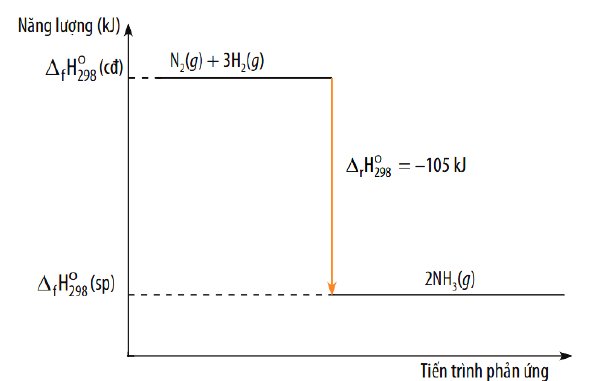
Đúng 1
Bình luận (0)
tính ∆h 298 của phản ứng sau: c2h2(k) + 2h2(k) = c2h6(k) cho biết năng lượng liên kết ở điều kiện chuẩn, 25oc. e (c-c) = 347.3 kj/mol e (c-h) = 412.9 kj/mol e (h-h) = 435.5 kj/mol e (c≡c) = 810.9 kj/mol
Đốt cháy butane (CH3-CH2-CH2-CH3) bằng oxygen tạo sản phẩm là carbon dioxide và nước.Năng lượng liên kết trong các hợp chất cho trong bảng dưới đây:Liên kết Phân tử Eb (kJ/mol) Liên kết Phân tử Eb (kJ/mol)C – C C4H10 346 C O CO2 799C – H C4H10 418 O – H H2O 467O O O2 495Một bình gas chứa 12 kg butane có thể đun sôi bao nhiêu ấm nước? Giả thiết mỗi ấm nướcchứa 3 L nước ở 250C, nhiệt dung của nước là 4,2 J/g.K, có 50% nhiệt đốt...
Đọc tiếp
Đốt cháy butane (CH3-CH2-CH2-CH3) bằng oxygen tạo sản phẩm là carbon dioxide và nước.
Năng lượng liên kết trong các hợp chất cho trong bảng dưới đây:
Liên kết Phân tử Eb (kJ/mol) Liên kết Phân tử Eb (kJ/mol)
C – C C4H10 346 C = O CO2 799
C – H C4H10 418 O – H H2O 467
O = O O2 495
Một bình gas chứa 12 kg butane có thể đun sôi bao nhiêu ấm nước? Giả thiết mỗi ấm nước
chứa 3 L nước ở 250C, nhiệt dung của nước là 4,2 J/g.K, có 50% nhiệt đốt cháy butane bị thất
thoát ra ngoài môi trường.
\(C_4H_{10}\left(g\right)+\dfrac{13}{2}O_2\left(g\right)->4CO_2\left(g\right)+5H_2O\left(l\right)\\ \Delta_rH^o_{298}=4\cdot346+10\cdot418+\dfrac{13}{2}\cdot495-\left(4\cdot2\cdot799+10\cdot467\right)=-2280,5kJ\cdot mol^{-1}\\ Q=\dfrac{12\cdot10^3}{58}\cdot2280,5=4,71\cdot10^5kJ=4,71\cdot10^8J\\ 4,71\cdot10^8\cdot0,5=N_{ấm}\cdot3000\cdot75\cdot4,2\\ N_{ấm}=249,6\)
Vậy có thể đun sôi tối đa 249 ấm nước.
Đúng 1
Bình luận (0)
khí thiên nhiên có thành phần theo thể tích gồm 90% CH4 2% C2H6 8% CO2 và N2 tính nhiệt lượng tỏa ra khi đốt cháy 0,5m3 khí thiên nhiên biết hiệu suất là 95% và năng suất tỏa nhiệt của CH4 C2H6 lần lượt là 880 kJ/mol và 1.560 kJ/mol
Cho phản ứng sau ở điều kiện chuẩn:
H-H(g) + F-F(g) -> 2H-F(g)
Tính năng lượng cần để phá vỡ các liên kết trong H2, F2 và năng lượng tỏa ra (theo kJ) khi hình thành liên kết trong HF cho phản ứng trên.
∆r\(H^o_{298}\) = EH-H + EF-F – 2.FH-F
∆r\(H^o_{298}\) = 436 + 159 – 2.565 = -535 kJ
Đúng 0
Bình luận (0)
Xét phản ứng trong giai đoạn đầu của quá trình Ostwald:4NH3(g) + 5O2(g) (Pt, t°) → 4NO(g) + 6H2O(g)a) Tính ΔrH^0_{298} của phản ứng trên và cho biết phản ứng là toả nhiệt hay thu nhiệt? Có thể tận dụng nhiệt lượng này để làm gì?Biết nhiệt tạo thành chuẩn của NH3(g), NO(g) và H2O(g) lần lượt là -45,9 kJ/mol; 90,3 kJ/mol và -241,8 kJ/mol.b) Tính năng lượng liên kết trong phân tử NO. Biết năng lượng liên kết N─H, O═O, O─H lần lượt là 386 kJ/mol, 494 kJ/mol và 459 kJ/mol.
Đọc tiếp
Xét phản ứng trong giai đoạn đầu của quá trình Ostwald:
4NH3(g) + 5O2(g) (Pt, t°) → 4NO(g) + 6H2O(g)
a) Tính Δ\(rH^0_{298}\) của phản ứng trên và cho biết phản ứng là toả nhiệt hay thu nhiệt? Có thể tận dụng nhiệt lượng này để làm gì?
Biết nhiệt tạo thành chuẩn của NH3(g), NO(g) và H2O(g) lần lượt là -45,9 kJ/mol; 90,3 kJ/mol và -241,8 kJ/mol.
b) Tính năng lượng liên kết trong phân tử NO. Biết năng lượng liên kết N─H, O═O, O─H lần lượt là 386 kJ/mol, 494 kJ/mol và 459 kJ/mol.












