Cho 10,8 gam kim loại X tan hoàn toàn trong ddH2SO4 loãng dư. Sau thí nghiệm khối lượng dung dịch tăng thêm 9,6 gam. Xác định tên kim loại X?

Những câu hỏi liên quan
Câu 4: Cho 10,8 gam kim loại X tan hoàn toàn trong ddH2SO4 loãng dư. Sau thí nghiệm khối lượng dung dịch tăng thêm 9,6 gam. Xác định tên kim loại X?
Cho 9,6 gam hỗn hợp X gồm canxi và kim loai R (hóa trị II) tan hoàn toàn trong dung dịch H2SO4 loãng thu được 6,72 lit khí ( đktc). Xác định kim loại R
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: Ca + H2SO4 → CaSO4 + H2
PTHH: R + H2SO4 → RSO4 + H2
\(\Rightarrow M_X=\dfrac{9,6}{0,3}=32\left(g/mol\right)\)
Mà \(M_X=\dfrac{M_{Ca}+M_R}{2}=\dfrac{40+M_R}{2}\)
\(\Rightarrow\dfrac{40+M_R}{2}=32\Leftrightarrow40+M_R=64\Leftrightarrow M_R=24\)
Vậy R là kim loại magie (Mg)
Đúng 0
Bình luận (0)
Cho 16,8 gam một kim loại R hóa trị 2 tan hoàn toàn trong dung dịch H2SO4 loãng thu được 6,72 lít khí (điều kiện tiêu chuẩn).Xác định tên kim loại ( R) và khối lượng muối thu được.
$R + H_2SO_4 \to RSO_4 + H_2$
$n_R = n_{H_2} = \dfrac{6,72}{22,4} = 0,3(mol)$
$M_R = \dfrac{16,8}{0,3} =56(Fe)$
Vậy R là Sắt
$n_{FeSO_4} = n_{H_2} = 0,3(mol)$
$m_{FeSO_4} = 0,3.152 =45,6(gam)$
Đúng 1
Bình luận (0)
1) Xác định tên kim loại A và M khi:a) Hòa tan hoàn toàn 2,7 gam kim loại A (hóa trị III) trong dung dịch HCl dư sau phản ứng thu được 13,35 gam muối.b) Hòa tan hoàn toàn 4,8 gam kim loại M trong dung dịch HCl dư sau phản ứng thu được 4,48 lit khí (đktc).
Đọc tiếp
1) Xác định tên kim loại A và M khi:
a) Hòa tan hoàn toàn 2,7 gam kim loại A (hóa trị III) trong dung dịch HCl dư sau phản ứng thu được 13,35 gam muối.
b) Hòa tan hoàn toàn 4,8 gam kim loại M trong dung dịch HCl dư sau phản ứng thu được 4,48 lit khí (đktc).
\(a,n_A=\dfrac{2,7}{M_A}\left(mol\right)\\ n_{ACl_3}=\dfrac{13,35}{M_A+106,5}\)
PTHH: \(2A+6HCl\rightarrow2ACl_3+3H_2\)
\(\dfrac{2,7}{M_A}\)-------------->\(\dfrac{2,7}{M_A}\)
\(\rightarrow\dfrac{2,7}{M_A}=\dfrac{13,35}{M_A+106,5}\\ \Leftrightarrow M_A=27\left(g\text{/}mol\right)\)
=> A là Al
\(b,n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: \(2M+2nHCl\rightarrow2MCl_n+nH_2\) (n là hoá trị của M, n ∈ N*)
\(\dfrac{0,4}{n}\)<---------------------------0,2
\(\rightarrow M_M=\dfrac{4,8}{\dfrac{0,2}{n}}=12n\left(g\text{/}mol\right)\)
Vì n là hoá trị của M nên ta có bảng
| n | 1 | 2 | 3 |
| MM | 12 | 24 | 36 |
| Loại | Mg | Loại |
Vậy M là Mg
Đúng 1
Bình luận (0)
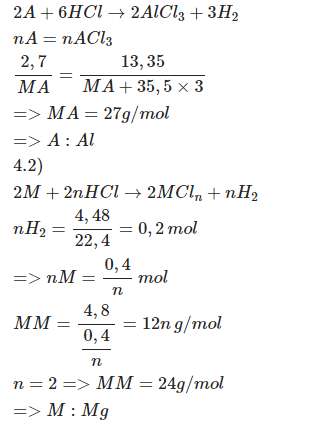
\(\Rightarrow\) \(M:mg\)
Câu4:Cho 2,7 gam kim loại A(hoá trịIll)Tan hoàn toàn trong dung dịch axit sunfuric Loãng dư thu được muối và 3,36lít khí hiđrô(đktc) a)Xác định kim loại A b)Tính khối lượng muối tạo thành
\(n_{H_2\left(dktc\right)}=\dfrac{V}{22,4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ PTHH:2A+3H_2SO_4->A_2\left(SO_4\right)_3+3H_2\)
tỉ lệ 2 : 3 : 1 : 3
n(mol) 0,1<------0,15<------------0,05<-------0,15
\(=>M_A=\dfrac{m}{n}=\dfrac{2,7}{0,1}=27\left(g/mol\right)\)
`=>A` là nhôm
`=>` muối là `Al_2 (SO_4)_3`
\(m_{Al_2\left(SO_4\right)_3}=n\cdot M=0,05\cdot342=17,1\left(g\right)\)
Đúng 3
Bình luận (0)
a, \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PT: \(2A+3H_2SO_4\rightarrow A_2\left(SO_4\right)_3+3H_2\)
Theo PT: \(n_A=\dfrac{2}{3}n_{H_2}=0,1\left(mol\right)\Rightarrow M_A=\dfrac{2,7}{0,1}=27\left(g/mol\right)\)
→ A là nhôm.
b, Theo PT: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{3}n_{H_2}=0,05\left(mol\right)\Rightarrow m_{Al_2\left(SO_4\right)_3}=0,05.342=17,1\left(g\right)\)
Đúng 3
Bình luận (0)
Để hòa tan hoàn toàn 10,8 gam một kim loại nhóm IIIA phải dùng hết 294 gam dung dịch axit sunfuric 20%. Xác định tên kim loại.
\(n_{H_2SO_4}=\dfrac{294.20}{100.98}=0,6\left(mol\right)\)
PTHH: 2R + 3H2SO4 --> R2(SO4)3 + 3H2
_____0,4<---0,6
=> \(M_R=\dfrac{10,8}{0,4}=27\left(g/mol\right)=>Al\)
Đúng 1
Bình luận (0)
. X, Y là hai kim loại có electron cuối cùng là 3p1 và 3d6. a. Dựa vào bảng tuần hoàn, hãy xác định tên hai kim loại X, Y. b. Hòa tan hết 8,3 gam hỗn hợp X, Y vào dung dịch HCl 0,5M (vừa đủ), ta thấy khối lượng dung dịch sau phản ứng tăng thêm 7,8 gam. Tính khối lượng mỗi kim loại và thể tích dung dịch HCl đã dùng.
Dựa vào bảng tuần hoàn ta tìm được X là Al và Y là Fe.
Gọi số mol các chất trong hỗn hợp: Al = a( mol); Fe = b (mol).
Ta có: 27a + 56b = 8,3 (1)
2Al + 6HCl → 2AlCl3 + 3H2 (2)
a 3a 1,5a
Fe + 2HCl → FeCl2 + H2 (3)
b 2b b
Khối lượng dung dịch sau phản ứng tăng thêm 7,8 gam nên: 8,3 - mH2 = 7,8.
Vậy: mH2 = 0,5 gam → nH2 = 0,25 mol → 1,5a + b = 0,25 (4)
Từ (1) và (4) ta tìm được: a = 0,1 mol; b = 0,1 mol.
mAl = 27.0,1 = 2,7 (gam)
mFe = 56.0,1 = 5,6 (gam);
VHCl = (3a + 2b) : 0,5 = 1 (lit).
Đúng 1
Bình luận (1)
Cho y gam kim loại M vào dung dịch F e 2 S O 4 3 dư, sau phản ứng hoàn toàn khối lượng phần dung dịch tăng thêm y gam. Kim loại M là
A. Ba
B. Cu
C. K
D. Ag
Đáp án B
Do thêm kim loại M vào dung dịch F e 2 S O 4 3 , khối lượng dung dịch tăng đúng bằng khối lượng kim loại phản ứng nên sau phản ứng không thu được kết tủa cũng không có khí thoát ra.
Vậy M là Cu.
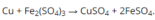
Đúng 0
Bình luận (0)
Cho y gam kim loại M vào dung dịch F e 2 S O 4 3 dư, sau phản ứng hoàn toàn khối lượng phần dung dịch tăng thêm y gam. Kim loại M là
A. Ba.
B. Cu.
C. K.
D. Ag.
Đáp án B
Do thêm kim loại M vào dung dịch F e 2 S O 4 3 , khối lượng dung dịch tăng đúng bằng khối lượng kim loại phản ứng nên sau phản ứng không thu được kết tủa cũng không có khí thoát ra.
Vậy M là Cu
![]()
Đúng 0
Bình luận (0)























