Cho hỗn hợp chất rắn gồm 2,8 gam Fe và 4 gam CuO phản ứng vừa đủ với 200ml dung dịch HCL
a)Viết PTHH
b)Tình thể tích khí H2 sinh ra
c)Tìm nồng độ mol HCL đã dùng
Cho 14 gam hỗn hợp X gồm CuO và Fe vào 200 ml dung dịch HCl thấy thoát ra 2,8 lít khí H 2 (đktc) và có 1,6 gam chất rắn chỉ có một kim loại. Biết rằng dung dịch sau phản ứng chỉ chứa 2 muối. Nồng độ mol của dung dịch HCl đã dùng là
A. 1,95M
B. 1.725M
C. 1,825M
D. 1.875M.
Cho hỗn hợp Y gồm 2,8 gam Fe và 0,81 gam Al vào 200ml dung dịch C chứa AgNO3 và Cu(NO3)2. Khi phản ứng kết thúc, thu được dung dịch D và 8,12 gam chất rắn E gồm 3 kim loại. Cho chất rắn E tác dụng với dung dịch HCl dư thì thu được 0,672 lít khí H2 (đktc). Nồng độ mol của AgNO3 và Cu(NO3)2 trong dung dịch C lần lượt là:
A. 0,15M và 0,25M
A. 0,15M và 0,25M
C. 0,3M và 0,5M.
D. 0,15M và 0,5M.
Chọn đáp án A
![]()
⇒ E gồm 3 kim loại thì đó là Ag, Cu và Fe dư ⇒ nFe dư = nH2 = 0,03 mol
Đặt n A g + = x mol; n C u 2 + = y mol ||→ mE = 8,12 gam = 108x + 64y + 0,03 × 56
![]()
![]()
Giải hệ có: x = 0,03 mol; y = 0,05 mol
![]()
Cho hỗn hợp Y gồm 2,8 gam Fe và 0,81 gam Al vào 200ml dung dịch C chứa AgNO3 và Cu(NO3)2. Khi phản ứng kết thúc, thu được dung dịch D và 8,12 gam chất rắn E gồm 3 kim loại. Cho chất rắn E tác dụng với dung dịch HCl dư thì thu được 0,672 lít khí H2 (đktc). Nồng độ mol của AgNO3 và Cu(NO3)2 trong dung dịch C lần lượt là:
A. 0,15M và 0,25M
B. 0,075M và 0,0125M.
C. 0,3M và 0,5M.
D. 0,15M và 0,5M.
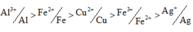
⇒ E gồm 3 kim loại thì đó là Ag, Cu và Fe dư
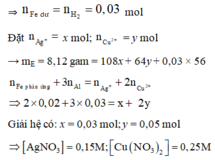
Đáp án A
Cho 6,5 gam Zn phản ứng vừa đủ với 200ml dung dịch axit clohiđric HCl. Sinh ra kẽm clorua (ZnCl2) và khí hiđrô.
a. Tính thể tích khí H2 sinh ra ở đktc.
b. Tính nồng độ mol dung dịch HCl đã dùng.
c. Tính nồng độ mol dung dịch thu được sau phản ứng (giả sử thể tích dung dịch thay đổi không đáng kể).
a, \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH: Zn + 2HCl ---> ZnCl2 + H2
0,1--->0,2------->0,1----->0,1
VH2 = 0,1.22,4 = 2,24 (l)
b, \(C_{M\left(HCl\right)}=\dfrac{0,2}{0,2}=1M\)
c, \(C_{M\left(ZnCl_2\right)}=\dfrac{0,1}{0,2}=0,5M\)
Cho hỗn hợp (Y) gồm 2,8 gam Fe và 0,81 gam Al vào 200ml dung dịch (C) chứa AgNO3 và Cu(NO3)2. Kết thúc phản ứng thu được dung dịch (D) và 8,12 gam chất rắn (E) gồm ba kim loại. Cho (E) tác dụng với dung dịch HCl dư, ta thu được 0,672 lít H2 (đktc). Tính nồng độ mol/l AgNO3, Cu(NO3)2 trước khi phản ứng.
![]()
![]()
![]()
![]()
Đáp án A.
Vì phản ứng giữa Al và AgNO3 xảy ra trước nên kim loại sau phản ứng phải có Ag, kế đến là CuSO4 có phản ứng tạo thành Cu. Theo giả thiết, có ba kim loại → kim loại thứ ba là Fe còn dư.
Ta có: nFe = 2,8/5,6 = 0,05 (mol)
nAl = 0,81/27 = 0,03 (mol)
và = 0,672/22,4 = 0,03 (mol)
Phản ứng: Fedư + 2HCl → FeCl2 + H2
(mol) 0,03 0,03
→ Số mol Fe phản ứng với muối: 0,05 – 0,03 = 0,02 (mol)
2Al + 3Cu2+ → 2Al3+ + 3Cu
Fe + 2Ag+ → Fe2+ + 2Ag
Fe + Cu2+ → Fe2+ + Cu
Ta có sự trao đổi electron như sau:
Al → Al3+ + 3e Fe → Fe2+ + 2e
0,03 0,09 (mol) 0,02 0,04 (mol)
Ag+ + 1e → Ag Cu2+ + 2e → Cu
x x x (mol) y 2y y (mol)
→ x + 2y = 0,09 + 0,04 = 0,13 (1) ; 108x + 64y + 56.0,03 = 8,12 (2)
Giải hệ phương trình (1) và (2), ta được x = 0,03; y = 0,05.
Vậy:

Hoà tan hoàn toàn 57,6 gam hỗn hợp X gồm , Fe 2 O 3 , FeO và Fe trong dung dịch HCl thì cần dùng 360 gam dung dịch HCl 18,25% để tác dụng vừa đủ. Sau phản ứng thu được V lít khí H 2 và dung dịch Y.
Cho toàn bộ H 2 sinh ra tác dụng hết với CuO dư ở nhiệt độ cao, sau phản ứng thu được hỗn hợp rắn gồm Cu và CuO có khối lượng nhỏ hơn khối lượng CuO ban đầu là 3,2 gam. Nếu cô cạn dung dịch Y thì thu được bao nhiêu gam muối khan ?
n HCl = 360 x 18,25/(100x36,5) = 1,8 mol
H 2 + CuO → t ° Cu + H 2 O
n CuO = x
Theo đề bài
m CuO (dư) + m Cu = m CuO (dư) + m Cu p / u - 3,2
m Cu = m Cu p / u - 3,2 => 64x = 80x - 3,2
=> x= 0,2 mol → m H 2 = 0,4g
Fe + 2HCl → FeCl 2 + H 2
Số mol HCl tác dụng với Fe 3 O 4 , Fe 2 O 3 , FeO là 1,8 - 0,4 = 1,4 mol
Phương trình hóa học của phản ứng:
Fe 3 O 4 + 8HCl → 2 FeCl 3 + FeCl 2 + 4 H 2 O (1)
Fe 2 O 3 + 6HCl → 2 FeCl 3 + 3 H 2 O (2)
FeO + 2HCl → FeCl 2 + H 2 O (3)
Qua các phản ứng (1), (2), (3) ta nhận thấy n H 2 O = 1/2 n HCl = 1,4:2 = 0,7 mol
Áp dụng định luật bảo toàn khối lượng, ta có:
m hỗn hợp + m HCl = m muối + m H 2 O + m H 2
57,6 + 1,8 x 36,5 = m muối + 0,7 x 18 +0,4
m muối = 57,6 + 65,7 - 12,6 - 0,4 = 110,3 (gam)
Nung hỗn hợp gồm 5,6 gam sắt và 1,6 gam lưu huỳnh trong điều kiện không có không khí. Sau phản ứng thu được hỗn hợp chất rắn A. Cho dung dịch HCl 0,5M phản ứng vừa đủ với chất rắn A thu được hỗn hợp khí B. Thể tích dung dịch HCl 0,5M đã dùng là
A. 100 ml
B. 200 ml
C. 300 ml
D. 400 ml
Câu 10. Hòa tan hoàn toàn 8,3 gam hỗn hợp Al và Fe bằng dung dịch HCl 0,2M (vừa đủ), sau phản ứng thu được 5,6 lít khí H2 và dung dịch X.
a. Tính thể tích dung dịch HCl đã dùng.
b. Tính nồng độ mol/l của dung dịch sau phản ứng
\(Đặt:n_{Al}=a\left(mol\right),n_{Fe}=b\left(mol\right)\)
\(m_{hh}=27a+56b=8.3\left(g\right)\left(1\right)\)
\(n_{H_2}=\dfrac{5.6}{22.4}=0.25\left(mol\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Tathấy:\)
\(n_{HCl}=2n_{H_2}=2\cdot0.25=0.5\left(mol\right)\)
\(V_{ddHCl}=\dfrac{0.5}{0.2}=2.5\left(l\right)\)
\(n_{H_2}=1.5a+b=0.25\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=b=0.1\)
\(C_{M_{AlCl_3}}=\dfrac{0.1}{2.5}=0.04\left(M\right)\)
\(C_{M_{FeCl_2}}=\dfrac{0.1}{2.5}=0.04\left(M\right)\)
Chúc em học tốt !!!
a, Ta có: \(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
BTNT H, có: \(n_{HCl}=2n_{H_2}=0,5\left(mol\right)\)
\(\Rightarrow V_{HCl}=\dfrac{0,5}{0,2}=2,5\left(l\right)\)
b, Giả sử: \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
⇒ 27x + 56y = 8,3 (1)
Các quá trình:
\(Al^0\rightarrow Al^{+3}+3e\)
x___________ 3x (mol)
\(Fe^0\rightarrow Fe^{+2}+2e\)
y____________2y (mol)
\(2H^++2e\rightarrow H_2^0\)
______0,5__0,25 (mol)
Theo ĐLBT mol e, có: 3x + 2y = 0,5 (2)
Từ (1) và (2) ⇒ x = y = 0,1 (mol)
BTNT Al và Fe, có: \(\left\{{}\begin{matrix}n_{AlCl_3}=n_{Al}=0,1\left(mol\right)\\n_{FeCl_3}=n_{Fe}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow C_{M_{AlCl_3}}=C_{M_{FeCl_3}}=\dfrac{0,1}{2,5}=0,04M\)
Bạn tham khảo nhé!
Cho 4,8 gam Magie tác dụng vừa đủ với 200ml dung dịch HCl. a. Tính nồng độ mol của dung dịch HCl đã dùng ? b. Cho toàn bộ lượng khí H2 thu được ở trên qua bình đựng 32g bột CuO nung nóng thu được m gam chất rắn. Tính phần trăm khố lượng các chất trong m ?
\(n_{Mg}=\dfrac{4.8}{24}=0.2\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(0.2.......0.4........................0.2\)
\(C_{M_{HCl}}=\dfrac{0.4}{0.2}=2\left(M\right)\)
\(n_{CuO}=\dfrac{32}{80}=0.4\left(mol\right)\)
\(CuO+H_2\underrightarrow{^{^{t^0}}}Cu+H_2O\)
Lập tỉ lệ : \(\dfrac{0.4}{1}>\dfrac{0.2}{1}\)
=> CuO dư
\(m_{cr}=m_{CuO\left(dư\right)}+m_{Cu}=32-0.2\cdot80+0.2\cdot64=28.8\left(g\right)\)
\(\%Cu=\dfrac{0.2\cdot64}{28.8}\cdot100\%=44.44\%\)
\(\%CuO\left(dư\right)=55.56\%\)