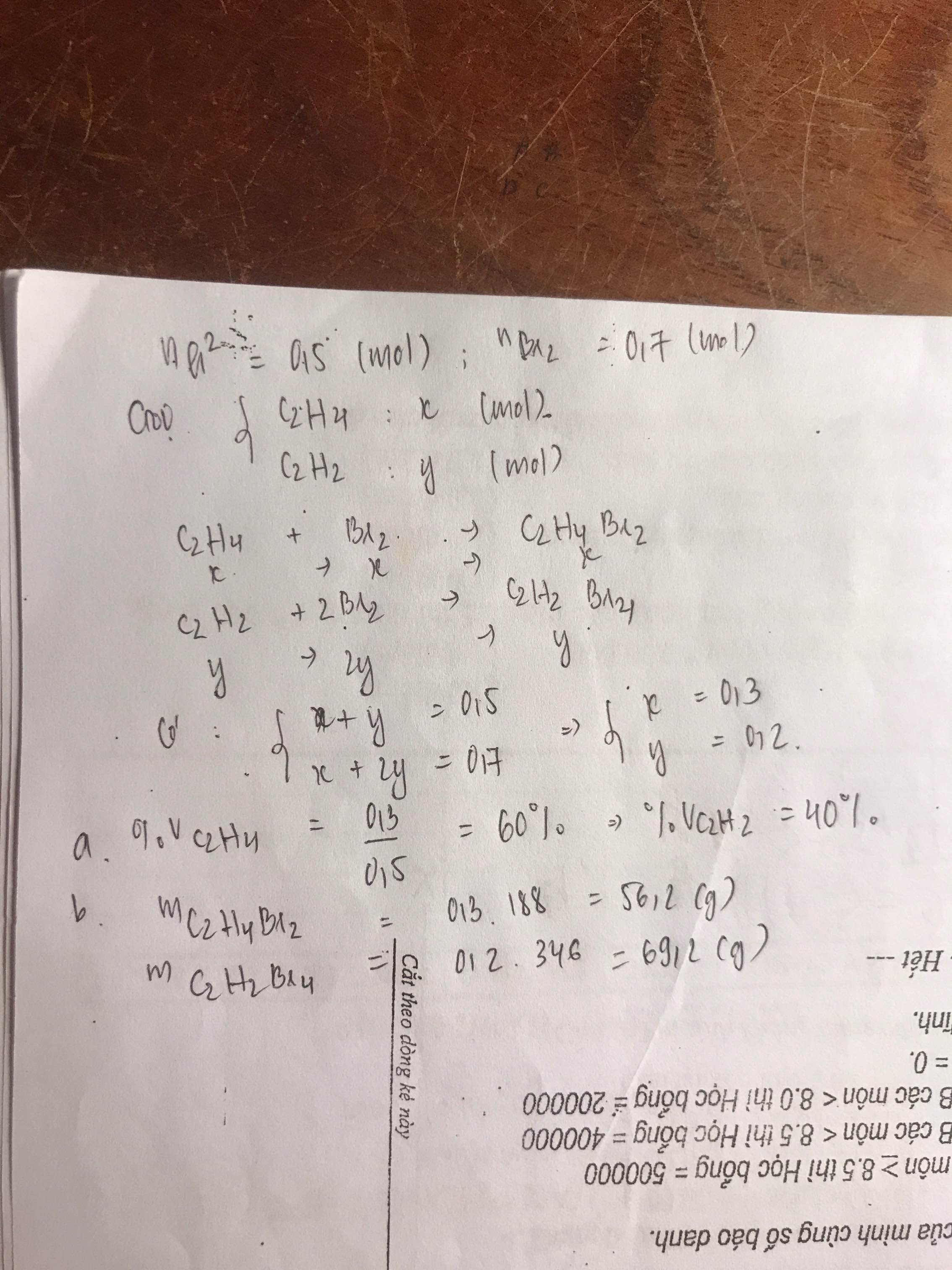Cho 6,72l hỗn hợp gồm Metan và axetilen tác dụng với dung dịch Brom sao phản ứng thấy khối lượng Brom tăng lên 2,8gam a) viết pt hoá học xảy ra b)tính % thể tích hỗn hợp ban đầu

Những câu hỏi liên quan
cho 5,6 lít hỗn hợp khí ( đktc) gồm metan và axetilen tác dụng với 100ml dung dịch brom vừa đủ sau phản ứng thấy khối lượng dung dịch brom tăng 2,6gam
A) tính % thể tích mỗi khí trong hỗn hợp
B) tính nòng độ mol của dung dịch brom đã dùng
a.\(m_{dd.Br_2\left(tăng\right)}=m_{C_2H_2}=2,6g\)
\(n_{hh}=\dfrac{5,6}{22,4}=0,25mol\)
\(n_{C_2H_2}=\dfrac{2,6}{26}=0,1mol\)
\(\%V_{C_2H_2}=\dfrac{0,1}{0,25}.100=40\%\)
\(\%V_{CH_4}=100\%-40\%=60\%\)
b.\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
0,1 0,2 ( mol )
\(C_{M\left(dd.Br_2\right)}=\dfrac{0,2}{0,1}=2M\)
Đúng 2
Bình luận (1)
Câu 3: Cho 3,36 lít hỗn hợp metan và axetilen sục vào dung dịch brom dư thấy có 2,4g brom tham gia phản ứng. a) Viết phương trình phản ứng hóa học xảy ra. b) Tính thể tích các khí trong hỗn hợp ban đầu biết các khí đo ở đktc. c) Tính % thể tích mỗi khí có trong hỗn hợp ban đầu?
\(n_{hh}=\dfrac{3,36}{22,4}=0,15mol\)
\(n_{Br_2}=\dfrac{2,4}{160}=0,015mol\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
0,0075 0,015 ( mol )
\(V_{C_2H_2}=0,0075.22,4=0,168l\)
\(V_{CH_4}=3,36-0,168=3,192l\)
\(\%V_{C_2H_2}=\dfrac{0,168}{3,36}.100=5\%\)
\(\%V_{CH_4}=100\%-5\%=95\%\)
Đúng 4
Bình luận (0)
Cho 11,2 lít hỗn hợp etilen và axetilen tác dụng với dung dịch brom dư thấy có 112 g brom phản ứng .
a/ Tính Phần trăm theo thể tích trong hỗn hợp ban đầu ?
b/ Tính khối lượng sản phảm sau phản ứng ?
GIÚP EM VỚI Ạ
Cho 7,84 lit hỗn hợp metan và etilen sục vào dung dịch brom dư thấy có 24g brom tham gia phản ứng.
a, Viết phương trình phản ứng hoá học xảy ra.
b, Tính % thể tích các khí trong hỗn hợp ban đầu, biết các khí đo ở đktc.
c. Tính khối lượng sản phẩm thu được
a, \(n_{hh}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
\(n_{Br2}=\dfrac{24}{160}=0,15\left(mol\right)\)
\(CH_2=CH_2+Br_2\rightarrow CH_2+CH_2\)
/Br /Br
0,15mol<----- 0,15mol
\(nC_2H_4=0,15\left(mol\right)\)
\(\Rightarrow nCH_3=0,35-0,15=0,2\left(mol\right)\)
\(\%VCH_4=\%nCH_4=\dfrac{0,2}{0,35}.100\%=57,14\%\)
\(\%VC_2H_4=100-57,14=42,86\%\)
Đúng 2
Bình luận (2)
Dẫn 11,2 lít khí (đktc) hỗn hợp A gồm metan và axetilen đi qua dung dịch brom, thấy có 48 gam brom tham gia phản ứng. a. Tính thành phần % thể tích trong hỗn hợp ban đầu b. Tính thể tích khí thoát ra ngoài
a, \(n_{Br_2}=\dfrac{48}{160}=0,3\left(mol\right)\)
PT: \(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
_____0,15____0,3 (mol)
\(\Rightarrow\%V_{C_2H_2}=\dfrac{0,15.22,4}{11,2}.100\%=30\%\)
\(\Rightarrow\%V_{CH_4}=100-30=70\%\)
b, - Khí thoát ra ngoài là CH4.
\(V_{CH_4}=11,2.70\%=7,84\left(l\right)\)
Đúng 1
Bình luận (1)
cho 11,3g hỗn hợp gồm metan,etilen,axetilen tác dụng vs brom dư thì k/lượng brom phản ứng là 72g.Mặt khác nếu cho toàn bộ hỗn hợp khí trên tác dụng vs 1 lượng dư bạcnitrat amoniac thu được 36g kết tủa
a) viết các pt xảy ra
b) tính % thể tích của các chất trong hỗn hợp ban đầu
Giup1 em vs...tks nkju ak
a) TN1: C2H4 + Br2---->C2H4Br2 (1) ,C2H2 + 2Br2----> C2H2Br4 (2), TN2: C2H2+ 2AgNO3+2NH3--->Ag2C2 +2NH4NO3 (3)
b) Đặt số mol: nC2H4=a(mol), nC2H2=b(mol), nCH4=c(mol). Theo TN2 và pt(3) => b=nAg2C2=36/MAg2C2=0,15(mol)=>mC2H2=3,9(gam).Theo TN1 và pt(1) và pt(2): a.160+ 2b.160=72 , b=0,15 =>a=0,15=> mC2H4=3.2(gam)=> mCH4=11,3-3,9-3,2=4,2(gam) =>nCH4=0,2(mol).Tổng thể tích của hỗn hợp=(a+b+c).22,4=11.2(lit)
phần trăm về thể tích của metan trong hỗn hợp đầu=[(0,2.22,4)/11,2].100%=40%
phần trăm về thể tích của etilen trong hỗn hợp đầu=[(0,15.22,4)/11,2].100%=30%
phần trăm về thể tích của axetilen trong hỗn hợp đầu=100%-30%-40%=30%
Đúng 0
Bình luận (0)
a) ptr pứ:
CH4+Br2→CH3Br+HBr
C2H4+Br2→C2H4Br2
C2H2+2Br2→C2H2Br4
C2H2+2AgNO3+2NH3→2NH4NO3+C2Ag2
b) Câu này chắc là phản ứng cộng với Br2 mới ra
nBr2=0,45mol ; nC2Ag2=0,15mol
C2H4 + Br2 ---> C2H4Br2
y ------> y
C2H2 + 2Br2 -----> C2H2Br4
z --------> 2z
==> y +2z = 0,45 (1)
C2H2 + 2AgNO3 + 2NH3 → 2NH4NO3 + C2Ag2
z=0,15 (2) <------------------------------------------ 0,15
btkl: 16x + 28y + 26z=11,3 (3)
giải hệ (1) (2) (3)
x=0,2; y=0,15; z=0,15
=> %VCH4=40%;
%VC2H4=30%
%VC2H2=30%
Đúng 0
Bình luận (0)
a) ptr pứ:
\(CH_4 + Br_2 \rightarrow CH_3Br +HBr\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
\(C_2H_2+2AgNO_3+2NH_3\rightarrow2NH_4NO_3+C_2Ag_2\)
b)
nBr2=0,45mol ; nC2Ag2=0,15mol
CH4 + Br2 -> CH3Br + HBr
x ----> x
C2H4 + Br2 ---> C2H4Br2
y ------> y
C2H2 + 2Br2 -----> C2H2Br4
z --------> 2z
==> x + y +2z = 0,45
Đúng 0
Bình luận (0)
Dẫn 6.72 lít ( ở đktc ) hỗn hợp khí gồm metan và etilen vào bình đựng dung dịch brom dư sau khi phản ứng xảy ra hoàn toàn thấy có 32 gam brom đã tham gia phản ứng a) tính % thể tích các khí trong hỗn hợp ban đầu b) tính khối lượng rượu etylic thu được khí trong lượng etilen trong hỗn hợp trên tác dụng với nước xúc tác axit , nhiệt độ thích hợp . Biết hiệu suất phản ứng đạt 80%
Cho 3,36 lít hỗn hợp khí gồm metan và axetilen qua bình đựng dung dịch nước brom dư, sau phản ứng thấy thoát ra 2,24 lít khí (đktc) a, Viết phương trình phản ứng xảy ra? b, Tính khối lượng brom tham gia phản ứng? c, Xác định thành phần % thể tích hỗn hợp đầu?
Đọc tiếp
Cho 3,36 lít hỗn hợp khí gồm metan và axetilen qua bình đựng dung dịch nước brom dư, sau phản ứng thấy thoát ra 2,24 lít khí (đktc)
a, Viết phương trình phản ứng xảy ra?
b, Tính khối lượng brom tham gia phản ứng?
c, Xác định thành phần % thể tích hỗn hợp đầu?
\(C_2H_2+2Br_2->C_2H_2Br_4\\ n_{hh}=\dfrac{3,36}{22,4}=0,15mol\\ n_{CH_4}=\dfrac{2,24}{22,4}=0,1mol\\ n_{C_2H_2}=0,05mol\\ n_{Br_2}=2.0,05=0,1mol\\ m_{Br_2}=0,1.160=16g\\ \%V_{CH_4}=\dfrac{0,1}{0,15}.100\%=66,67\%\\ \%V_{C_2H_2}=33,33\%\)
Đúng 1
Bình luận (0)
Cho 0,56 lít (đktc) hỗn hợp khí metan và axetilen tác dụng với dung dịch brom dư, lượng brom đã tham gia phản ứng là 5,6 gam. Thành phần phần trăm về thể tích của axetilen trong hỗn hợp ban đầu lần lượt là
A. 20%.
B. 70%.
C . 40%.
D. 60%.