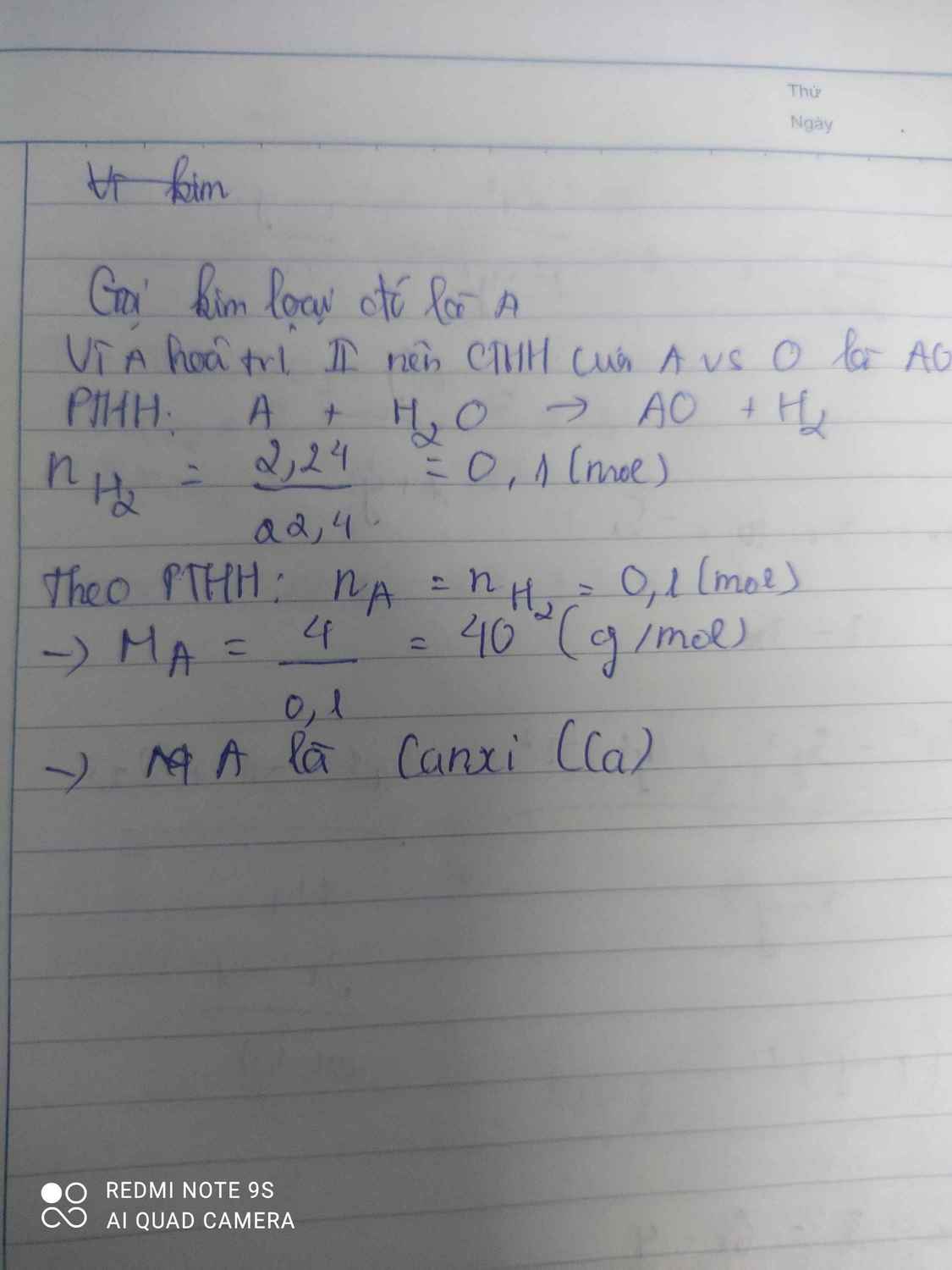Cho 3,22g kim loại hoá trị I tác dụng hết với nước. Sau phản ứng thu được 1,568 lít khí H2 (đktc). Kim loại hoá trị I là

Những câu hỏi liên quan
Bài 15. Cho 18 gam kim loại hoá trị II tác dụng với dung dịch H2SO4 loãng sau phản ứng thu được 16,8 lít khí H2 (đktc). Xác định kim loại hoá trị II?
Gọi Kim loại là A
PT: A + H2SO4 -> ASO4 + H2
nA = nH2 = V/22,4 = 16,8/22,4= 0,75(mol)
=> MA = m/n = 18/0,75 = 24(g/mol)
=> A là Mg (Magie)
Đúng 2
Bình luận (0)
Cho 5,85 gam một kim loại hóa trị I tác dụng hết với nước, sau phản ứng thu được 1,68 lít khí (đktc). Tìm tên kim loại
Gọi kim loại cần tìm là R
PTHH: \(R+H_2O\rightarrow ROH+\dfrac{1}{2}H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\) \(\Rightarrow n_R=0,15\left(mol\right)\)
\(\Rightarrow M_R=\dfrac{5,85}{0,15}=39\left(đvC\right)\) \(\Rightarrow\) R là Kali
Đúng 2
Bình luận (0)
\(n_{H_2}=\dfrac{1.68}{22.4}=0,075\left(mol\right)\)
\(n_X=\dfrac{5,85}{X}\left(mol\right)\)
\(2X+2H_2O\rightarrow2XOH+H_2\uparrow\)
0,15 ←0,075
Ta có:
\(\dfrac{5,85}{X}=0,15\)
\(\Leftrightarrow X=\dfrac{5,85}{0,15}=39\left(K\right)\)
Vậy kim loại đó là K
Đúng 0
Bình luận (0)
Hoà tan 16,8g kim loại hoá trị II vào dung dịch HCl dư, sau phản ứng thu được 6,72 lít khí
H
2
(đktc). Kim loại đem hoà tan là: A. Mg B. Zn C. Pb D. Fe
Đọc tiếp
Hoà tan 16,8g kim loại hoá trị II vào dung dịch HCl dư, sau phản ứng thu được 6,72 lít khí H 2 (đktc). Kim loại đem hoà tan là:
A. Mg
B. Zn
C. Pb
D. Fe
Cho 13.65g một kim loại chưa rõ hoá trị tác dụng với nước thu được một bazơ và 7.84 lít khí h2( đktc). Tìm CTHH của bazơ thu được
Gọi n là hóa trị của kim loại R cần tìm
$2R + 2nH_2O \to 2R(OH)_n + nH_2$
$n_{H_2} = \dfrac{7,84}{22,4} = 0,35(mol)$
Theo PTHH : $n_R = \dfrac{2}{n}.n_{H_2} = \dfrac{0,7}{n}(mol)$
$\Rightarrow \dfrac{0,7}{n}.R = 13,65$
$\Rightarrow R = 19,5n$
(Sai đề)
Đúng 1
Bình luận (0)
Hoà tan hoàn toàn 4g một kim loại hoá trị ll vào nước, sau phản ứng thu được 2.24 lít khí (đktc). Kim loại đó là
đặt kim loại Hóa Trị II là X
pthh: X + 2H2O --> X(OH)2 + H2
số mol của H2:
\(n_{H_2}=\dfrac{V_{H_2}}{22.4}=\dfrac{2.24}{22.4}=0.1mol\)
=> số mol của X là 0.1
KL mol là:
\(M_X=\dfrac{m_x}{n_x}=\dfrac{4}{0.1}=40\) g/mol
=> X là Ca
Đúng 0
Bình luận (2)
cho 2,4g kim loại hóa trị II tác dụng với dung dịch HCl lấy dư, sau khi phản ứng kết thức thu được 2,24 lít khí H2 (ở đktc) xác định tên kim loại?
cho 2,7g kim loại hóa trị III tác dụng với dung dịch H2SO4 lấy dư, sau khi phản ứng kết thúc thu được 3,36 lí khia H2 (ở đktc) xác định tenn kim loại?
Bài 1 :
$R + 2HCl \to RCl_2 + H_2$
n R = n H2 = 2,24/22,4 = 0,1(mol)
M R = 2,4/0,1 = 24(Mg) - Magie
Bài 2 :
$2R + 6HCl \to 2RCl_3 + 3H_2$
n H2 = 3,36/22,4 = 0,15(mol)
n R = 2/3 n H2 = 0,1(mol)
M R = 2,7/0,1 = 27(Al) - Nhôm
Đúng 3
Bình luận (0)
Cho 16,2 gam kim loại M (có hoá trị n không đổi) tác dụng với 3,36 lít O2 (đktc). Hoà tan chất rắn sau phản ứng bằng dung dịch HCl dư thấy thoát ra 13,44 lít H2 (đktc). Kim loại M là A. Mg B. Ca C. Fe D. Al
Đọc tiếp
Cho 16,2 gam kim loại M (có hoá trị n không đổi) tác dụng với 3,36 lít O2 (đktc). Hoà tan chất rắn sau phản ứng bằng dung dịch HCl dư thấy thoát ra 13,44 lít H2 (đktc). Kim loại M là
A. Mg
B. Ca
C. Fe
D. Al
cho 11,2g sắt tác dụng với 43,8g axit clohidric sau phản ứng thu được dung dịch muối và V lít khí hidro đktc. Tính giá trị V b, để khử hoàn toàn 36g oxit một kim loại hoá trị 2 cần đung 11,2 lít khi h2 đktc. Tìm CTHH của oxit trên cho: Fe=5,6 O=16 H=1 Cl=35,5 Mọi người giúp em vs ạ
Câu 1:
PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
Ta có: \(\left\{{}\begin{matrix}n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\\n_{HCl}=\dfrac{43,8}{36,5}=1,2\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,2}{1}< \dfrac{1,2}{2}\) \(\Rightarrow\) HCl còn dư, Fe p/ứ hết
\(\Rightarrow n_{H_2}=0,2\left(mol\right)\) \(\Rightarrow V_{H_2}=0,2\cdot22,4=4,48\left(l\right)\)
Đúng 2
Bình luận (0)
Câu 2:
PTHH: \(RO+H_2\underrightarrow{t^o}R+H_2O\)
Ta có: \(n_{RO}=n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(\Rightarrow\dfrac{36}{M_R+16}=0,5\) \(\Rightarrow M_R=56\) (Sắt)
Vậy CTHH cần tìm là FeO
Đúng 1
Bình luận (0)
Giúp mình với mình đang cần gấp đề cương hoá cuối kì || Cho 3 gam 1 kim loại ( chưa rõ hoá trị ) tác dụng với nước dư, thu được 1,68 lít khí hiđro ( do ở đktc ). Hãy xác định tên kim loại, biết rằng kim loại có giá trị tối đa là |||
Gọi kim loại cần tìm là `A` và có hóa trị là `x`
`2A + 2xH_2 O -> 2A(OH)_x + x H_2↑`
`[0,15] / x` `0,075` `(mol)`
`n_[H_2] = [ 1,68 ] / [ 22,4 ] = 0,075 (mol)`
`=>M_A = 3 / [ [ 0,15 ] / x ] = [ 3x ] / [ 0,15]`
`@ x = 1 => M_A = 20 ( g // mol ) ->` Loại
`@ x = 2 => M_A = 40 ( g // mol )->` Nhận và `A` là `Ca`
`@ x = 3 => M_A = 60 ( g // mol )->` Loại
Vậy tên kim loại cần tìm là `Ca`
Đúng 1
Bình luận (0)
Gọi R là kim loại cần tìm
.......x là hóa trị của R
=> nH2 =\(\dfrac{1,68}{22,4}\)0,15\x<---------------------------0,075
Ta có: ⇒MR=\(\dfrac{3x}{0,15}=20x\)=20x
Biện luận:
| x | 1 | 2 |
| MR | 20 (loại) | 40 (nhận) |
Đúng 0
Bình luận (0)