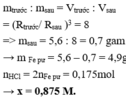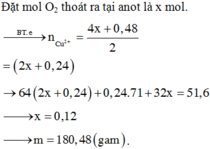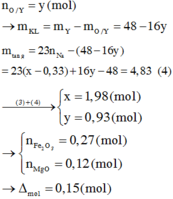Thả viên bi sắt (hình cầu) nặng 5,6 gam vào dung dịch HCl. Sau khi đường kính viên bị chỉ còn lại ½ thì thấy khí ngừng thoát ra. Tính khối lượng axit đã phản ứng

Những câu hỏi liên quan
Thả một viên bi sắt hình cầu nặng 5,6 gam vào 200 ml dung dịch HCl chưa biết nồng độ. Sau khi đường kính viên bi còn lại bằng 1/2 so với ban đầu thu khí ngừng thoát ra ( giả sử viên bi bị mòn đều từ mọi phía). Nồng độ (mol/l) của dung dịch HCl là? A . 0,5M B. 1,376 M C . 0,125 M D. 0,875 M
Đọc tiếp
Thả một viên bi sắt hình cầu nặng 5,6 gam vào 200 ml dung dịch HCl chưa biết nồng độ. Sau khi đường kính viên bi còn lại bằng 1/2 so với ban đầu thu khí ngừng thoát ra ( giả sử viên bi bị mòn đều từ mọi phía). Nồng độ (mol/l) của dung dịch HCl là?
A . 0,5M
B. 1,376 M
C . 0,125 M
D. 0,875 M
m = d∗V = d∗4πR^3 : 3
Sau khi phản xảy ra thu đương kinh viên con lại bằng
m1 = d∗V1 = d ∗ 4πR1^3 : 3
m2 = d∗V2 = d ∗ 4πR2^3 : 3
→ m1 = 8m2→ m2 = 0.7g
Khối lượng Fe phản ứng là: 5.6 - 0.7 = 4.9g
Số mol Fe tham gia pư là: 4.9/56 = 0.0875 mol
→ CM HCl = 0.0875∗20.2 = 0.875M
=> Đáp án D
Đúng 0
Bình luận (0)
Thả một viên bi sắt nguyên chất hình cầu nặng 5,6 gam vào 200 ml dung dịch HCl nồng độ x mol/l. Khi khí ngừng thoát ra thì đường kính viên bi còn lại bằng ½ đường kính ban đầu (giả sử viên bi bị ăn mòn đều về mọi phía). Giá trị của x là
A. 1,000
B. 0,125
C. 0,500
D. 0,875
Thả một viên bi hình cầu bán kính là r0 làm bằng kim loại Al nặng 5,4 gam vào 1,75 lít dung dịch HCl 0,3M. khi khí ngừng thoát ra (phản ứng hoàn toàn) thì bán kính viên bi là r1 (giả sử viên bi bị mòn đều từ các phía) nhận xét đúng là: A. r0 0,25 r1 B. r0 r1 C. r0 2 r1 D. r1 2 r0
Đọc tiếp
Thả một viên bi hình cầu bán kính là r0 làm bằng kim loại Al nặng 5,4 gam vào 1,75 lít dung dịch HCl 0,3M. khi khí ngừng thoát ra (phản ứng hoàn toàn) thì bán kính viên bi là r1 (giả sử viên bi bị mòn đều từ các phía) nhận xét đúng là:
A. r0 =0,25 r1
B. r0 = r1
C. r0 =2 r1
D. r1 =2 r0
Điện phân dung dịch gồm 28,08 gam NaCl và m gam Cu(NO3)2 với điện cực trơ, màng ngăn xốp đến khi khối lượng dung dịch giảm 51,60 gam thì ngừng điện phân thu được dung dịch X. nhúng thanh sắt dư vào X, sau khi các phản ứng kết thúc thấy khối lượng thanh sắt giảm 6,24 gam, thấy thoát ra khí NO duy nhất. Giá trị của m gần nhất với giá trị nào sau đây ? A. 160 B. 180 C. 170 D. 190
Đọc tiếp
Điện phân dung dịch gồm 28,08 gam NaCl và m gam Cu(NO3)2 với điện cực trơ, màng ngăn xốp đến khi khối lượng dung dịch giảm 51,60 gam thì ngừng điện phân thu được dung dịch X. nhúng thanh sắt dư vào X, sau khi các phản ứng kết thúc thấy khối lượng thanh sắt giảm 6,24 gam, thấy thoát ra khí NO duy nhất. Giá trị của m gần nhất với giá trị nào sau đây ?
A. 160
B. 180
C. 170
D. 190
Cho 5,6 gam Fe tác dụng với dd axit clohidric 15% , sau phản ứng thu được dd sắt (II) clorua và khí hidro a viết phương trình phản ứng b. tính thể tích hidro thoát ra (ở đktc) c. tính khối lượng dung dịch hcl tham gia phản ứng
Fe + 2HCl -> FeCl2 + H2
nFe = 5,6/56 = 0,1 mol
=>nH2 = 0,1 mol
=> VH2= 0,1*22,4= 2,24 lít
Đúng 1
Bình luận (0)
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PTHH: Fe + 2HCl ---> FeCl2 + H2
0,1-->0,2------------------>0,1
=> \(\left\{{}\begin{matrix}m_{ddHCl}=\dfrac{0,2.36,5}{15\%}=\dfrac{146}{3}\left(g\right)\\V_{H_2}=0,1.22,4=4,48\left(l\right)\end{matrix}\right.\)
Đúng 0
Bình luận (2)
Hòa tan 5,6 (g) sắt (Fe) vào dung dịch chứa 7,3 gam axit clohiđric (HCl) thu được 12,7 (g) muối sắt (II) clorua (FeCl2 ) và khí hiđro. Hãy tính khối lượng của khí hiđro tạo ra sau phản ứng.
BTKL: \(m_{Fe}+m_{HCl}=m_{muối}+m_{H_2}\)
\(\Rightarrow m_{H_2}=5,6+7,3-12,7=0,2\left(g\right)\)
Đúng 1
Bình luận (0)
Một viên bi sắt có đường kính 2cm ngập trong một cốc chứa 100ml axit có pH 0, phản ứng xảy ra hoàn toàn. Bán kính viên bi sắt sau phản ứng (coi rằng viên bi bị mòn đều từ mọi phía, khối lượng riêng của sắt là 7,8 g/
cm
3
)là A. 0,56cm B. 0,84cm C.0,78cm D.0,97cm
Đọc tiếp
Một viên bi sắt có đường kính 2cm ngập trong một cốc chứa 100ml axit có pH = 0, phản ứng xảy ra hoàn toàn. Bán kính viên bi sắt sau phản ứng (coi rằng viên bi bị mòn đều từ mọi phía, khối lượng riêng của sắt là 7,8 g/ cm 3 )là
A. 0,56cm
B. 0,84cm
C.0,78cm
D.0,97cm
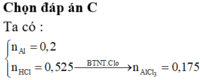
Cho hơi nước đi qua than nóng đỏ chỉ thu được hỗn hợp khí X. Dẫn X qua bình đựng 48 gam hỗn hợp rắn Y chứa Fe2O3; MgO đến phản ứng hoàn toàn (chất rắn còn lại trong bình vẫn chứa oxit sắt). Hấp thụ hết lượng khí và hơi thoát ra vào bình đựng dung dịch nước vôi trong dư thu được 24 gam kết tủa. Hòa tan phần rắn còn lại bằng dung dịch chứa 0,33 mol KNO3 và x mol HCl thì khối lượng dung dịch tăng thêm 27,78 gam (không còn axit dư) và thoát ra 0,37 mol hỗn hợp khí T chứa NO; NO2; H2. Thêm một lượng...
Đọc tiếp
Cho hơi nước đi qua than nóng đỏ chỉ thu được hỗn hợp khí X. Dẫn X qua bình đựng 48 gam hỗn hợp rắn Y chứa Fe2O3; MgO đến phản ứng hoàn toàn (chất rắn còn lại trong bình vẫn chứa oxit sắt). Hấp thụ hết lượng khí và hơi thoát ra vào bình đựng dung dịch nước vôi trong dư thu được 24 gam kết tủa. Hòa tan phần rắn còn lại bằng dung dịch chứa 0,33 mol KNO3 và x mol HCl thì khối lượng dung dịch tăng thêm 27,78 gam (không còn axit dư) và thoát ra 0,37 mol hỗn hợp khí T chứa NO; NO2; H2. Thêm một lượng NaOH vừa đủ vào dung dịch tạo thành thấy khối lượng chất tan tiếp tục tăng 4,83 gam. Hiệu số mol hai chất trong Y là
A. 0,05 mol
B. 0,10 mol
C. 0,15 mol
D. 0,20 mol
Bài1: 9,5 gam hỗn hợp CaO và K vào nước dư.Sau phản ứng thấy có 1,12 lít khí (đktc) thoát ra. Tính % khối lượng mỗi chất trong hỗn hợpBài 2 : Cho 3,6 gam một oxit sắt vào dung dịch HCl dư.Sau phản ứng xảy ra hoàn hoàn thu được 6,35 gam một muối sắt clorua. Xác định công thức của sắtBài 3: Cho 10,4 gam oxit của một nguyên tố kim loại hoá trị 2 tác dụng với dung dịch HCl dư,sau p/ư tạo thành 15,9 gam muối.Xác định nguyên tố kim loạiBài 4 : Cho một dòng khí H2 dư qua 4,8 gam hỗn hợp CuO và một oxi...
Đọc tiếp
Bài1: 9,5 gam hỗn hợp CaO và K vào nước dư.Sau phản ứng thấy có 1,12 lít khí (đktc) thoát ra. Tính % khối lượng mỗi chất trong hỗn hợp
Bài 2 : Cho 3,6 gam một oxit sắt vào dung dịch HCl dư.Sau phản ứng xảy ra hoàn hoàn thu được 6,35 gam một muối sắt clorua. Xác định công thức của sắt
Bài 3: Cho 10,4 gam oxit của một nguyên tố kim loại hoá trị 2 tác dụng với dung dịch HCl dư,sau p/ư tạo thành 15,9 gam muối.Xác định nguyên tố kim loại
Bài 4 : Cho một dòng khí H2 dư qua 4,8 gam hỗn hợp CuO và một oxit sắt nung nóng thu được 3,52 gam chất rắn.Nếu cho chất rắn đó hoà tan trong axit HCl thì thu được 0,896 lít H2 (đktc).Xác định khối lượng mỗi oxit trong hỗn hợp và xác đijnh công thức của oxit sắt.
Bài 5:
Thả 2,3 gam Na vào 200 gam dung dịch NaOH 5% thấy thoát ra khí.
a) Tính nồng độ % dung dịch sau p/ư
b) Tính nồng độ mol dung dịch sau p/ư biết thể tích là 200ml
Bài 6:
Thả 4 gam Ca vào 200 gam dung dịch NaOH 5% thấy thoát ra khí.
a) Tính nồng độ % dung dịch sau p/ư
b) Cho V=1 lít.Tính nồng độ mol mỗi chất sau p/ư
1 ) CAO +H2O => CA(OH)2 (1)
2K + 2H2O => 2KOH + H2(2)
n (H2) =1,12/22,4 =0,05
theo ptpư 2 : n(K) = 2n (h2) =2.0.05=0,1(mol)
=> m (K) =39.0,1=3,9 (g)
% K= 3,9/9,5 .100% =41,05%
%ca =100%-41,05%=58,95%
Đúng 0
Bình luận (0)
xo + 2hcl =>xcl2 +h2o
10,4/X+16 15,9/x+71
=> giải ra tìm đc X bằng bao nhiêu thì ra
Đúng 0
Bình luận (0)
gọi CTHH của oxit sắt là FexOy
PTHH:FexOy +2yHCl => xFeCl2y/x +yH2O
10,4/56x + 16y 6,35/56x +71 y
=> giải ra x,y
bài nay Hân k chắc lém
Đúng 0
Bình luận (0)