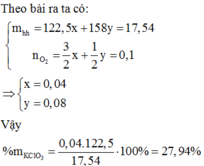mn ơi cho em hỏi là khi nhiệt phân cùng 1 lượng KCLO3 và KMnO4 thì chất nào thu được nhiều khí O2 hơn và vì sao ạ? 😢

Những câu hỏi liên quan
nhiệt phân hoàn toàn kclo3 và kmno4 và thu được lượng oxi như nhau. hỏi lượng chất nào dùng nhiều hơn? vì sao?
KClO3 --> KCl + O2
2KMnO4 --> MnO2 + O2 + K2MnO4
Để tạo 1 mol O2 cần 1 mol KClO3 nhưng cần 2 mol KMnO4
Vậy khi thu được lượng oxi như nhau thì cần dùng lượng KMnO4 nhiều hơn
Đúng 2
Bình luận (2)
Gọi n là số mol của 2 phản ứng
PTHH:
\(2KClO_3\xrightarrow[t^o]{MnO_2}2KCl+3O_2\left(1\right)\)
\(2KMnO_4\overset{t^o}{--->}K_2MnO_4+MnO_2+O_2\left(2\right)\)
Theo PT(1): \(n_{KClO_3}=\dfrac{2}{3}n\left(mol\right)\)
\(\Rightarrow m_{KClO_3}=122,5.\dfrac{2}{3}n=\dfrac{245}{3}n\left(g\right)\)
Theo PT(2): \(n_{KMnO_4}=2n\left(mol\right)\)
\(\Rightarrow m_{KMnO_4}=158.2n=316n\left(g\right)\)
Ta thấy: \(\dfrac{245}{3}n< 316n\)
Vậy KMnO4 dùng nhiều hơn
Đúng 1
Bình luận (1)
Đề bài không cho cùng KL hay cùng số mol à?
Đúng 0
Bình luận (0)
Nung a gam KClO3 và b gam KMnO4 thu được cùng một lượng O2. Tính tỉ lệ a/b
Câu 8. Lấy cùng một lượng KClO3 và KMnO4 để điều chế khí O2. Chất nào cho nhiều khí O2 hơn.
Để điều chế khí oxi người ta phân hủy KMnO4 và KCLO3 a/Để thu được lượng khí oxi như nhau,chất nào cần số mol nhiều hơn?Cần dùng khối lượng nhiều hơn? b/phân hủy cùng số mol,chất nào sinh ra khí nhiều hơn? c/phân hủy cùng khối lượng chất nào sinh ra khí oxi nhiều hơn? d/Biết giá thành 1kg KMnO4 là 200000đ,1kg KCLO3 là 300000đ,hãy cho biết để điều chế khí oxi như nhau,thì dùng chất nào có giá thành rẻ nhiều hơn?
Đọc tiếp
Để điều chế khí oxi người ta phân hủy KMnO4 và KCLO3
a/Để thu được lượng khí oxi như nhau,chất nào cần số mol nhiều hơn?Cần dùng khối lượng nhiều hơn?
b/phân hủy cùng số mol,chất nào sinh ra khí nhiều hơn?
c/phân hủy cùng khối lượng chất nào sinh ra khí oxi nhiều hơn?
d/Biết giá thành 1kg KMnO4 là 200000đ,1kg KCLO3 là 300000đ,hãy cho biết để điều chế khí oxi như nhau,thì dùng chất nào có giá thành rẻ nhiều hơn?
a)6KMnO4--->3K2MnO4 + 3MnO2 + 3O2 (1)
2KClO3---> 2KCl + 3O2 (2)
Dựa vào phương trình trên ---> thu cùng lượng O2, KMnO4 cần nhiều số mol hơn, và khối lượng nhiều hơn.
b)6KClO3-->6KCl + 9O2 (3)
1,3--->Cùng số mol, KClO3 cho nhiều O2 hơn.
c)Giả sử cả 2 chất cùng có khối lượng là 100g
nKMnO4=50/79(mol)
nKClO3=40/49
Thay vào các phương trình phản ứng tính ra mO2
Cụ thể: KMnO4 cho ra 800/79 (g) O2
KClO3 cho ra 1920/49 (g) O2
---> Cùng m thì KClO3 cho nhiều g O2 hơn.
d) Giả sử cần điều chế 32 g O2
--->nO2=1 mol
--->nKMnO4=2 mol--->mKMnO4=316g
và nKClO3=2/3 mol--->nKClO3=245/3g
Ta có:
-1000g KMnO4 <=> 200000đ
316 g=========>63200đ
-1000g KClO3 <=> 300000đ
245/3g========> 24500đ
Vậy để điều chế cùng lượng O2, KClO3 có giá thành rẻ hơn.
Đúng 0
Bình luận (0)
Lấy cùng một lượng
K
C
l
O
3
và
K
M
n
O
4
để điều chế oxi. Chất nào tạo ra nhiều khí
O
2
hơn. Nếu điều chế dùng một thể tích khí oxi thì dùng chất nào kinh tế hơn? Biết rằng giá
K
M
n
O
4
là 30.000 đ/kg và
K
C
l...
Đọc tiếp
Lấy cùng một lượng K C l O 3 và K M n O 4 để điều chế oxi. Chất nào tạo ra nhiều khí O 2 hơn. Nếu điều chế dùng một thể tích khí oxi thì dùng chất nào kinh tế hơn? Biết rằng giá K M n O 4 là 30.000 đ/kg và K C l O 3 là 96.000 đ/kg.
Giả sử cần điều chế 3,36lit O 2 tương đương với 0,15 mol O 2
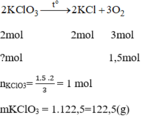
Số tiền mua 122,5g để điều chế 1,5mol O 2 :
0,1225.96000 = 11760 (đồng)
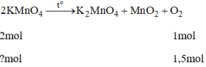
n K M n O 4 = 1,5 . 2 =3 mol
n K M n O 4 = 3.158 = 474 (g)
Số tiền mua 474g để điều chế 1,5 mol O 2 :
0,474.30000 = 14220(đồng)
Vậy để điều chế cùng 1 thể tích khí O 2 thì dùng K C l O 3 để điều chế kinh tế hơn mặc dù giá tiền cao mua 1 kg K C l O 3 cao hơn nhưng thể tích khí O 2 sinh ra nhiều hơn.
Đúng 0
Bình luận (0)
trong phòng thí nghiệm người ta điều chế oxi bằng cách nhiệt phân kmno4 hoặc kclo3.hỏi sử dụng khối lượng kmno4 và kclo3 bằng nhau thì cái nào thu khí oxi nhiều hơn
Hm....
KClO3 thu đc nhiều hơn
Nung KClO3 và KMnO4 thu được một lượng khí O2 ở(đktc).Hỏi cần khối lượng chất nào ít hơn
Giả sử: nO2 = x (mol)
PT: \(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
___2/3.x_____________x (mol) ⇒ \(m_{KClO_3}=\dfrac{2}{3}x.122,5=\dfrac{245}{3}x\left(g\right)\)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
2x_________________________x (mol) ⇒ \(m_{KMnO_4}=2x.158=316x\left(g\right)\)
Có: \(\dfrac{245}{3}x< 316x\Rightarrow m_{KClO_3}< m_{KMnO_4}\)
Vậy: Khối lượng KClO3 cần dùng ít hơn.
Bạn tham khảo nhé!
Đúng 1
Bình luận (0)
Cần khối lượng chất nào ít hơn để thu thể tích O2 nhiều hơn à?
Đúng 0
Bình luận (0)
Nhiệt phân 17,54 gam hỗn hợp X gồm KClO3 và KMnO4, thu được O2 và m gam chất rắn gồm K2MnO4, MnO2 và KCl. Toàn bộ lượng O2 tác dụng hết với cacbon nóng đỏ, thu được 3,584 lít hỗn hợp khí Y (đktc) có tỉ khối so với O2 là 1. Thành phần % theo khối lượng của KClO3 trong X là: A. 62,76% B. 74,92% C. 72,06% D. 27,94%
Đọc tiếp
Nhiệt phân 17,54 gam hỗn hợp X gồm KClO3 và KMnO4, thu được O2 và m gam chất rắn gồm K2MnO4, MnO2 và KCl. Toàn bộ lượng O2 tác dụng hết với cacbon nóng đỏ, thu được 3,584 lít hỗn hợp khí Y (đktc) có tỉ khối so với O2 là 1. Thành phần % theo khối lượng của KClO3 trong X là:
A. 62,76%
B. 74,92%
C. 72,06%
D. 27,94%
1. Nhiệt phân hoang toàn 12,25g KClO3. Tính thể khí O2 ở đktc thu được 2. Muốn điều chế được 48g O2 thì khối lượng KClO3 cần nhiệt phân là bao nhieu g 3. Muốn điều chế được 2,8 lít O2 ở đktc thì khối lượng KMnO4 cần nhiệt phân là bao nhiêu
Xem chi tiết
PTHH : \(2KClO_3\rightarrow t^0\rightarrow2KCl+3O_2\uparrow\)
Số mol KClO3 tham gia phản ứng : \(n_{KClO_3}=\frac{m_{KClO_3}}{M_{KClO_3}}=\frac{12,25}{122,5}=0,1\left(mol\right)\)
1. Theo PTHH : Cứ 2 mol KClO3 tham gia phản ứng thì tạo thành 3 mol O2
=> Cứ 0,1 mol KClO3 tham gia phản ứng thì tạo thành 0,15 mol O2
=> Thể tích khí O2 thu được ở đktc là : \(V_{O_2}=n_{O_2}\times22,4=0,15\times22,4=3,36\left(l\right)\)
2. Số mol O2 tạo thành sau phản ứng : \(n_{O_2}=\frac{m_{O_2}}{M_{O_2}}=\frac{48}{32}=1,5\left(mol\right)\)
Theo PTHH : Cứ 3 mol O2 tạo thành sau phản ứng thì có 2 mol KClO3 tham gia phản ứng
=> Cứ 1,5 mol O2 tạo thành sau phản ứng thì có 1 mol KClO3 tham gia phản ứng
=> Khối lượng KClO3 cần nhiệt phân : \(m_{KClO_3}=n_{KClO_3}\times M_{KClO_3}=1\cdot126,9=126,9\left(g\right)\)
3. Số mol O2 thu được sau phản ứng ở đktc : \(n_{O_2}=\frac{V_{O_2}}{22,4}=\frac{2,8}{22,4}=0,125\left(mol\right)\)
Theo PTHH : Cứ 3 mol O2 tạo thành sau phản ứng thì có 2 mol KClO3 tham gia phản ứng
=> Cứ 0.125 mol O2 tạo thành sau phản ứng thì có 1/12 mol KClO3 tham gia phản ứng
=> Khối lượng KClO3 cần nhiệt phân : \(m_{KClO_3}=n_{KClO_3}\times M_{KClO_3}=\frac{1}{12}\cdot126,9=10.575\left(g\right)\)
Quỳnh•Sinestrea⁰⁷ : đừng làm hóa nữa, làm toàn nhầm thôi đấy
1. PTHH : \(2KClO_3-t^o->2KCl+3O_2\)
. \(n_{KClO_3}=\frac{12,25}{122,5}=0,1\left(mol\right)\)
Theo pthh : \(n_{O_2}=\frac{3}{2}n_{KClO_3}=0,15\left(mol\right)\)
=> \(V_{O_2}=0,15\cdot22,4=3,36\left(l\right)\)
2. PTHH : \(2KClO_3-t^o->2KCl+3O_2\)
\(n_{O_2}=\frac{48}{32}=1,5\left(mol\right)\)
Theo pthh : \(n_{KClO_3}=\frac{2}{3}n_{O_2}=1\left(mol\right)\)
=> \(m_{KClO_3}=1\cdot122,5=122,5\left(g\right)\)
3. PTHH : \(2KMnO_4-t^o->K_2MnO_4+MnO_2+2O_2\)
\(n_{O_2}=\frac{2,8}{22,4}=0,125\left(mol\right)\)
Theo pthh : \(n_{KMnO_4}=n_{O_2}=0,125\left(mol\right)\)
=> \(m_{KMnO_4}=0,125\cdot158=19,75\left(g\right)\)
Lấy cùng một lượng K C l O 3 và K M n O 4 để điều chế oxi. Chất nào tạo ra nhiều khí O 2 hơn. Viết phương trình phản ứng và giải thích.
Giả sử ta lấy cùng một khối lượng là a g
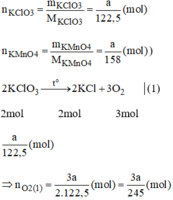
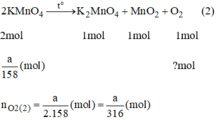
Vậy 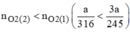 nên khi nhiệt phân cùng 1 lượng chất cho nhiều oxi hơn là
K
C
l
O
3
nên khi nhiệt phân cùng 1 lượng chất cho nhiều oxi hơn là
K
C
l
O
3
Đúng 0
Bình luận (0)