Cho 10g hh gồm CH4 , C2H4 tác dụng với 100ml dd Brom 2M Tính thành phần % theo khối lượng của các khí trong hh

Những câu hỏi liên quan
Cho hh X gồm CH4, C2H4 và C2H2. Lấy 8,6 gam X t/d hết với dd brom (dư) thì khối lượng brom pư là 48 gam. Mặt khác, nếu cho 13,44 lít (ở đktc) hh khí X t/d với lượng dư dd AgNO3 trong NH3, thu được 36 gam kết tủa. Phần trăm thể tích của CH4 có trong X là A. 20% B. 50% C. 25% D. 40%
Đọc tiếp
Cho hh X gồm CH4, C2H4 và C2H2. Lấy 8,6 gam X t/d hết với dd brom (dư) thì khối lượng brom pư là 48 gam. Mặt khác, nếu cho 13,44 lít (ở đktc) hh khí X t/d với lượng dư dd AgNO3 trong NH3, thu được 36 gam kết tủa. Phần trăm thể tích của CH4 có trong X là
A. 20%
B. 50%
C. 25%
D. 40%
Đáp án B
Gọi x, y, z 1à số mol của CH4, C2H4 và C2H2 trong 8,6g hh X
=> 16x + 28y + 26z = 8,6 (1)
- Khi cho X td với dung dịch Br2 dư:
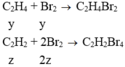
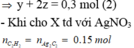

Đúng 0
Bình luận (0)
Cho 5,6 lít hh etilen và metan tác dụng với 200g dd brom 20% thủ được dd A a. Tính khối lượng chất tan có trong A b. Tính khối lượng dd brom cần dùng c. Tính thành phần phần trăm từng khí trong hh bạn đầu. Giúp mình với
Xem chi tiết
\(n_{hh}=\dfrac{5.6}{22.4}=0.25\left(mol\right)\)
\(m_{Br_2}=200\cdot\dfrac{20}{100}=40\left(g\right)\)
\(n_{Br_2}=\dfrac{40}{160}=0.25\left(mol\right)\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(0.25........0.25..........0.25\)
\(\)\(n_{C_2H_4}=n_{hh}=0.25\left(mol\right)\)
=> Sai đề
Đúng 2
Bình luận (0)
Giúp em câu này với ạ. Em cần hơi gấp. Em cảm ơn nhiều. Dẫn 56 lít khí hh gồm C2H4 và C2H2(đktc) tác dụng với 480 gam dd Brom dư.Tính thành phần phần trăm theo thể tích của mỗi chất có trong hh trên.
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
Ta có: \(n_{C_2H_4}+n_{C_2H_2}=\dfrac{56}{22,4}=2,5\left(mol\right)\left(1\right)\)
Theo PT: \(n_{Br_2}=n_{C_2H_4}+2n_{C_2H_2}=\dfrac{480}{160}=3\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{C_2H_4}=2\left(mol\right)\\n_{C_2H_2}=0,5\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{2.22,4}{56}.100\%=80\%\\\%V_{C_2H_2}=100-80=20\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
cho 10g hh Cu và CuO tác dụng vừa đủ với đd H2SO4 loãng lọc lấy chất rắn không tan ,cho vào dd H2SO4 đặc nóng thì thu được 1,12 lít khí A (đktc)
a, viết PTHH và cho biết tên của khí A
b, tính thành phần % khối lượng các chất có trong hh
A là hh khí gồm CH4 , C2H4 và H2. Cho 3360 ml A sục qua dd brom thấy dd bị nhạt màu và khối lượng tăng thêm 0,84 g.a. Xác định % thể tích mỗi khí trong A. Biết rằng 0,7 lit hh khí này có khối lượng 0,4875g.b. Đốt cháy hoàn toàn 1,68 lít A rồi dẫn sản phẩm vào 1 lít dd Ca(OH) 2 0,05M ( D 1,025). Tính nồng độ % của chất sau phản ứng. Các thể tích khí đo ở đktc.
Đọc tiếp
A là hh khí gồm CH4 , C2H4 và H2. Cho 3360 ml A sục qua dd brom thấy dd bị nhạt màu và khối lượng tăng thêm 0,84 g.
a. Xác định % thể tích mỗi khí trong A. Biết rằng 0,7 lit hh khí này có khối lượng 0,4875g.
b. Đốt cháy hoàn toàn 1,68 lít A rồi dẫn sản phẩm vào 1 lít dd Ca(OH) 2 0,05M ( D= 1,025). Tính nồng độ % của chất sau phản ứng. Các thể tích khí đo ở đktc.
a) \(m_{tăng}=m_{C_2H_4}=0,84\left(g\right)\)
=> \(n_{C_2H_4}=\dfrac{0,84}{28}=0,03\left(mol\right)\)
Gọi số mol CH4, H2 trong 3360 ml A là a, b
=> \(a+b=\dfrac{3,36}{22,4}-0,03=0,12\left(mol\right)\) (1)
Gọi số mol CH4, H2 trong 0,7 lít hh là ak, bk
=> ak + bk + 0,03k = \(\dfrac{0,7}{22,4}=0,03125\) (2)
Và 16ak + 2bk + 0,84k = 0,4875 (3)
(1)(2)(3) => \(\left\{{}\begin{matrix}a=0,09\left(mol\right)\\b=0,03\left(mol\right)\\k=\dfrac{5}{24}\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,03}{0,15}.100\%=20\%\\\%V_{CH_4}=\dfrac{0,09}{0,15}.100\%=60\%\\\%V_{H_2}=\dfrac{0,03}{0,15}.100\%=20\%\end{matrix}\right.\)
b)
\(n_{C_2H_4}=\dfrac{1,68}{22,4}.20\%=0,015\left(mol\right)\)
\(n_{CH_4}=\dfrac{1,68}{22,4}.60\%=0,045\left(mol\right)\)
\(n_{H_2}=\dfrac{1,68}{22,4}.20\%=0,015\left(mol\right)\)
Bảo toàn C: \(n_{CO_2}=0,075\left(mol\right)\)
Bảo toàn H: \(n_{H_2O}=0,135\left(mol\right)\)
\(n_{Ca\left(OH\right)_2}=0,05.1=0,05\left(mol\right)\)
\(m_{ddCa\left(OH\right)_2}=1000.1,025=1025\left(g\right)\)
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
0,05---->0,05----->0,05
CaCO3 + CO2 + H2O --> Ca(HCO3)2
0,025<--0,025------------>0,025
\(m_{CaCO_3}=\left(0,05-0,025\right).100=2,5\left(g\right)\)
mdd sau pư = 1025 + 0,075.44 + 0,135.18 - 2,5 = 1028,23 (g)
\(C\%_{Ca\left(HCO_3\right)_2}=\dfrac{0,025.162}{1028,23}.100\%=0,3939\%\)
Đúng 3
Bình luận (0)
Đốt V lít hh khí ch4, c2h4. Cho toàn bộ sp hấp thụ hết vào 100ml dd naoh 2M thu đc dd A. Thêm A vào lượng dư bacl2 thu 11,82g kết tủa
viết pthh
tính % theo thể tích mỗi chất trong hh ban đầu. Bjết rằng nếu cho V lit đkc hh đó qua lượng dư dd brom có 3,2g brom phản ứng
hh x gồm 5,25g Cu và Zn tác dụng với dd H2SO4 loãng có 1,12 lít khí thoát ra . Tính thành phần % khối lượng kim loại trong hh ban đầu
$Zn + H_2SO_4 \to ZnSO_4 + H_2$
$n_{Zn} = n_{H_2} = \dfrac{1,12}{22,4} = 0,05(mol)$
$\%m_{Zn} = \dfrac{0,05.65}{5,25}.100\% = 61,9\%$
$\%m_{Cu} =1 00\% -61,9\% = 38,1\%$
Đúng 1
Bình luận (0)
Pthh:
\(Zn+H2SO4->ZnSO\text{4+H2}\)
\(nZn=nH2=\dfrac{1,12}{22,4}=0,05mol\)
\(=>mZn=0,05.65=3,25g\)\(=>\%mZn=\dfrac{3,25}{5,25}.100\%=62\%\)
\(=>\%mCu=100-62=38\%\)
Đúng 0
Bình luận (0)
Có một hh A gam gồm rượu etylic và axit axetic người ta đa thực hiện thí nghiệm sau:
Cho A tác dụng với Na dư thu được 6.72 lít khí đktc
Cho A tác dụng với 100ml đ NaOH 2M thì vừa hết
a) tính % theo khối lượng của mỗi chất có trong A
b) đun nóng hh trên thu được bao nhiêu gam este có axit xúc tác H=82%
n H2 =0,3 mol
n NaOH =0,2 mol
=>n OH= n H+ =0,2 mol
=>n CH3COOH=0,2 mol
=>m CH3COOH=0,2.60=12g
->n C2H5OH=0,1 mol
=>m C2H5OH=4,6g
=>mC2H5OH=\(\dfrac{4,6}{4,6+12}100=27,71\%\)
=>maxit=72,29%
b)
CH3COOH+C2H5OH->CH3COOC2H5+H2O
0,1-------------0,1
=>H=82%
=>m CH3COOC2H5=0,082.88=7,216g
Đúng 2
Bình luận (2)



















