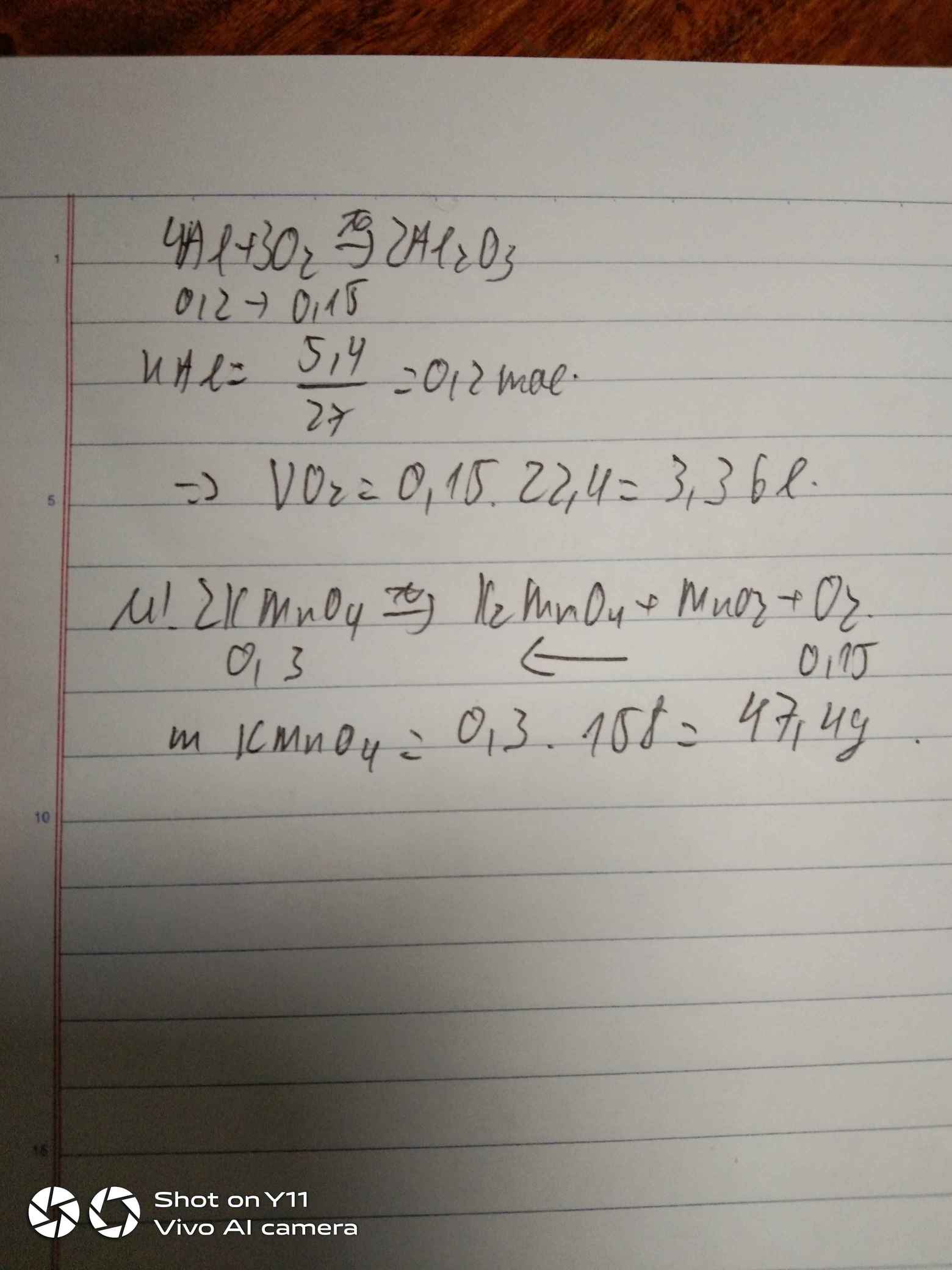Đốt cháy hoàn toàn 5,4 g kim loại nhôm Al trong khí oxi. a. Tính thể tích khí oxi (đktc) cần dùng cho phản ứng. b. Tính khối lượng KClO3 cần dùng để điều chế lượng oxi trên.

Những câu hỏi liên quan
Đốt cháy hoàn toàn m gam nhôm trong oxi dư người ta thu được 30,6 gam nhôm oxit (Al2O3)a) Tìm khối lượng nhôm phản ứng, thể tích oxi, thể tích không khí cần dùng b)Tính khối lượng Kaliclorat (KClO3 )cần dùng để điều chế được lượng oxi dùng cho phản ứng trên? (Hiệu suất phản ứng nung là H100%) c)Tính khối lượng Kaliclorat cần dùng để điều chế được lượng oxi dùng cho phản ứng trên? (Hiệu suất phản ứng nung là H75%) (K39, Cl35,5, Al27, O16)
Đọc tiếp
Đốt cháy hoàn toàn m gam nhôm trong oxi dư người ta thu được 30,6 gam nhôm oxit (Al2O3)
a) Tìm khối lượng nhôm phản ứng, thể tích oxi, thể tích không khí cần dùng
b)Tính khối lượng Kaliclorat (KClO3 )cần dùng để điều chế được lượng oxi dùng cho phản ứng trên? (Hiệu suất phản ứng nung là H=100%)
c)Tính khối lượng Kaliclorat cần dùng để điều chế được lượng oxi dùng cho phản ứng trên? (Hiệu suất phản ứng nung là H=75%) (K=39, Cl=35,5, Al=27, O=16)
a.\(n_{Al_2O_3}=\dfrac{30,6}{102}=0,3mol\)
\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
0,6 0,45 0,3 ( mol )
\(m_{Al}=0,6.27=16,2g\)
\(V_{O_2}=0,45.22,4=10,08l\)
\(V_{kk}=10,08.5=50,4l\)
b.\(2KClO_3\rightarrow\left(t^o,MnO_2\right)2KCl+3O_2\)
0,3 0,45 ( mol )
\(m_{KClO_3}=0,3.122,5=36,75g\)
c.\(2KClO_3\rightarrow\left(t^o,MnO_2\right)2KCl+3O_2\)
0,3 0,45 ( mol )
\(n_{KClO_3}=\dfrac{0,3}{75\%}=0,4mol\)
\(m_{KClO_3}=0,4.122,5=49g\)
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn 16.2g nhôm trong bình chứa khí oxi(đktc) thu được nhôm oxit al2o3 a) tính thể tích khí oxi cần dùng b) tính khối lượng al2o3 c) cần dùng bao nhiêu gam KMnO4 để điều chế vừa đủ khí oxi cho phản ứng trên
nAl=16,2/27= 0,6(mol)
a) PTHH: 4 Al +3 O2 -to-> 2 Al2O3
nO2= 3/4 . nAl=3/4 . 0,6= 0,45(mol)
=> V(O2,đktc)=0,45 x 22,4=10,08(l)
b) nAl2O3= nAl/2=0,6/2=0,3(mol)
=>mAl2O3=102. 0,3= 30,6(g)
c) 2KMnO4 -to-> K2MnO4 + MnO2 + O2
nKMnO4= 2.nO2=2. 0,45=0,9(mol)
=>mKMnO4= 158 x 0,9= 142,2(g)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 16,8 lít khí hidro.
a)Tính thể tích khí oxi và thể tích không khí cần dùng cho phản ứng trên (biết các thể tích đo ở đktc và oxi chiếm 20% thể tích không khí)
b)tính khối lượng KMnO4(hoặc KClO3)cần dùng để điều chế đc lượng oxi trên
Theo gt ta có: $n_{H_2}=0,75(mol)$
a, $2H_2+O_2\rightarrow 2H_2O$
Ta có: $n_{O_2}=0,5.n_{H_2}=0,375(mol)\Rightarrow V_{O_2}=8,4(l)\Rightarrow V_{kk}=42(l)$
b, $2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2$
Ta có: $n_{KMnO_4}=2.n_{O_2}=0,75(mol)\Rightarrow m_{KMnO_4}=118,5(g)$
Đúng 1
Bình luận (0)
a)
\(2H_2 + O_2 \xrightarrow{t^o} 2H_2O\\ V_{O_2} = \dfrac{V_{H_2}}{2} = \dfrac{16,8}{2} = 8,4(lít)\\ V_{không\ khí} = \dfrac{8,4}{20\%} = 42(lít)\)
b)
\(n_{O_2} = \dfrac{8,4}{22,4} = 0,375(mol)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ n_{KMnO_4} = 2n_{O_2} = 0,75(mol)\\ \Rightarrow m_{KMnO_4} = 0,75.158 = 118,5(gam)\\ 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\\ n_{KClO_3} = \dfrac{2}{3}n_{O_2} = 0,25(mol)\\ \Rightarrow m_{KClO_3} = 0,25.122,5 = 30,625(gam)\)
Đúng 1
Bình luận (0)
\(n_{H_2}=\dfrac{16.8}{22.4}=0.75\left(mol\right)\)
\(2H_2+O_2\underrightarrow{t^0}2H_2O\)
\(0.75...0.375\)
\(V_{O_2}=0.375\cdot22.4=8.4\left(l\right)\)
\(V_{kk}=5V_{O_2}=8.4\cdot5=42\left(l\right)\)
\(2KMnO_4\underrightarrow{t^0}K_2MnO_4+MnO_2+O_2\)
\(0.75..............................................0.375\)
\(m_{KMnO_4}=0.75\cdot158=118.5\left(g\right)\)
\(2KClO_3\underrightarrow{t^0}2KCl+3O_2\)
\(0.25.......................0.375\)
\(m_{KClO_3}=0.25\cdot122.5=30.625\left(g\right)\)
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Bài 3: Tính khối lượng KMnO4 cần điều chế được lượng oxi đủ phản ứng cho 36 g kim loại sắt. (sp Fe3O4) Bài 4: Khi đốt cháy nhôm trong khí oxi thu được nhôm oxit Al2O3. a) Tính khối lượng Nhôm và thể tích khí oxi (đktc) cần dùng để điều chế 51 gam nhôm oxit. b) Tính khối lượng kali pemanganat cần dùng để điều chế lượng khí oxi nói trên. c) Tính khối lượng kali clorat cần dùng để điều chế lượng khí oxi nói trên.Bài 5: Khi đốt cháy hoàn toàn 14,4 gam Mg trong bình chứa 4,48 lít O2...
Đọc tiếp
Bài 3: Tính khối lượng KMnO4 cần điều chế được lượng oxi đủ phản ứng cho 36 g kim loại sắt. (sp Fe3O4)
Bài 4: Khi đốt cháy nhôm trong khí oxi thu được nhôm oxit Al2O3.
a) Tính khối lượng Nhôm và thể tích khí oxi (đktc) cần dùng để điều chế 51 gam nhôm oxit.
b) Tính khối lượng kali pemanganat cần dùng để điều chế lượng khí oxi nói trên.
c) Tính khối lượng kali clorat cần dùng để điều chế lượng khí oxi nói trên.
Bài 5: Khi đốt cháy hoàn toàn 14,4 gam Mg trong bình chứa 4,48 lít O2 (đktc) thu được m gam hỗn hợp chất rắn. Giá trị của là ?
Bài 6: Đốt cháy hoàn toàn 12,8 gam Cu cần vừa đủ V lít không khí (đktc) thu được m gam CuO. Tính giá trị của m và V. Biết trong không khí oxi chiếm 20% thể tích.
Bài 7: Nung 79 gam KMnO4 thu được V lít khí O2 đo ở đktc. Biết hiệu suất phản ứng nhiệt phân là 80%, hãy tính giá trị của V ?
Bài 8: Nung 24,5 gam KClO3 thu được V lít khí O2 đo ở đktc. Biết hiệu suất phản ứng nhiệt phân là 50%, hãy tính giá trị của V ?
Bài 9: Nung m gam KClO3 thu được 6,72 lít khí O2 đo ở đktc. Biết hiệu suất phản ứng nhiệt phân là 70%, hãy tính giá trị của m ?
Bạn tách ra từng câu nhé!
Bài 3.
\(n_{Fe}=\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{36}{56}=0,6428mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,6428 ----- 0,4285 ( mol )
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,857 0,4285 ( mol )
\(m_{KMnO_4}=n_{KMnO_4}.M_{KMnO_4}=0,857.158=135,406g\)
Bài 4.
a.\(n_{Al_2O_3}=\dfrac{m_{Al_2O_3}}{M_{Al_2O_3}}=\dfrac{51}{102}=0,5mol\)
\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
1 0,75 0,5 ( mol )
\(m_{Al}=n_{Al}.M_{Al}=1.27=27g\)
\(V_{O_2}=n_{O_2}.22,4=0,75.22,4=16,8l\)
b.\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
1,5 0,75 ( mol )
\(m_{KMnO_4}=n_{KMnO_4}.M_{KMnO_4}=1,5.158=237g\)
\(2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\)
0,5 0,75 ( mol )
\(m_{KClO_3}=n_{KClO_3}.M_{KClO_3}=0,5.122,5=61,25g\)
Đúng 1
Bình luận (0)
Bài 5.
\(n_{Mg}=\dfrac{m_{Mg}}{M_{Mg}}=\dfrac{14,4}{24}=0,6mol\)
\(n_{O_2}=\dfrac{V_{O_2}}{22,4}=\dfrac{4,48}{22,4}=0,2mol\)
\(2Mg+O_2\rightarrow\left(t^o\right)2MgO\)
0,6 < 0,2 ( mol )
0,4 0,2 0,2 ( mol )
\(m_{MgO}=n_{MgO}.M_{MgO}=0,2.40=8g\)
Bài 6.
\(n_{Cu}=\dfrac{m_{Cu}}{M_{Cu}}=\dfrac{12,8}{64}=0,2mol\)
\(2Cu+O_2\rightarrow\left(t^o\right)2CuO\)
0,2 0,1 0,2 ( mol )
\(V_{kk}=V_{O_2}.5=\left(0,1.22,4\right).5=2,24.5=11,2l\)
\(m_{CuO}=n_{CuO}.M_{CuO}=0,2.80=16g\)
Đúng 2
Bình luận (1)
Đốt cháy hoàn toàn 5,4 gam nhôm. A. Tính thể tích khí oxi cần dùng (đktc) B. Tính số gam KMnO4 cần dùng để điều chế lượng oxi trên.
nAl = 5,4/27 = 0,2 (mol)
PTHH: 4Al + 3O2 -> (t°) 2Al2O3
Mol: 0,2 ---> 0,15
VO2 = 0,15 . 22,4 = 3,36 (l)
PTHH: 2KMnO4 -> (t°) K2MnO4 + MnO2 + O2
nKMnO4 = 0,15 . 2 = 0,3 (mol)
mKMnO4 = 0,3 . 158 = 47,4 (g)
Đúng 3
Bình luận (1)
Đốt cháy hoàn toàn 21,6g bột nhôm trong oxi
a. Tính thể tích khí oxi (đktc)
b. Tính khối lượng sản phẩm thu được sau phản ứng
c. Để có lượng oxi dùng cho phản ứng trên cần phải nung bao nhiêu g KClO3?
a)\(n_{Al}=\dfrac{21,6}{27}=0,8\left(m\right)\)
\(PTHH:4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
tỉ lệ :4 3 2
số mol :0,8 0,6 0,4
\(V_{O_2}=0,6.22,4=13,44\left(g\right)\)
b)\(m_{Al_2O_3}=0,4.102=40,8\left(g\right)\)
c)\(PTHH:2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
tỉ lệ : 2 2 3
số mol :0,4 0,4 0,6
\(m_{KClO_3}=0,4.122,5=49\left(g\right)\)
Đúng 1
Bình luận (0)
: Đốt cháy hoàn toàn 6,4 g Magie trong bình chứa khí oxi.
a. Viết phương trình hoá học xảy ra
b. Tính thể tích khí oxi cần dùng (đktc)
c. Tính khối lượng KMnO4 cần dùng để điều chế lượng oxi dùng cho phản ứng trên.
a.b.\(n_{Mg}=\dfrac{m}{M}=\dfrac{6,4}{24}=\dfrac{4}{15}mol\)
\(2Mg+O_2\rightarrow\left(t^o\right)2MgO\)
4/15 2/15 ( mol )
\(V_{O_2}=n.22,4=\dfrac{2}{15}.22,4=\dfrac{224}{75}l\)
c.\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
4/15 2/15 ( mol )
\(m_{KMnO_4}=n.M=\dfrac{4}{15}.158=\dfrac{632}{15}g\)
Đúng 4
Bình luận (0)
nMg = 6,4 : 24= 0,26(mol)
pthh : 2Mg+O2 -t--> 2MgO
0,26 --> 0,13 (mol )
=> VO2(đktc) = 0,13.22,4=2,912(l)
pthh : 2KMnO4-t--> K2MnO4 + MnO2+ O2
0,26<------------------------------0,13(mol)
=> mKMnO4 = 0,26.158= 41,08(g)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 3,1 (g) phot pho trong bình chứa khí oxi thu được P205 a) viết PTHH của phản ứng? b) Tính thể tích khí oxi đã phản ứng? c) tính khối lượng KMnO4 cần dùng để điều chế được lượng khí oxi dùng cho phản ứng trên? d) phân loại các phản ứng trên?
nP = 3,1 : 31 = 0,1 (mol)
pthh : 4P + 5O2 -t--> 2P2O5 (1)
0,1--> 0,125 (mol)
=> VO2 = 0,125 .22,4 = 2,8(l)
pthh : 2KMnO4 -t--> K2MnO4 + MnO2 +O2 (2)
0,25<--------------------------- 0,125(mol)
=> mKMnO4 = 0,25 .158 = 39,5(g)
d ) (1) là Phản ứng hóa hợp
(2) là phản ứng phân hủy
Đúng 3
Bình luận (0)
nP = 3,1/31 = 0,1 (mol)
PTHH: 4P + 5O2 -> (t°) 2P2O5 (phản ứng hóa hợp)
Mol: 0,1 ---> 0,125
VO2 = 0,125 . 22,4 = 2,8 (l)
PTHH: 2KMnO4 -> (t°) K2MnO4 + MnO2 + O2 (phản ứng phân hủy)
nKMnO4 = 0,125 . 2 = 0,25 (mol)
mKMnO4 = 0,25 . 158 = 39,5 (g)
Đúng 3
Bình luận (1)
a) PTHH: 4P (0,1 mol) + 5O2 (0,125 mol) \(\underrightarrow{t^o}\) 2P2O5.
b) Ở đktc: \(V_{O_2pư}\)=0,125.22,4=2,8 (lít).
c) Điều chế oxi tử KMnO4:
2KMnO4 (0,25 mol) \(\underrightarrow{t^o}\) K2MnO4 + MnO2↓ + O2↑ (0,125 mol).
Khối lượng KMnO4 cần dùng:
\(m_{KMnO_4}\)=0,25.158=39,5 (g).
d) Hai phản ứng trên đều là phản ứng oxy hóa - khử.
Đúng 1
Bình luận (0)
B8 : Đốt cháy 36g kim loại trong bình chứa khí oxi đến phản ứng hoàn toàn a) Tính khối lượng magie oxit tạo thành b) Tính khối lượng kalipenmanganat cần đùng để điều chế lượng oxi dùng cho phản ứng trên . c) Dùng lượng oxi trên oxi hóa hoàn toàn 96g một kim loại M hóa trị II . Xác định tên và KHH của kim loại đã dùng . giúp mk vs ạ :(( , mai mk thi r
Đọc tiếp
B8 : Đốt cháy 36g kim loại trong bình chứa khí oxi đến phản ứng hoàn toàn
a) Tính khối lượng magie oxit tạo thành
b) Tính khối lượng kalipenmanganat cần đùng để điều chế lượng oxi dùng cho phản ứng trên .
c) Dùng lượng oxi trên oxi hóa hoàn toàn 96g một kim loại M hóa trị II . Xác định tên và KHH của kim loại đã dùng .
giúp mk vs ạ :(( , mai mk thi r