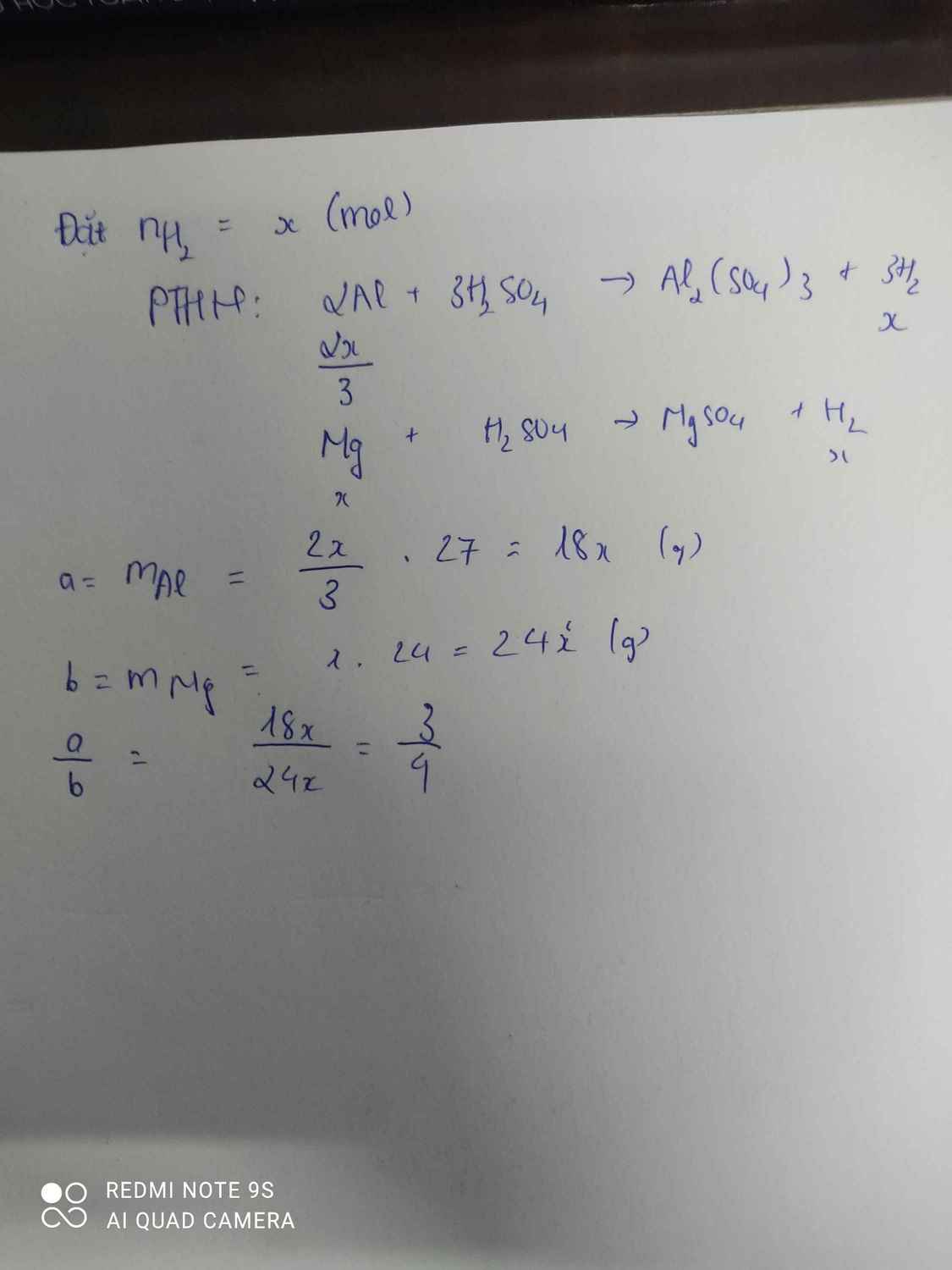Hòa tan a gam Al và b gam Zn bằng dung dịch HCl dư , thu được những thể tích khí H2 như nhau ( ở cùng điều kiện nhiệt độ và áp suất ) . Tính tỉ lệ a : b

Những câu hỏi liên quan
4.2 Hòa tan a gam Al và b gam Mg vào dung dịch axit H2SO4 dư thu được những thể tích khí H2 bằng nhau trong cùng điều kiện. tính tỉ lệ a/b
Hòa tan a gam Al và b gam Zn vào dung dịch axit H2SO4 dư thu được những thể tích khí H2 bằng nhau. Tính tỉ lệ a:b
Hãy cứu lấy tui~
Cảm ơn nhiềuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuuu~
Gọi \(n_{H_2}=x\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(\dfrac{2}{3}x\) x ( mol )
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(x\) x ( mol )
\(a:b=\dfrac{\dfrac{2}{3}x.27}{65x}=\dfrac{18x}{65x}=\dfrac{18}{65}\)
Đúng 3
Bình luận (1)
Đặt nH2 là x(mol)
PTHH: 2Al + 3H2SO4 -----> Al2(SO4)3 + 3H2
2x/3 x
mAl= 2x/3 . 27= 18x (g)
PTHH: Mg + H2SO4 -------> MgSO4 + H2
x x
mMg= 1x . 24= 24x (g)
Theo tỉ lệ: a/b= 18x/24x= 3/4
Đúng 1
Bình luận (1)
Hòa tan a gam Al và b gam Zn bằng dung dịch HCl thu được những thể tích khí Hidro bằng nhau.Tính tỉ lệ a,b
2Al+6HCl-->2AlCl3+3H2 (1)
Zn+2HCl-->ZnCl2+H2 (2)
Gọi số mol của H2 ở 2 pt là a(mol)
Số mol của Al là:
nAl=2/3nH2=2/3.a(mol)
K/lượng của Al là:
m=n.M=2/3a.27=18a(g)
Số mol của Zn là:
nZn=nH2=a(mol)
K/lượng của Zn là:
m=n.M=a.65(g)
Tỉ lệ a,b là:
a/b=mAl/mZn=18a/65a=18/65
Vậy tỉ lệ a/b là 18/65
Đúng 1
Bình luận (0)
Có một hỗn hợp bột các kim loại Al và Fe. Nếu cho a gam hỗn hợp này tác dụng với dung dịch NaOH dư, người ta thu được một thể tích khí H2 đúng bằng thể tích của 9,6 gam khí oxi (đo ở cùng điều kiện nhiệt độ và áp suất). Nếu cho a gam hỗn hợp trên tác dụng với dung dịch HCl dư, phản ứng xong thu được 8,96 lít khí H2 (đktc).a) Viết các phương trình phản ứng xảy ra.b) Tính a và thành phần % khối lượng mỗi kim loại trong hỗn hợp.
Đọc tiếp
Có một hỗn hợp bột các kim loại Al và Fe. Nếu cho a gam hỗn hợp này tác dụng với dung dịch NaOH dư, người ta thu được một thể tích khí H2 đúng bằng thể tích của 9,6 gam khí oxi (đo ở cùng điều kiện nhiệt độ và áp suất). Nếu cho a gam hỗn hợp trên tác dụng với dung dịch HCl dư, phản ứng xong thu được 8,96 lít khí H2 (đktc).
a) Viết các phương trình phản ứng xảy ra.
b) Tính a và thành phần % khối lượng mỗi kim loại trong hỗn hợp.
a)
2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
2Al + 6HCl --> 2AlCl3 + 3H2
Fe + 2HCl --> FeCl2 + H2
b)\(n_{O_2}=\dfrac{9,6}{32}=0,3\left(mol\right)\) => \(n_{H_2}=0,3\left(mol\right)\)
PTHH: 2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
0,2<---------------------------------------0,3
=> nAl = 0,2 (mol)
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,2---------------------->0,3
Fe + 2HCl --> FeCl2 + H2
0,1<---------------------0,1
=> a = 0,2.27 + 0,1.56 = 11(g)
\(\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2.27}{11}.100\%=49,09\%\\\%m_{Fe}=\dfrac{0,1.56}{11}.100\%=50,91\%\end{matrix}\right.\)
Đúng 5
Bình luận (2)
Hỗn hợp X gồm x mol Na, y mol Zn và z mol Fe; hỗn hợp Y gồm 18y gam Al và (11,5x + 28z) gam
kim loại M. Hòa tan hoàn toàn X hoặc Y bằng lượng dư dung dịch H2SO4 0,5M đều thu được V lít khí H2
(đo ở cùng điều kiện nhiệt độ, áp suất).
Xác định kim loại M.
B1: ở cùng điều kiện nhiệt độ và áp suất: a mol khí H2 ( khối lương 4g) và x mol khí cacbonic có khối lượng y gam chiếm thể tích bằng nhaua) Tính x và yb) Tính số nguyên tử và số phân tử trong mỗi lượng chất trên B2: Hòa tan hoàn toàn 9,6 gam một kim loại X có hóa trị II bằng dung dịch HCl vừa đủ. Khi phản ứng kết thúc thu được 8,96 lít khí (đktc)a) Xác định tên kim loại X ?b) Tính thể tích dung dịch HCl 1 M cần dùng cho phản ứng trên B3: Để khử hoàn toàn 47,2 gam hỗn hợp CuO, FeO, Fe3O4 cần dùn...
Đọc tiếp
B1: ở cùng điều kiện nhiệt độ và áp suất: a mol khí H2 ( khối lương 4g) và x mol khí cacbonic có khối lượng y gam chiếm thể tích bằng nhau
a) Tính x và yb) Tính số nguyên tử và số phân tử trong mỗi lượng chất trên B2: Hòa tan hoàn toàn 9,6 gam một kim loại X có hóa trị II bằng dung dịch HCl vừa đủ. Khi phản ứng kết thúc thu được 8,96 lít khí (đktc)a) Xác định tên kim loại X ?b) Tính thể tích dung dịch HCl 1 M cần dùng cho phản ứng trên B3: Để khử hoàn toàn 47,2 gam hỗn hợp CuO, FeO, Fe3O4 cần dùng V lít khí H2 ( ở đktc). Sau pứ thu được m gam kim loại và 14,4 gam nướca) Viết PTHH xảy rab) Tính giá trị m và V? B4: Cho 21,5 gam hỗn hợp kim loại M và M2O3 nung ở nhiệt độ cao, rồi dẫn luồng khí CO đi qua để pứ xảy ra hoàn toàn thu được m gam kim loại và 6,72 lít khí CO2 ( ở đktc) a) Xác định kim loại M và oxit M2O3, gọi tên các chất đó?b) Tìm m biết tỉ lệ số mol của M và M2O3 là 1:1 B5: Hòa tan hoàn toàn 6,5 gam Zn bằng dung dịch H2SO4 loãng vừa đủ thu được dung dịch A và V lít khí ở đktc.Tính klg chất tan có trong dd A4) x,y lần lượt là số mol của M và M2O3
=> nOxi=3y=nCO2=0,3 => y=0,1
Đề cho x=y=0,1 =>0,1M+0,1(2M+48)=21,6 =>M=56 => Fe và Fe2O3
=> m=0,1.56 + 0,1.2.56=16,8
Đúng 1
Bình luận (0)
2)X + 2HCl === XCl2 + H2
n_h2 = 0,4 => X = 9,6/0,4 = 24 (Mg)
=>V_HCl = 0,4.2/1 = 0,8 l
Đúng 1
Bình luận (0)
3) n_H2O = 0,8 => n_H2 = 0,8 => v = 0,8.22,4 = 17,92 l
áp dụng đl bảo toàn khối lượng
=> 47,2 + 0,8.2 = m + 14,4
=> m = 34,4 (g)
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
hòa tan 2,7 gam al bằng dung dịch hcl thu được a gam muối khan. tính thể tích khí h2 thoát ra ở điều kiện tiêu chuẩn : a,tính Vh2 đktc b,Tính C% muối khan thu được ,biết rằng sau phản ứng khối lượng dung dịch là 500g
a) 2Al + 6HCl -> 2AlCl3 + 3H2
b)nAl = 2.7/27=0.1mol
2Al + 6HCl -> 2AlCl3 + 3H2
(mol) 0.1 0.3 0.1 0.15
VH2 = 0.15*22.4=3.36l
mAlCl3= 0.1*133.5=13.35g
=>C%=\(\dfrac{13,35}{500+27}100=2,533\%\)
Đúng 1
Bình luận (4)
Câu 2: Hòa tan hoàn toàn 13 gam zinc (Zn) thì cần dung dịch hydrochloric acid (HCl), sau khi phản ứng kết thúc thu được zinc chloride (ZnCl2) và khí hydrogen (H2).
a) Tính thể tích khí hydrogen thu được ở điều kiện chuẩn (250C và 1 bar)?
b) Tính khối lượng zinc chloride thu được?
c) Nếu sau phản ứng trên thu được 3,225 lít khí hydrogen ở điều kiện chuẩn thì hiệu suất của phản ứng bằng bao nhiêu?
Đọc tiếp
Câu 2: Hòa tan hoàn toàn 13 gam zinc (Zn) thì cần dung dịch hydrochloric acid (HCl), sau khi phản ứng kết thúc thu được zinc chloride (ZnCl2) và khí hydrogen (H2).
a) Tính thể tích khí hydrogen thu được ở điều kiện chuẩn (250C và 1 bar)?
b) Tính khối lượng zinc chloride thu được?
c) Nếu sau phản ứng trên thu được 3,225 lít khí hydrogen ở điều kiện chuẩn thì hiệu suất của phản ứng bằng bao nhiêu?
Ta có: \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
a, nH2 = nZn = 0,2 (mol)
⇒ VH2 = 0,2.24,79 = 4,958 (l)
b, nZnCl2 = nZn = 0,2 (mol)
⇒ mZnCl2 = 0,2.136 = 27,2 (g)
c, \(H=\dfrac{3,225}{4,958}.100\%\approx65,05\%\)
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 3,9 gam Zn vào dung dịch HCl 14,6 % a. Tính số gam dung dịch HCL 14,6% cần dùng và thể tích khí h2 thoát ra ở điều kiện tiêu chuẩn
Theo gt ta có: $n_{Zn}=0,06(mol)$
$Zn+2HCl\rightarrow ZnCl_2+H_2$
a, Ta có: $n_{HCl}=0,12(mol)\Rightarrow m_{ddHCl}=30(g)$
b, Ta có: $n_{H_2}=0,06(mol)\Rightarrow V_{H_2}=1,344(l)$
Đúng 2
Bình luận (0)
a)
n Zn = 3,9.65 = 0,06(mol)
Zn + 2HCl $\to$ ZnCl2 + H2
Theo PTHH :
n HCl = 2n Zn =0,12(mol)
=> mdd HCl = 0,12.36,5/14,6% = 30(gam)
n H2 = n Zn = 0,06(mol)
V H2 = 0,06.22,4 = 1,344 lít
Đúng 1
Bình luận (0)
nZn=0,06(mol)nZn=0,06(mol)
Zn+2HCl→ZnCl2+H2Zn+2HCl→ZnCl2+H2
a, Ta có: nHCl=0,12(mol)⇒mddHCl=30(g)nHCl=0,12(mol)⇒mddHCl=30(g)
b, Ta có: nH2=0,06(mol)⇒VH2=1,344(l)
Đúng 0
Bình luận (0)