Cho 8,3 gam hỗn hợp gồm Al, Fe có số mol bằng nhau tác dụng với dung dịch H2SO4 thu được dung dịch A và V lit H2.
a. Tính khối lượng H2SO4 phản ứng.
b. Tính V và tính khối lượng muối trong dung dịch A
Cho m gam hỗn hợp gồm Fe và Fe2O3 tác dụng với dung dịch H2SO4 vừa đủ thu được dung dịch A chứa 55,2 gam muối và 2,24 lit H2.
a. Tính m
b. Tính khối lượng H2SO4 phản ứng
Biết Fe2O3 + H2SO4 ® Fe2(SO4)3 + H2O
Cho hỗn hợp gồm 5,4 gam Al và 10,2 gam Al2O3 tác dụng vừa đủ với dung dịch HCl thu được dung dịch A và V lit H2.
a. Tính khối lượng HCl phản ứng
b. Tính V và tính khối lượng muối thu được
Biết Al2O3 + HCl ® AlCl3 + H2O
Ta có: \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
\(n_{Al_2O_3}=\dfrac{10,2}{102}=0,1\left(mol\right)\)
PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
a, Theo PT: \(n_{HCl}=3n_{Al}+6n_{Al_2O_3}=1,2\left(mol\right)\)
\(\Rightarrow m_{HCl}=1,2.36,5=43,8\left(g\right)\)
b, Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}=0,3\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)
\(n_{AlCl_3}=n_{Al}+2n_{Al_2O_3}=0,4\left(mol\right)\)
\(\Rightarrow m_{AlCl_3}=0,4.133,5=53,4\left(g\right)\)
cho 11g một hỗn hợp gồm Fe và Al tác dụng vừa đủ với 200ml dung dịch axit H2SO4 2(M), thì thu được V lit khí H2 (dktc)
a) xác định thành phần % về khối lượng của mỗi kim loại trong hỗn hợp đầu
b) tìm V
c) tính nồng độ các muối trong dung dịch sau phản ứng
\(n_{H_2SO_4}=0,2.2=0,4\left(mol\right)\)
Fe + H2SO4 → FeSO4 + H2
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Gọi x,y lần lượt là số mol Fe, Al
\(\left\{{}\begin{matrix}56x+27y=11\\x+\dfrac{3}{2}y=0,4\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
=>\(\%m_{Fe}=\dfrac{0,1.56}{11}.100=50,91\%\)
=> %m Al = 100 - 50,91 =49,09 %
b)Theo PT: \(n_{H_2}=n_{H_2SO_4}=0,4\left(mol\right)\)
=> \(V_{H_2}=0,4.22,4=8,96\left(l\right)\)
c) \(CM_{FeSO_4}=\dfrac{0,1}{0,2}=0,5M\)
\(CM_{Al_2\left(SO_4\right)_3}=\dfrac{\dfrac{0,2}{2}}{0,2}=0,5M\)
Cho 19,3 gam hỗn hợp gồm Al và Fe tác dụng vừa đủ với 200 ml dung dịch gồm HCl 2M và H2SO4 2,25M (loãng) thu được V lít khí H2 (đktc) và dung dịch B.
a) Tính thành phần phần trăm khối lượng của Al và Fe trong hỗn hợp ban đầu.
b) Tính tổng khối lượng muối có trong dung dịch B.
\(n_{Al}=a\left(mol\right)\)
\(n_{Fe}=b\left(mol\right)\)
\(m=27a+56b=19.3\left(g\right)\left(1\right)\)
\(n_{H^+}=0.2\cdot2+0.2\cdot2.25\cdot2=1.3\left(mol\right)\)
\(2Al+6H^+\rightarrow2Al^{3+}+3H_2\)
\(Fe+2H^+\rightarrow Fe^{2+}+H_2\)
\(n_{H^+}=3a+2b=1.3\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.3,b=0.2\)
\(\%Al=\dfrac{0.3\cdot27}{19.3}\cdot100\%=41.96\%\)
\(\%Fe=58.04\%\)
\(b.\)
\(n_{H_2}=\dfrac{1}{2}n_{H^+}=0.65\left(mol\right)\)
Bảo toàn khối lượng :
\(m_{Muối}=19.3+0.4\cdot36.5+0.45\cdot98-0.65\cdot2=76.7\left(g\right)\)
Hoà tan 19.3 gam hỗn hợp X (Al,Fe) bằng dung dịch H2SO4 loãng dư thu được V lít khí H2 và dung dịch A, cô cạn dung dịch A thu được 81.7 gam hỗn hợp muối
a, Tính % khối lượng của mỗi chất trong hỗn hợp đầu
b, Tính V (đktc)
c, tính khối lượng của H2SO4 đã tham gia phản ứng
Gọi x và y lần lượt là số mol Fe và Al tham gia phản ứng
a/PTHH: Fe + H2SO4 -----> FeSO4 + H2
(mol) x x x x
PTHH: 2Al + 3H2SO4 -----> Al2(SO4)3 + 3H2
(mol) y 3y/2 y/2 3y/2
Suy ra hệ : \(\begin{cases}152x+\frac{342y}{2}=81,7\\56x+27y=19,3\end{cases}\) \(\Leftrightarrow\begin{cases}x=0,2\\y=0,3\end{cases}\)
=> mFe = 0,2.56 = 11,2 (g)
\(\Rightarrow\%Fe=\frac{11,2}{19,3}.100\approx58,03\%\)
%Al = 100% - 58,03% = 41,97%
b/ nH2 = x+3y/2 = 0,2 + 3.0,3/2 = 0,65 (mol)
=> VH2 = 22,4.0,65 = 14,56 (l)
c/ nH2SO4 = x+3y/2 = 0,65 (mol)
=> mH2SO4 = 98.0,65 = 63,7 (g)
1/ Cho 0,83g hổn hợp gồm Al và Fe tác dụng vừa đủ với dd H2SO4 20%, sau phản ứng thu được 0,56 lit khí H2 ( đktc)
a) Tính thành phần % theo khối lượng mỗi kim loại trong hỗn hợp ban đầu.
b) Tính khối lượng dung dịch h2so4 20% đã dùng
a, Ta có: 27nAl + 56nFe = 0,83 (1)
PT: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}+n_{Fe}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow n_{Al}=n_{Fe}=0,01\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,01.27}{0,83}.100\%\approx32,53\%\\\%m_{Fe}\approx67,47\%\end{matrix}\right.\)
b, nH2SO4 = nH2 = 0,025 (mol)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{0,025.98}{20\%}=12,25\left(g\right)\)
Cho 10,38 gam hỗn hợp gồm Fe, Al và Ag chia làm 2 phần bằng nhau:
Phần 1: Tác dụng với dung dịch H2SO4 loãng dư thu được 2,352 lit khi (đktc).
Phần 2: Tác dụng với dung dịch H2SO4 đặc, nóng dư thu được 2,912 lit khí SO2 (đktc).
a. Tính khối lượng từng kim loại trong hỗn hợp ban đầu.
b. Tính số mol axit tham gia phản ứng ở mỗi phần.
a)
Gọi số mol Fe, Al, Ag trong mỗi phần là a, b,c (mol)
=> 56a + 27b + 108c = 5,19 (1)
Phần 1:
\(n_{H_2}=\dfrac{2,352}{22,4}=0,105\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
a----->a------------------>a
2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
b------>1,5b------------------->1,5b
=> a + 1,5b = 0,105 (2)
Phần 2:
\(n_{SO_2}=\dfrac{2,912}{22,4}=0,13\left(mol\right)\)
PTHH: 2Al + 6H2SO4 --> Al2(SO4)3 + 3SO2 + 6H2O
b----->3b-------------------->1,5b
2Fe + 6H2SO4 --> Fe2(SO4)3 + 3SO2 + 6H2O
a------>3a--------------------->1,5a
2Ag + 2H2SO4 --> Ag2SO4 + SO2 + 2H2O
c-------->c------------------>0,5c
=> 1,5a + 1,5b + 0,5c = 0,13 (3)
(1)(2)(3) => a = 0,03 (mol); b = 0,05 (mol); c = 0,02 (mol)
=> \(\left\{{}\begin{matrix}m_{Fe}=2.0,03.56=3,36\left(g\right)\\m_{Al}=2.0,05.27=2,7\left(g\right)\\m_{Ag}=2.0,02.108=4,32\left(g\right)\end{matrix}\right.\)
b)
- Phần 1:
\(n_{H_2SO_4}=a+1,5b=0,105\left(mol\right)\)
- Phần 2:
\(n_{H_2SO_4}=3a+3b+c=0,26\left(mol\right)\)
Cho hỗn hợp X gồm 0,35 mol Fe và 0,04 mol Al tác dụng với dung dịch chứa Cu(NO3)2 và H2SO4, thu được dung dịch Y, hỗn hợp hai khí NO và H2 (có tỉ khối so với H2 bằng 5,2) và 10,04 gam hỗn hợp hai kim loại (trong đó kim loại yếu hơn chiếm 19,1235% theo khối lượng). Cô cạn dung dịch Y, thu được hỗn hợp muối khan Z. Phần trăm khối lượng muối nhôm trong Z gần nhất với
A. 4,13.
B. 39,89.
C. 17,15.
D. 35,75.
Đáp án C
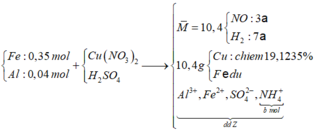
nCu = (10,4. 0,191235 )/64= 0,03 (mol) => nCu(NO3)2 = 0,03
=> nFe dư = ( 10,4 -0,03.64)/56 = 0,145 (mol) => nFe pư = 0,35 – 0,145 = 0,205 (mol)
Hỗn hợp khí có M = 10,4 => Dùng quy tắc đường chéo => nNO = 3a và nH2 = 7a (mol)
Bảo toàn nguyên tố N ta có: nNO + nNH4+ = 2nCu(NO3)2
=> 3a + b = 0,03.2 (1)
Bảo toàn e: 2nFe pư + 3nAl = 3nNO + 2nH2 + 8nNH4+ + 2nCu2+
=> 2.0,205 + 3. 0,04 = 3.3a + 2.7a + 8b + 2. 0,03
=> 23a + 8b = 0,47 (2)
Từ (1) và (2) => a = 0,01 và b = 0,03 (mol)
Bảo toàn điện tích với dung dịch Y gồm Al3+ (0,04 ); Fe2+: (0,205); NH4+ (0,03) và SO42-
=> 3.0,04 + 2.0,205 = 0,03 + 2nSO4
=> nSO4 = 0,28 (mol)
=> mmuối = mAl3+ + mFe2+ + mNH4+ + mSO42-
= 0,04.27 + 0,205.56 + 0,03.18 + 0,28.96
= 39,98 (g)
% Al2(SO4)3 = (0,02. 342) :39,98 ).100% = 17,11% ≈ 17,15%
Hòa tan hết 14,76 gam hỗn hợp gồm Mg, Al, MgCO3, Al(NO3)3 trong dung dịch chứa 0,05 mol HNO3 và 0,45 mol H2SO4, sau phản ứng kết thúc thu được dung dịch X chỉ chứa các muối trung hòa và hỗn hợp khí Y gồm CO2, N2, N2O và H2 (trong đó H2 có số mol là 0,08 mol). Tỉ khối của Y so với He bằng 135/29. Cho dung dịch X tác dụng với dung dịch NaOH dư, thấy lượng NaOH phản ứng 40,0 gam, thu được 16,53 gam kết tủa. Phần trăm về khối lượng của N2 trong hỗn hợp Y là:
A. 20,74%.
B. 25,93%.
C. 15,56%.
D. 31,11%.