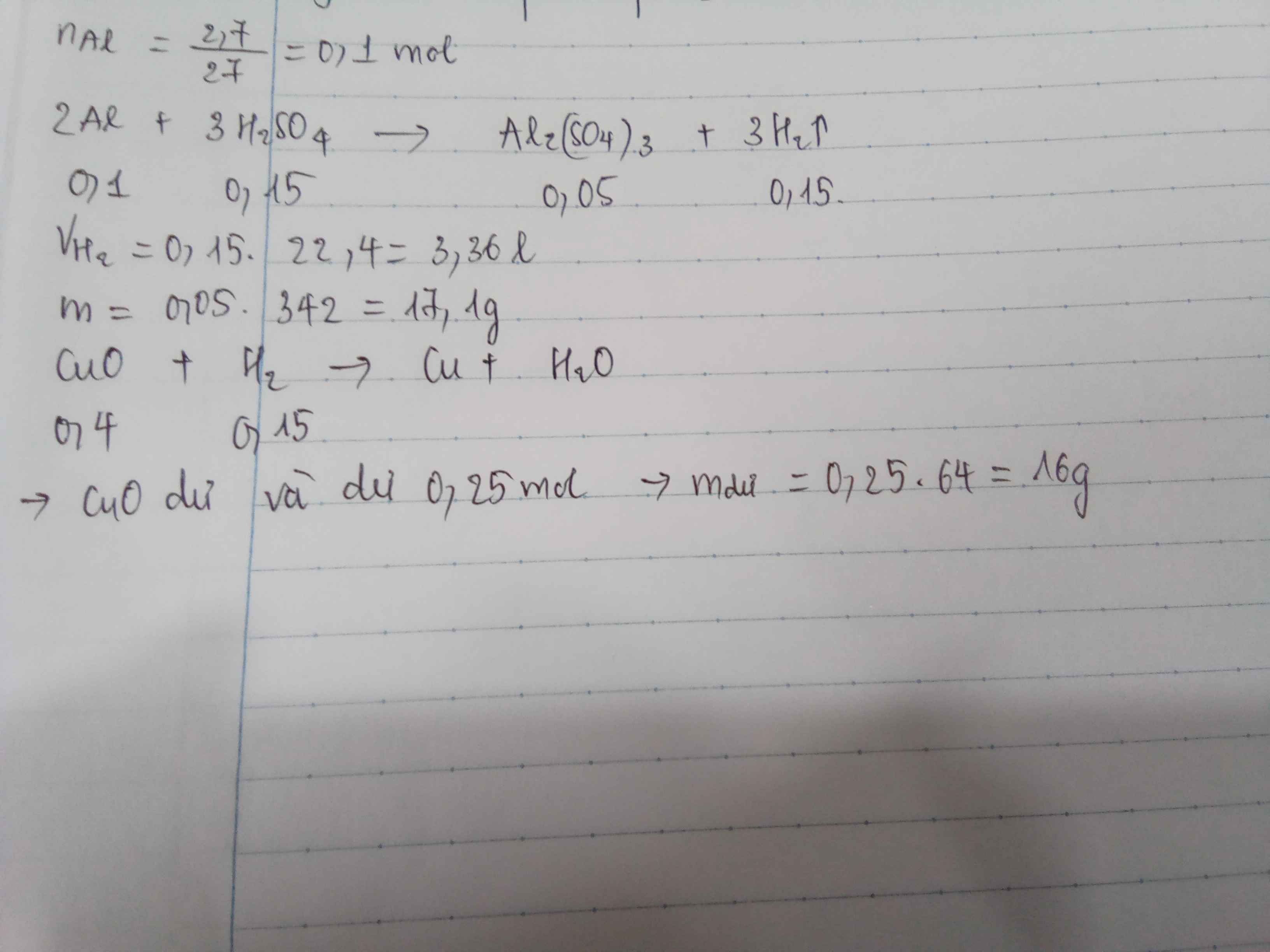cho a( g) ba tác dụng với dung dịch có chứa 9,8(g) h2so4 thu được 6,72 lít H2 ở điều kiện tiêu chuẩn.tính a

Những câu hỏi liên quan
Câu hỏi :a) Cho 11,2 g Fe tác dụng với dung dịch HCl . Tính thể tích H2 thu được ở điều kiện xác định ?b) Cho Al tác dụng với dung dịch HCl thu được AlCl3 và 6,72 lít H2 . Ở điều kiện tiêu chuẩn hãy tính khối lượng Al đã phản ứng ?
Đọc tiếp
Câu hỏi :
a) Cho 11,2 g Fe tác dụng với dung dịch HCl . Tính thể tích H2 thu được ở điều kiện xác định ?
b) Cho Al tác dụng với dung dịch HCl thu được AlCl3 và 6,72 lít H2 . Ở điều kiện tiêu chuẩn hãy tính khối lượng Al đã phản ứng ?
Trong 26 g Zn bỏ vào bình chứa dung dịch H2SO4 dư Sau khi phản ứng kết thúc thì thu được 6,72 lít H2 ở điều kiện tiêu chuẩn Tính khối lượng tạp chất có trong miếng Zn
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Theo PT: \(n_{Zn}=n_{H_2}=0,3\left(mol\right)\Rightarrow m_{Zn}=0,3.65=19,5\left(g\right)\)
⇒ m tạp chất = 26 - 19,5 = 6,5 (g)
Đúng 2
Bình luận (0)
Cho sắt tác dụng với 200 ml dung dịch H2 SO4 thu được 6,72 lít khí bay ra ở điều kiện tiêu chuẩn vào dung dịch FeSO4 a Tính khối lượng sắt tham gia phản ứng B Tính nồng độ mol dung dịch H2SO4 ban đầu C nếu cho lượng sắt ở trên phản ứng với 49 gam dung dịch H2SO4 40% tính nồng độ các dung dịch sau phản ứng
Sửa lại câu c .
\(n_{H_2SO_4}=\dfrac{49.40}{100}:98=0,2\left(mol\right)\)
\(PTHH:\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
trc p/u : 0,3 0,2
p/u : 0,2 0,2 0,2 0,2
sau : 0,1 0 0,2 0,2
-> Fe dư
\(m_{ddFeSO_4}=0,3.56+49-0,4=65,4\left(g\right)\) ( ĐLBTKL )
\(m_{FeSO_4}=0,2.152=30,4\left(g\right)\)
\(C\%=\dfrac{30,4}{65,4}.100\%\approx46,48\%\)
Đúng 2
Bình luận (0)
PTHH :
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
0,3 0,3 0,3 0,3
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(a,m_{Fe}=0,3.56=16,8\left(g\right)\)
\(b,C_M=\dfrac{n}{V}=\dfrac{0,3}{0,2}=1,5M\)
\(c,n_{H_2SO_4}=\dfrac{\dfrac{49.40}{100}}{98}=0,2\left(mol\right)\)
\(\rightarrow n_{FeSO_4}=n_{H_2SO_4}=0,2\left(mol\right)\)
\(m_{FeSO_4}=0,2.152=30,4\left(g\right)\)
\(m_{ddFeSO_4}=49+\left(0,2.56\right)-0,2.2=59,8\left(g\right)\)( định luật bảo toàn khối lượng )
\(C\%=\dfrac{30,4}{59,8}.100\%\approx50,84\%\)
Đúng 1
Bình luận (1)
a) Cho Fe tác dụng vừa hết với dung dịch chứa 7,3 g HCl có PTHH là Fe + 2HCl → FeCl2 +H2. Khối lượng sắt thu được làb) Cho kim loại R hóa trị III tác dụng hết với dung dịch H2SO4 thu được 6,72 lít H2 đktc và 34,2 gam R2(SO4)3. Biết PTHH là 2R + 3H2SO4 → R2(SO4)3 + 3H2. R làc) Cho 8 gam Fe2O3 tác dụng vừa hết với HCl: Fe2O3 + 6HCl → FeCl3 +3H2O. Khối lượng FeCl3 làd) Cho kim loại nhôm (Al) tác dụng vừa hết với 7,3 g HCl: 2Al+ 6HCl → 2AlCl3 +3H2. Tính thể tích khí H2 sinh ra ở đktc.e) Cho 5,1 g...
Đọc tiếp
a) Cho Fe tác dụng vừa hết với dung dịch chứa 7,3 g HCl có PTHH là Fe + 2HCl → FeCl2 +H2. Khối lượng sắt thu được là
b) Cho kim loại R hóa trị III tác dụng hết với dung dịch H2SO4 thu được 6,72 lít H2 đktc và 34,2 gam R2(SO4)3. Biết PTHH là 2R + 3H2SO4 → R2(SO4)3 + 3H2. R là
c) Cho 8 gam Fe2O3 tác dụng vừa hết với HCl: Fe2O3 + 6HCl → FeCl3 +3H2O. Khối lượng FeCl3 là
d) Cho kim loại nhôm (Al) tác dụng vừa hết với 7,3 g HCl: 2Al+ 6HCl → 2AlCl3 +3H2. Tính thể tích khí H2 sinh ra ở đktc.
e) Cho 5,1 gam Al2O3 tác dụng vừa hết với HCl: Al2O3 + 6HCl → AlCl3 +3H2O. Tính khối lượng AlCl3 tạo thành.
f) Cho Mg tác dụng hết với dung dịch HCl thu được 4,48 lít H2 đktc, biết rằng R có phản ứng sau: Mg + 2HCl → MCl2 + H2. Số mol HCl phản ứng là
cho Al tác dụng với dung dịch H2 SO4 thu được 6,72 lít khí ở điều kiện tiêu chuẩn A viết phương trình hóa học b tính khối lượng muối tạo thành sau phản ứng
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\\ a.2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ b.n_{Al_2\left(SO_4\right)_3}=\dfrac{0,3}{3}=0,1mol\\ m_{Al_2\left(SO_4\right)_3}=0,1.342=34,2g\)
Đúng 2
Bình luận (3)
Cho 2,7 gam nhôm tác dụng hết với dung dịch H2SO4 sau phản ứng thu được với V lít khí H2 ở điều kiện tiêu chuẩn và m gam muối.
a/ Viết phương trình hóa học
b/ Tính giá trị V
c/ Tính giá trị m
d/ Lượng khí Hidro thu được ở trên qua bình đựng 32 g CuO nung nóng. Hỏi chất nào còn dư sau phản ứng?
Tính thể tích khí H2 (đktc) thu được khi cho:
a. 4,8 g Mg tác dụng với dung dịch có chứa 18,25 g HCl.
b. 2,8 g Fe tác dụng với dung dịch có chứa 9,8 g H2SO4.
c. 14,95 g Zn tác dụng với dung dịch có chứa 21,9 g HCl.
giúp mình với ạ mình cần gấp
\(a,n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\ n_{HCl}=\dfrac{18,25}{36,5}=0,5\left(mol\right)\)
PTHH: Mg + 2HCl ---> MgCl2 + H2
LTL: \(0,2< \dfrac{0,5}{2}\) => HCl dư
Theo pthh: nH2 = nMg = 0,2 (mol)
=> VH2 = 0,2.22,4 = 4,48 (l)
\(b,n_{Fe}=\dfrac{2,8}{56}=0,.05\left(mol\right)\\ n_{H_2SO_4}=\dfrac{9,8}{98}=0,1\left(mol\right)\)
PTHH: Fe + H2SO4 ---> FeSO4 + H2
LTL: 0,05 < 0,1 => H2SO4 dư
Theo pthh: nH2 = nFe = 0,05 (mol)
=> VH2 = 0,05.22,4 = 1,12 (l)
\(c,n_{Zn}=\dfrac{14,95}{65}=0,23\left(mol\right)\\ n_{HCl}=\dfrac{21,9}{36,5}=0,6\left(mol\right)\)
PTHH: Zn + 2HCl ---> ZnCl2 + H2
LTL: \(0,23< \dfrac{0,6}{2}\) => HCl dư
Theo pthh: nH2 = nZn = 0,23 (mol)
=> VH2 = 0,23.22,4 = 5,152 (l)
Đúng 2
Bình luận (0)
X gồm Na và Ba cho a gam x tác dụng vừa đủ với dung dịch HCl thu được 3,36 l khí H2 ở điều kiện tiêu chuẩn cho b gam x tác dụng vừa đủ với 10,8 g nước.
a, viết các phương trình xảy ra. b, Tính tỉ lệ khối lượng a / b
Xem chi tiết
\(a) 2Na + 2HCl \to 2NaCl + H_2\\ Ba + 2HCl \to BaCl_2 + H_2\\ 2Na + 2H_2O \to 2NaOH + H_2\\ Ba + 2H_2O \to Ba(OH)_2 + H_2\)
\(TN1 : n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)\\ n_{Na} = x ; n_{Ba} = y\\ n_{H_2} = 0,5x + y = 0,15\\ TN2 : n_{Na} = xk ; n_{Ba} = yk\\ n_{H_2O} = n_{Na} + 2n_{Ba} =xk + 2yk = k.0,15.2 = \dfrac{10,8}{22,4} = 0,45\\ \Rightarrow k = 1,5\\ Suy\ ra: \dfrac{a}{b} = k = 1,5\)
Đúng 2
Bình luận (0)
Cho 6,8 gam hỗn hợp các kim loại Al, Cr, Fe tác dụng với lượng dư dung dịch
H
2
SO
4
loãng nóng (trong điều kiện không có không khí), thu được dung dịch X và 6,72 lít khí
H
2
(ở đktc). Cô cạn dung dịch X (trong điều kiện không có không khí) được m gam muối khan. Giá trị của m là: A. 35,6 B. 22,5 C. 64,4 D. 21,2
Đọc tiếp
Cho 6,8 gam hỗn hợp các kim loại Al, Cr, Fe tác dụng với lượng dư dung dịch H 2 SO 4 loãng nóng (trong điều kiện không có không khí), thu được dung dịch X và 6,72 lít khí H 2 (ở đktc). Cô cạn dung dịch X (trong điều kiện không có không khí) được m gam muối khan. Giá trị của m là:
A. 35,6
B. 22,5
C. 64,4
D. 21,2