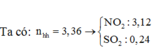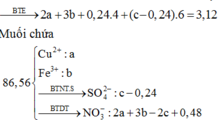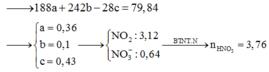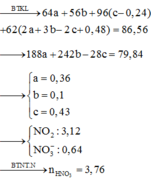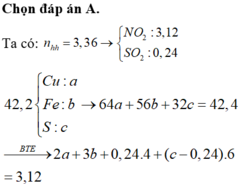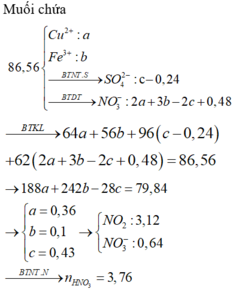Hòa tan hết 1,6 gam Cu trong dung dịch H²SO⁴ đặc 98%, đun nóng, thu được Vml khí SO² ở đktc. Tính V và khối lượng dung dịch H²SO⁴ 98% đã tham gia phản ứng

Những câu hỏi liên quan
hoà tan hết 1,6 gam Cu trong dung dịch axit sunfuric đặc(H2SO4 đặc 98 ),đun nóng thu được V ml khí SO2 (ở ĐKTC)
Tính V và khối lượng dung dịch H2SO4 đặc đã tham gia phản ứng
PTHH: Cu+ H2SO4 ---> CUO + SO2+ H2O
tính nCu=1,6:64=0,025 mol
Theo PTHH có nH2O=nCu=0,025 mol
Suy ra VSO2=0,025*22,4=0,56
Đúng 1
Bình luận (0)
PTHH: \(Cu+2H_2SO_4\rightarrow CuSO_4+SO_2+2H_2O\)
\(n_{Cu}=\dfrac{1,6}{64}=0,025\left(mol\right)\)
Theo PT ta có: \(n_{Cu}=n_{SO_2}=0,025\left(mol\right)\)
\(\Rightarrow V_{SO_2}=0,025.22,4=0,56\left(l\right)\)
Theo PT ta có: \(n_{H_2SO_4}=2.n_{Cu}=2.0,025=0,05\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=0,05.98=4,9\left(g\right)\)
Đúng 1
Bình luận (0)
PTHH: \(Cu+2H_2SO_4\rightarrow2H_2O+SO_2+CuSO_4\\ 0,025mol:0,05mol\rightarrow0,05mol:0,025mol\)
\(n_{Cu}=\dfrac{1,6}{64}=0,025\left(mol\right)\)
\(V_{SO_2}=0,025.22,4=0,56\left(l\right)\)
\(m_{H_2SO_4}=0,05.98=4,9\left(g\right)\)
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Cho 12 gam Mg tác dụng hết với dung dịch H 2 SO 4 98% (đặc) thì thu được 2,8 (đktc) lít khí X
(là sản phẩm khử duy nhất).
a. Tìm X.
b. Tìm khối lượng H 2 SO 4 98% đã dùng (biết lấy dư 50% so với lượng phản ứng). Tìm nồng độ
% của dung dịch mới.
a)
$n_{Mg} = \dfrac{12}{24} = 0,5(mol)$
$n_X = \dfrac{2,8}{22,4} = 0,125(mol)$
Gọi n là số electron nhận của X.
Bảo toàn electron : $2n_{Mg} = n.n_X$
$\Rightarrow n = \dfrac{0,5.2}{0,125} = 8$
Vậy X là $H_2S$
b) $n_{MgSO_4} = n_{Mg} = 0,5(mol)$
$n_{H_2SO_4} = n_{MgSO_4} + n_{H_2S} = 0,625(mol)$
$n_{H_2SO_4\ dư} = 0,625.50\% = 0,3125(mol)$
$n_{H_2SO_4\ đã\ dùng} = 0,625 + 0,3125 = 0,9375(mol)$
$m_{dd\ H_2SO_4} = \dfrac{0,9375.98}{98\%} = 93,75(gam)$
$m_{dd\ sau\ pư} = 12 + 93,75 - 0,125.34 = 101,5(gam)$
$C\%_{MgSO_4} = \dfrac{0,5.120}{101,5}.100\% = 59,11\%$
Đúng 4
Bình luận (0)
Hòa tan hết 15,2 gam Fe, Cu bằng dung dịch H,SO, đặc nóng sau phản ứng thu được dung dịch X. Cho X tác dụng với NaOH dư thu được kết tủa Y. Nung Y ngoài không khí đến khối lượng không đổi thu được 20,8 gam hỗn hợp Fe,O,, CuO. Tính % khối lượng mỗi kim loại trong hỗn hợp ban đầu?
\(2Fe+6H_2SO_4\to Fe_2(SO_4)_3+3SO_2\uparrow+6H_2O\\ Cu+2H_2SO_4\xrightarrow{t^o}CuSO_4+SO_2\uparrow+2H_2O\\ Fe_2(SO_4)_3+6NaOH\to 2Fe(OH)_3\downarrow+3Na_2SO_4\\ CuSO_4+2NaOH\to Cu(OH)_2\downarrow+Na_2SO_4\\ 2Fe(OH)_3\xrightarrow{t^o}Fe_2O_3+3H_2O\\ Cu(OH)_2\xrightarrow{t^o}CuO+H_2O\)
Đặt \(n_{Cu}=x(mol);n_{Fe}=y(mol)\Rightarrow 64x+56y=15,2(1)\)
Theo các PT: \(n_{Fe_2O_3}=0,5y(mol);n_{CuO}=x(mol)\)
\(\Rightarrow 80x+80y=20,8(2)\\ (1)(2)\Rightarrow x=0,08(mol);y=0,18(mol)\\ \Rightarrow \%_{Cu}=\dfrac{0,08.64}{15,2}.100\%=33,68\%\\ \Rightarrow \%_{Fe}=100\%-33,68\%=66,32\%\)
Đúng 2
Bình luận (0)
Hoà tan hết hỗn hợp gồm 1,12 gam Fe và 9,28 gam Fe x O y trong dung dịch H 2 SO 4 đặc, nóng thu được dung dịch X và 0,784 lít khí SO 2 (đktc). Để phản ứng hết với lượng muối sắt (III) trong dung dịch X cần dùng vừa hết 3,52 gam Cu. Xác định công thức của Fe x O y
THAM KHẢO
Quy đổi hỗn hợp Fe và FexOy thành Fe và O.
Số mol của Fe và O là x và y.
Xét các quá trình :
Fe, O H2SO4đ,n−−−−−−−−→H2SO4đ,n→ Fe3+, O2-, S+4(SO2) Cu−→Cu→ Fe2+, Cu2+
(Đối với PP bảo toàn e thì chỉ xét số oxi của nguyên tố ở đầu và cuối quá trình)
Quá trình nhường eQuá trình nhận e
Fe -> Fe2+ + 2e
x=--2x
Cu -> Cu2+ + 2e
0,055=0,11
O +2e -> O2-
y-.2y
S+6 +2e -> S+4
--0,07..0,035
Vì ne nhường =ne nhận <=> 2x+0,11=2y+0,07 (1)
Khối lượng Fe + O = khối lượng Fe + FexOy = 1,12 + 9,28=10,4
=> 56x + 16y =10,4 (2)
Giải hệ pt (1) và (2) => x=0,14; y=0,16
Ta có nFe (Fe ban đầu)=1,12/56=0,02
=> nFe(FexOy) = 0,12
=> xy=nFe(FexOy)/nO=0,12/0,16=3/4
=> oxit cần tìm là Fe3O4.
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 42,4 gam hỗn hợp gồm CuS, FeS2, Cu2S trong dung dịch HNO3 đun nóng. Sau phản ứng thu được 75,264 lít hỗn hợp khí (đktc) gồm NO2 và SO2 có tổng khối lượng là 158,88 gam. Dung dịch sau phản ứng chỉ chứa 86,56 gam các muối trung hòa. Số mol HNO3 đã tham gia phản ứng là: A. 3,76 B. 3,24 C. 3,82 D. 3,42
Đọc tiếp
Hòa tan hoàn toàn 42,4 gam hỗn hợp gồm CuS, FeS2, Cu2S trong dung dịch HNO3 đun nóng. Sau phản ứng thu được 75,264 lít hỗn hợp khí (đktc) gồm NO2 và SO2 có tổng khối lượng là 158,88 gam. Dung dịch sau phản ứng chỉ chứa 86,56 gam các muối trung hòa. Số mol HNO3 đã tham gia phản ứng là:
A. 3,76
B. 3,24
C. 3,82
D. 3,42
Hòa tan hoàn toàn 42,4 gam hỗn hợp gồm CuS, FeS2, Cu2S trong dung dịch HNO3 đun nóng. Sau phản ứng thu được 75,264 lít hỗn hợp khí (đktc) gồm NO2 và SO2 có tổng khối lượng là 158,88 gam. Dung dịch sau phản ứng chỉ chứa 86,56 gam các muối trung hòa. Số mol HNO3 đã tham gia phản ứng là: A. 3,76 B. 3,24 C. 3,82 D. 3,42
Đọc tiếp
Hòa tan hoàn toàn 42,4 gam hỗn hợp gồm CuS, FeS2, Cu2S trong dung dịch HNO3 đun nóng. Sau phản ứng thu được 75,264 lít hỗn hợp khí (đktc) gồm NO2 và SO2 có tổng khối lượng là 158,88 gam. Dung dịch sau phản ứng chỉ chứa 86,56 gam các muối trung hòa. Số mol HNO3 đã tham gia phản ứng là:
A. 3,76
B. 3,24
C. 3,82
D. 3,42
Hòa tan hoàn toàn 42,4 gam hỗn hợp gồm CuS, FeS2, Cu2S trong dung dịch HNO3 đun nóng. Sau phản ứng thu được 75,264 lít hỗn hợp khí (đktc) gồm NO2 và SO2 có tổng khối lượng là 158,88 gam. Dung dịch sau phản ứng chỉ chứa 86,56 gam các muối trung hòa. Số mol HNO3 đã tham gia phả ứng là: A. 3,76 B. 3,24 C. 3,82 D. 3,42
Đọc tiếp
Hòa tan hoàn toàn 42,4 gam hỗn hợp gồm CuS, FeS2, Cu2S trong dung dịch HNO3 đun nóng. Sau phản ứng thu được 75,264 lít hỗn hợp khí (đktc) gồm NO2 và SO2 có tổng khối lượng là 158,88 gam. Dung dịch sau phản ứng chỉ chứa 86,56 gam các muối trung hòa. Số mol HNO3 đã tham gia phả ứng là:
A. 3,76
B. 3,24
C. 3,82
D. 3,42
Câu 1: Cho 10,5 gam hỗn hợp hai kim loại Cu, Zn vào dung dịch H₂SO₄ loãng dư, người ta thu được 2,24 lít khí (đktc). Tính khối lượng chất rắn còn lại trong dung dịch sau phản ứng.
Câu 2: Hòa tan 12 gam hỗn hợp gồm Al, Ag vào dung dịch H₂SO₄ loãng, dư. Phản ứng kết thúc thu được 13,44 lít khí H₂ (đktc). Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp.
Câu 3: Hòa tan 25,8 gam hỗn hợp gồm bột Al và Al₂O₃ trong dung dịch HCl dư. Sau phản ứng người ta thu được 0,6 gam khí H₂. Tính khối lượng mu...
Đọc tiếp
Câu 1: Cho 10,5 gam hỗn hợp hai kim loại Cu, Zn vào dung dịch H₂SO₄ loãng dư, người ta thu được 2,24 lít khí (đktc). Tính khối lượng chất rắn còn lại trong dung dịch sau phản ứng. Câu 2: Hòa tan 12 gam hỗn hợp gồm Al, Ag vào dung dịch H₂SO₄ loãng, dư. Phản ứng kết thúc thu được 13,44 lít khí H₂ (đktc). Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp. Câu 3: Hòa tan 25,8 gam hỗn hợp gồm bột Al và Al₂O₃ trong dung dịch HCl dư. Sau phản ứng người ta thu được 0,6 gam khí H₂. Tính khối lượng muối AlCl₃ thu được.
Câu 2:
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\\ n_{Al}=\dfrac{2.0,6}{3}=0,4\left(mol\right)\\ \%m_{Al}=\dfrac{0,4.27}{12}.100\%=90\%\Rightarrow\%m_{Ag}=100\%-90\%=10\%\)
Đúng 3
Bình luận (0)
Câu 3:
\(n_{H_2}=\dfrac{0,6}{2}=0,3\left(mol\right)\\ 2Al+6HCl\rightarrow2AlCl_3+3H_2\\ Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\\ n_{Al}=\dfrac{2}{3}.0,3=0,2\left(mol\right)\\ n_{Al_2O_3}=\dfrac{25,8-0,2.27}{102}=0,2\left(mol\right)\\ n_{AlCl_3}=n_{Al}+2n_{Al_2O_3}=0,2+2.0,2=0,6\left(mol\right)\\ m_{AlCl_3}=133,5.0,6=80,1\left(g\right)\)
Đúng 2
Bình luận (0)
Câu 1:
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\ n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ n_{Zn}=n_{H_2}=0,1\left(mol\right)\\ m_{Zn}=0,1.65=6,5\left(g\right)\\ m_{rắn}=m_{hhCu,Zn}-m_{Zn}=10,5-6,5=4\left(g\right)\)
Đúng 2
Bình luận (0)
Nung a gam Cu trong V lít khí O2 đến phản ứng hoàn toàn thu được chất rắn A. Đun nóng A trong b gam dung dịch H2SO4 98%( lượng vừa đủ sau khi tan hết được dung dịch B chứa 19,2 gam muối và khí SO2. Cho khí SO2 hấp thụ hoàn toàn bởi 300ml dung dịch NaOH 0,1M thu được 2,3 gam hỗn hợp muối. Tính a,b và V(đktc).
giúp tôi nha cám ơn nhiều
nNaOH = 0,1.0,3 = 0,03 (mol)
Gọi \(\left\{{}\begin{matrix}n_{Na_2SO_3}=a\left(mol\right)\\n_{NaHSO_3}=b\left(mol\right)\end{matrix}\right.\)
=> 126a + 104b = 2,3
Bảo toàn Na: 2a + b = 0,03
=> a = 0,01 (mol); b = 0,01 (mol)
Bảo toàn S: \(n_{SO_2}=0,02\left(mol\right)\)
\(n_{CuSO_4}=\dfrac{19,2}{160}=0,12\left(mol\right)\)
Bảo toàn Cu: nCu = 0,12 (mol)
=> a = 0,12.64 = 7,68 (g)
Bảo toàn S: \(n_{H_2SO_4}=n_{CuSO_4}+n_{SO_2}=0,12+0,02=0,14\left(mol\right)\)
=> \(m_{H_2SO_4}=0,14.98=13,72\left(g\right)\)
=> \(b=m_{dd.H_2SO_4}=\dfrac{13,72.100}{98}=14\left(g\right)\)
Bảo toàn H: \(n_{H_2O}=n_{H_2SO_4}=0,14\left(mol\right)\)
BTKL: \(m_{Cu}+m_{O_2}+m_{H_2SO_4}=m_{CuSO_4}+m_{SO_2}+m_{H_2O}\)
=> mO2 = 19,2 + 0,02.64 + 0,14.18 - 7,68 - 13,72 = 1,6 (g)
=> \(n_{O_2}=\dfrac{1,6}{32}=0,05\left(mol\right)\)
=> \(V_{O_2}=0,05.22,4=1,12\left(l\right)\)
Đúng 3
Bình luận (0)
Hòa tan hết 17,92 gam hỗn hợp X gồm Fe3O4, FeO, Fe, CuO, Cu, Al và Al2O3 (trong đó Oxi chiếm 25,446% về khối lượng) vào dung dịch HNO3 loãng dư, kết thúc các phản ứng thu được dung dịch Y và 1,736 lít (đktc) hỗn hợp khí Z gồm N2 và N2O có tỷ khối hơi so với H2 là 15,29. Cho dung dịch NaOH tới dư vào Y rồi đun nóng, không có khí thoát ra. Số mol HNO3 đã phản ứng với X có giá trị gần nhất với A. 1,2. B. 1,3. C. 1,4. D. 1,5.
Đọc tiếp
Hòa tan hết 17,92 gam hỗn hợp X gồm Fe3O4, FeO, Fe, CuO, Cu, Al và Al2O3 (trong đó Oxi chiếm 25,446% về khối lượng) vào dung dịch HNO3 loãng dư, kết thúc các phản ứng thu được dung dịch Y và 1,736 lít (đktc) hỗn hợp khí Z gồm N2 và N2O có tỷ khối hơi so với H2 là 15,29. Cho dung dịch NaOH tới dư vào Y rồi đun nóng, không có khí thoát ra. Số mol HNO3 đã phản ứng với X có giá trị gần nhất với
A. 1,2.
B. 1,3.
C. 1,4.
D. 1,5.