Ngâm một lá đồng vào 340 gam dung dịch AgNO3 10%. Sau khi tất cả bạc bị đẩy ra khỏi dung dịch AgNO3 và bám hết vào lá đồng, thì khối lượng lá đồng tăng lên 38%. Xác định khối lượng lá đồng ban đầu.

Những câu hỏi liên quan
Ngâm một lá đồng vào 340 gam dung dịch AgNO3 10%. Sau khi tất cả bạc bị đẩy ra khỏi dung dịch AgNO3 và bám hết vào lá đồng, thì khối lượng lá đồng tăng lên 38%. Xác định khối lượng lá đồng ban đầu.
Ngâm 1 lá Sắt vào 320 gam dung dịch CuSO4 10%. Sau khi tất cả đồng đẩy ra khỏi dd CuSO4 và bám hết vào miếng sắt tăng lên 8%. Xác định khối lượng miếng sắt ban đầu
Ta có: mCuSO4=(320x10):100=32g=>nCuSO4=32:160=0...
ptpu: Fe + CuSO4 => FeSO4 + Cu
0,2 0,2 mol 0,2 mol
Độ tăng khối lượng của miếng sắt là: 0,2x(64-56)=1,6g
Theo đề: độ tăng của miếng sắt là 8% nên
1,6g -------> 8%
20g <--------- 100%
Vậy khối lượng miếng sắt ban đầu là 20g
BẠN THAM KHẢO
Đúng 0
Bình luận (1)
Cho một lá sắt vào 160 gam dung dịch CuSO 4 10%. Sau khi Cu bị đẩy hết ra khỏi dung dịch CuSO 4 và bám hết vào lá sắt, thì khối lượng lá sắt tăng lên 4%. Xác định khối lượng lá sắt ban đầu.
Số mol CuSO 4 = 10/100 = 0,1 mol
Phương trình hóa học của phản ứng:
Fe + CuSO 4 → FeSO 4 + Cu
Khối lượng Fe phản ứng: 0,1 . 56 =5,6(gam)
Khối lượng Cu sinh ra: 0,1 . 64 = 6,4 (gam)
Gọi x là khối lượng lá sắt ban đầu
Khối lượng lá sắt khi nhúng vào dung dịch CuSO 4 tăng lên là: 4x/100 = 0,04x (gam)
Khối lượng lá sắt tăng lên = m Cu sinh ra - m Fe phản ứng = 0,04x = 6,4 -5,6 = 0,8
=> x= 20 gam
Đúng 0
Bình luận (0)
Ngâm một lá kim loại Kẽm vào 400ml dung dịch AgNO, 0,1M. Sau khi tất cả Bạc bị đẩy ra và bám hết vào lá Kẽm thì khối lượng là Kẽm tăng lên 4% so với lúc đầu. Xác định khối lượng lá Kẽm lúc đầu.
Xem chi tiết
\(400ml=0,4l\)
\(n_{AgNO_3}=0,4.0,1=0,04mol\)
\(Zn+2AgNO_3\rightarrow Zn\left(NO_3\right)_2+2Ag\)
\(\rightarrow n_{Zn}=0,02mol\) và \(n_{Ag}=0,04mol\)
\(\rightarrow m_{rm\text{kim loại tăng}}=0,04.108-65.0,02=3,02g\)
\(\rightarrow m_{Zn\left(bđ\right)}=\frac{3,02}{4\%}=75,5g\)
Ngâm một lá đồng trong 20ml dung dịch bạc nitrat cho đến khi đồng không thể tan thêm được nữa. Lấy lá đồng ra, rửa nhẹ, làm khô và cân thì khối lượng lá đồng tăng thêm 1,52g. Hãy xác định nồng độ mol của dung dịch bạc nitrat đã dùng (giả thiết toàn bộ bạc giải phóng ra bám hết vào lá đồng). A. 0,75 M B. 0,5 M C. 1 M D. 0,25 M
Đọc tiếp
Ngâm một lá đồng trong 20ml dung dịch bạc nitrat cho đến khi đồng không thể tan thêm được nữa. Lấy lá đồng ra, rửa nhẹ, làm khô và cân thì khối lượng lá đồng tăng thêm 1,52g. Hãy xác định nồng độ mol của dung dịch bạc nitrat đã dùng (giả thiết toàn bộ bạc giải phóng ra bám hết vào lá đồng).
A. 0,75 M
B. 0,5 M
C. 1 M
D. 0,25 M
Cu → 2Ag
1 2 → mtang = 2.108-64 = 152g
x 2x → mtang = =1,52g
⇒ x = 1,52/152 = 0,01 mol
⇒ n A g N O 3 = n A g = 2x = 0,02 mol
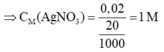
⇒ Chọn C.
Đúng 0
Bình luận (0)
Ngâm 1 lá đồng vào 300g dung dịch AgNO3 5% .a) tính kg đồng và khối lượng của bạc bị đẩy ra.b) tính C% của dung dịch sau phản ứng
PTHH: \(Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag\)
a) Ta có: \(n_{AgNO_3}=\dfrac{300\cdot5\%}{170}=\dfrac{3}{34}\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Ag}=\dfrac{3}{34}\left(mol\right)\\n_{Cu}=\dfrac{3}{68}\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Ag}=\dfrac{3}{34}\cdot108\approx9,53\left(g\right)\\m_{Cu}=\dfrac{3}{68}\cdot64\approx2,82\left(g\right)\end{matrix}\right.\)
b) Coi như p/ứ vừa đủ
Theo PTHH: \(n_{Cu\left(NO_3\right)_2}=n_{Cu}=\dfrac{3}{68}\left(mol\right)\) \(\Rightarrow m_{Cu\left(NO_3\right)_2}=\dfrac{3}{68}\cdot188\approx8,29\left(g\right)\)
Mặt khác: \(m_{dd\left(sau.p/ứ\right)}=m_{Cu}+m_{ddAgNO_3}-m_{Ag}=293,29\left(g\right)\)
\(\Rightarrow C\%_{Cu\left(NO_3\right)_2}=\dfrac{8,29}{293,29}\cdot100\%\approx3,46\%\)
Đúng 3
Bình luận (1)
Ngâm 1 lá đồng vào 300g dung dịch AgNO3 5% .a) tính kg đồng và khối lượng của bạc bị đẩy ra.b) tính C% của dung dịch sau phản ứng
\(n_{AgNO_3}=\dfrac{300.5\%}{170}=\dfrac{3}{34}\left(mol\right)\)
\(Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag\)
Ta có : \(n_{Cu}=\dfrac{1}{2}n_{AgNO_3}=\dfrac{3}{68}\left(mol\right)\)
=> \(m_{Cu}=\dfrac{3}{68}.64=2,82\left(g\right)\)
\(n_{Ag}=n_{AgNO_3}=\dfrac{3}{34}\left(mol\right)\)
=>\(m_{Ag}=\dfrac{3}{34}.108=9,53\left(g\right)\)
\(m_{ddsaupu}=2,82+300-9,53=293,29\left(g\right)\)
Ta có : \(n_{Cu\left(NO_3\right)_2}=\dfrac{1}{2}n_{AgNO_3}=\dfrac{3}{68}\left(mol\right)\)
\(\Rightarrow C\%_{Cu\left(NO_3\right)_2}=\dfrac{\dfrac{3}{68}.188}{293,29}.100=2,83\%\)
Đúng 1
Bình luận (0)
Cho một lá đồng có khối lượng 5g vào 125g dung dịch AgNO3 4%. Sau một thời gian khi lấy lá đồng ra thì khối lượng AgNO3 trong dung dịch giảm 17%. Xác định khối lượng kim loại Cu sau phản ứng.
Ngâm một lá sắt trong 100ml dung dịch đồng nitrat cho đến khi sắt không thể tan thêm được nữa. Lấy lá sắt ra, rửa nhẹ, làm khô và cân thì khối lượng lá sắt tăng thêm 1,6g. Hãy xác định nồng độ mol của dung dịch đồng nitrat đã dùng (giả thiết toàn bộ đồng giải phóng ra bám hết vào lá sắt). A. 1 M B. 0,5 M C. 1,5 M D. 2 M
Đọc tiếp
Ngâm một lá sắt trong 100ml dung dịch đồng nitrat cho đến khi sắt không thể tan thêm được nữa. Lấy lá sắt ra, rửa nhẹ, làm khô và cân thì khối lượng lá sắt tăng thêm 1,6g. Hãy xác định nồng độ mol của dung dịch đồng nitrat đã dùng (giả thiết toàn bộ đồng giải phóng ra bám hết vào lá sắt).
A. 1 M
B. 0,5 M
C. 1,5 M
D. 2 M















