Cho 15,6g hỗn hợp gồm bột Fe và bột Cu tác dụng vừa đủ với 100g
dung dịch HCl, thu được 4,48 lít khí H2 (đktc).
a. Viết phương trình hóa học của phản ứng xảy ra ?
b. Tính khối lượng các chất rắn ban đầu ?
Câu 3:(3,0 điểm)Cho 12 gam hỗn hợp gồm kim loại Cu và Fe tác dụng vừa đủ với dung dịch HCl 10% thu được dung dịch A, chất rắn B và 3,36 lít khí C (đktc).
a) Viết phương trình hóa học xảy ra.
b) Tính % khối lượng mỗi kim loại trong hỗn hợp ban đầu
c) Tính khối lượng dung dịch HCl đã tham gia phản ứng.
d) Tính nồng độ % của dung dịch A tạo thành sau phản ứng.
(Cho Cu = 64, Fe = 56, H = 1, O = 16, Cl = 35,5)
a) Fe + 2HCl --> FeCl2 + H2
b) \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
_____0,15<-0,3<----0,15<---0,15
\(\left\{{}\begin{matrix}\%Fe=\dfrac{0,15.56}{12}.100\%=70\%\%\\\%Cu=100\%-70\%=30\%\end{matrix}\right.\)
c) mHCl = 0,3.36,5 = 10,95 (g)
=> \(m_{dd}=\dfrac{10,95.100}{10}=109,5\left(g\right)\)
d) mdd = 12 + 109,5 - 0,15.2 = 121,2 (g)
\(C\%\left(FeCl_2\right)=\dfrac{0,15.127}{121,2}.100\%=15,718\%\)
a: \(Cu+2HCl->CuCl_2+H_2\)
\(Fe+2HCl->FeCl_2+H_2\)
Cho 12 gam hỗn hợp X gồm Fe và FeO tác dụng vừa đủ với dung dịch HCl. Sau phản ứng thu được 3,36 lít khí H2 (đktc).
a. Viết các phương trình phản ứng xảy ra.
b. Tính khối lượng của mỗi chất trong hỗn hợp X và thể tích dung dịch HCl 2M đã dùng.
c. Cho lượng hỗn hợp X nói trên vào dung dịch CuSO4 dư thì sau phản ứng thu được bao nhiêu gam chất rắn.
a)
$Fe + 2HCl \to FeCl_2 + H_2$
$FeO + 2HCl \to FeCl_2 + H_2O$
b)
Theo PTHH : $n_{Fe} = n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)$
$m_{Fe} = 0,15.56 = 8,4(gam)$
$m_{FeO} = 12 - 8,4 = 3,6(gam)$
$n_{FeO} =0,05(mol)$
Theo PTHH : $n_{HCl} = 2n_{Fe} + 2n_{FeO} = 0,4(mol)$
$V_{dd\ HCl} = \dfrac{0,4}{2} = 0,2(lít)$
c) $Fe + CuSO_4 \to FeSO_4 + Cu$
$n_{Cu} = n_{Fe} = 0,15(mol) \Rightarrow m_{chất\ rắn} = m_{FeO} + m_{Cu}$
$= 3,6 + 0,15.64 = 13,2(gam)$
Cho 4,4 g hỗn hợp gồm Mg và MgO tác dụng vừa đủ với dung dịch HCl 7,3% thu được 2,24 lít khí (đkc) A) viết các phương trình phản ứng xảy ra b) tính khối lượng mỗi chất trong hỗn hợp ban đầu C) tính khối lượng dung dịch HCl phản ứng D) tính c% của dung dịch muối thu được sau phản ứng Ghi rõ ra để mình biết các câu để mình ghi nha
Cho hỗn hợp gồm Fe, Mg có khối lượng 8g tác dụng hết với dung dịch HCl thu được 4,48 lít khí H2 (đktc).
a) Viết phương trình hóa học của Fe và Mg với dung dịch HCl.
b) Tính tỉ lệ theo số mol của Fe và của Mg trong hỗn hợp ban đầu (Fe=56, Mg=24)
Bài 3. Cho 17,6 gam hỗn hợp Fe và Cu phản ứng với lượng dư dung dịch HCl loãng, sau phản ứng thu được 4,48 lít khí (đktc) a. Tính %m mỗi chất trong hỗn hợp ban đầu. b. Dẫn khí H2 thu được ở trên đi qua bột Fe2O3 nung nóng, tính khối lượng Fe tối đa có thể thu được
a) Ta có: nH2=4,48/22,4=0,2(mol)
PTHH: Fe +2 HCl -> FeCl2 + H2
0,2________0,4______0,2__0,2(mol)
mFe=0,2.56=11,2(g)
=> %mFe= (11,2/17,6).100=63,636%
=> %mCu= 36,364%
b) Fe2O3 + 3 H2 -to-> 2 Fe + 3 H2O
Ta có: nH2=0,2(mol) => nFe=2/3. 0,2= 2/15(mol)
=> mFe= 2/15 . 56=7,467(g)
Số moll của khí hidro ở dktc
nH2 = \(\dfrac{V_{H2}}{22,4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Pt : Fe + 2HCl → FeCl2 + H2\(|\)
1 2 1 1
0,2 0,2
a) Số mol của sắt
nFe = \(\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
Khối lượng của sắt
mFe = nFe . MFe
= 0,2. 56
= 11,2 (g)
Khối lượng của đồng
mCu = 17,6 - 11,2
= 6,4 (g)
0/0Fe = \(\dfrac{m_{Fe}.100}{m_{hh}}=\dfrac{11,2.100}{17,6}=63,64\)0/0
0/0Cu = \(\dfrac{m_C.100}{m_{hh}}=\dfrac{6,4.100}{17,6}=36,36\)0/0
b) 3H2 + Fe2O3 → (to) 2Fe + 3H2O\(|\)
3 1 2 3
0,2 0,13
Số mol của sắt
nFe = \(\dfrac{0,2.2}{3}=0,13\left(mol\right)\)
Khối lượng của sắt
mFe = nFe . MFe
= 0,13 . 56
= 7,28 (g)
Chúc bạn học tốt
cho 11 gam hỗn hợp gồm al và fe tác dụng vừa đủ với đ hcl tạo 8,96 lít khí h2 thoát thành ra ở đktc. Viết pthh và tính:
a)tính % về khối lượng các chất ban đầu
b)dẫn toàn bộ khí trên qua 16 gam bột cuo đun nóng đến phản ứng kết thúc. tính cu thu được
a) PTHH: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
a_____________________\(\dfrac{3}{2}\)a (mol)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
b____________________b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}27a+56b=11\\\dfrac{3}{2}a+b=\dfrac{8,96}{22,4}=0,4\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2\cdot27}{11}\cdot100\%\approx49,09\%\\\%m_{Fe}=50,91\%\end{matrix}\right.\)
b) PTHH: \(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\\n_{H_2}=\dfrac{3}{2}a+b=0,4\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) H2 còn dư, tính theo CuO
\(\Rightarrow n_{Cu}=0,2\left(mol\right)\) \(\Rightarrow m_{Cu}=0,2\cdot64=12,8\left(g\right)\)
Gọi n Al = a ( mol ) , n Fe = b ( mol )
Có: n H2 = 0,4 ( mol )
PTHH
2AL + 6HCL ===> 2ALCL3 + 3H2
a--------------------------------------a
Fe + 2HCl ====> FeCL2 + H2
b------------------------------------b
Ta có hpt:
\(\left\{{}\begin{matrix}27a+56b=11\\1,5a+b=0,4\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
=> m AL = 5,4 ( g ) ; m Fe = 5,6 ( g )
b) Có : n CuO = 0,2 ( mol )
PTHH:
CuO + H2 ====> Cu +H2O
0,2----0,2-----------0,2
theo pthh: n Cu = 0,2 ( mol ) => m Cu = 12,8 ( g )
\(n_{H2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Pt : \(2Al+6HCl\rightarrow2AlCl_3+3H_2|\)
2 6 2 3
a 1,5a
\(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
b 1b
a) Gọi a là số mol của Al
b là số mol của Fe
\(m_{Al}+m_{Fe}=11\left(g\right)\)
⇒ \(n_{Al}.M_{Al}+n_{Fe}.M_{Fe}=11g\)
⇒ 27a + 56b = 11g (1)
Theo phương trình : 1,5a +1b = 0,4(2)
Từ (1),(2), ta có hệ phương trình :
27a + 56b = 11
1,5a + 1b = 0,4
⇒ \(\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
\(m_{Al}=0,2.27=5,4\left(g\right)\)
\(m_{Fe}=0,1.56=5,6\left(g\right)\)
0/0Al = \(\dfrac{5,4.100}{11}=49,09\)0/0
0/0Fe = \(\dfrac{5,6.100}{11}=50,91\)0/0
b) Pt : \(H_2+CuO\rightarrow\left(t_o\right)Cu+H_2O|\)
1 1 1 1
0,4 0,4
\(n_{Cu}=\dfrac{0,4.1}{1}=0,4\left(mol\right)\)
⇒ \(m_{Cu}=0,4.64=25,6\left(g\right)\)
Chúc bạn học tốt
Cho 35 g hỗn hợp hai kim loại sắt và đồng tác dụng với dung dịch HCl dư. Sau khi phản ứng xong thu được chất rắn A và 8,96 lít khí (ở đktc).
a)Viết phương trình phản ứng hóa học xảy ra.
b)Tính thành phần trăm theo khối lượng của hỗn hợp ban đầu.
a, \(Fe+2HCl\rightarrow FeCl_2+H_2\)
b, \(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Theo PT: \(n_{Fe}=n_{H_2}=0,4\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{0,4.56}{35}.100\%=64\%\\\%m_{Cu}=36\%\end{matrix}\right.\)
Cho hỗn hợp gồm Fe và FeS tác dụng với dung dịch HCl (dư), thu được 2,464 lít hỗn hợp khí (đktc). Cho hỗn hợp khí này đi qua dung dịch Pb(NO3)2 (dư), thu được 23,9g kết tủa màu đen.
a) Viết các phương trình hóa học của phản ứng đã xảy ra.
b) Hỗn hợp khí thu được gồm những khí nào? Thể tích mỗi khí là bao nhiêu (đktc)?
c) Tính khối lượng của Fe và FeS có trong hỗn hợp ban đầu?
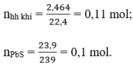
a) Phương trình hóa học của phản ứng:
Fe + 2HCl → FeCl2 + H2 (1)
FeS + 2HCl → FeCl2 + H2S (2)
H2S + Pb(NO3)2 → PbS + 2HNO3 (3)
b) Hỗn hợp khí thu được là H2 và H2S
Theo pt (3) ⇒ nH2S = nPbS = 0,1 mol
⇒ nH2 = nhh khí - nH2S = 0,11 – 0,1 = 0,01 mol
VH2 = 0,01 x 22,4 = 0,224l.
VH2S = 0,1 x 22,4 = 2,24l.
c) Theo PT (2) ⇒ nFeS = nH2S = 0,1 mol
⇒ mFeS = 0,1 × 88 = 8,8g.
Theo PT (1) nFe = nH2 = 0,01 mol ⇒ mFe = 56 × 0,01 = 0,56g.
Cho 28,4 gam hỗn hợp bột mịn X (gồm Al, Cr, Fe, Cu và Ag) vào dung dịch H 2 S O 4 loãng, nóng. Sau khi các phản ứng xảy ra hoàn toàn có 17,2 gam chất rắn tách ra, đồng thời thu được 4,48 lít khí (đktc). Độ tăng khối lượng của dung dịch sau phản ứng so với khối lượng dung dịch H2SO4 ban đầu là
A. 15,2 gam
B. 10,8 gam
C. 10 gam
D. 11,2 gam