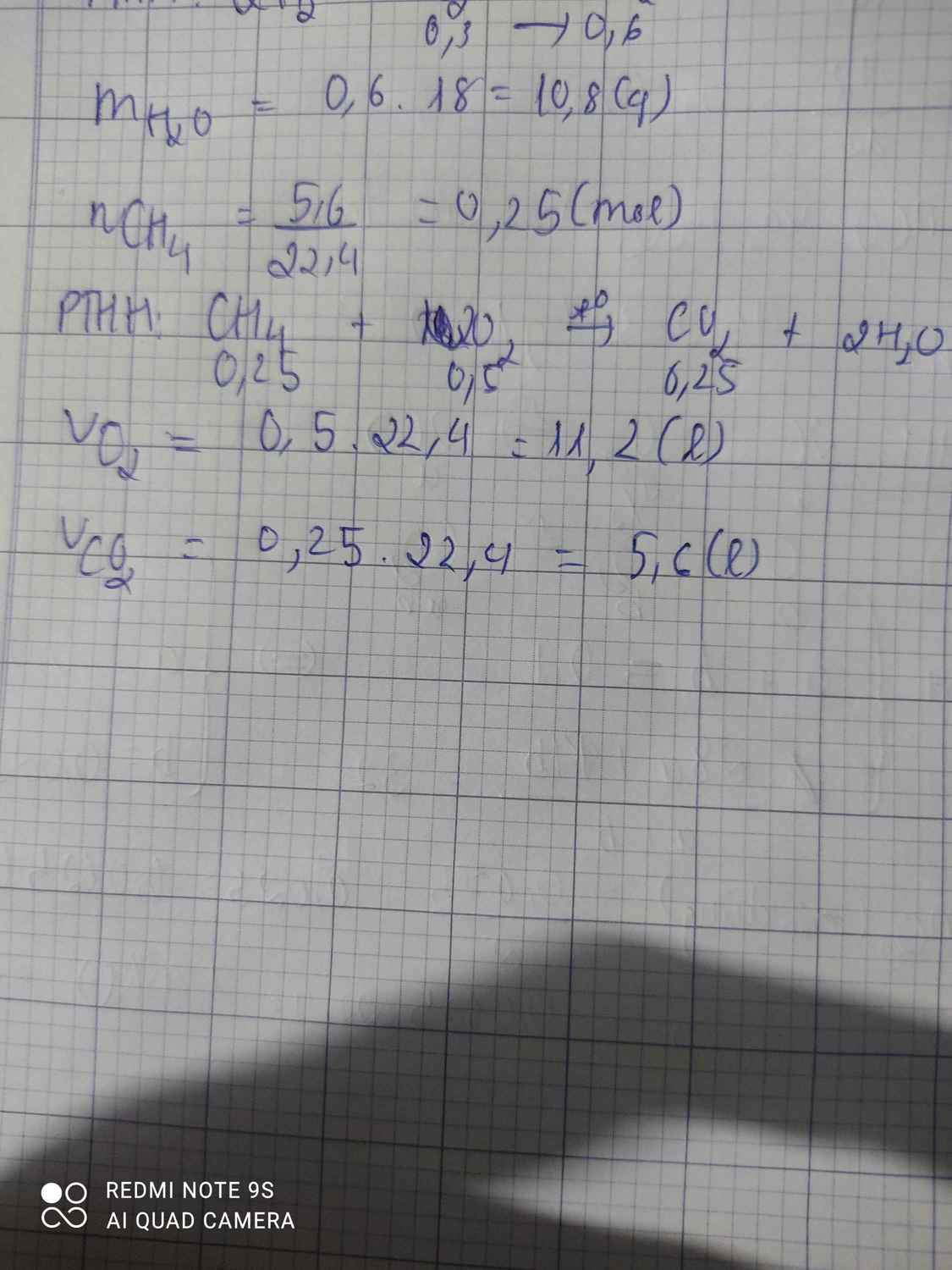Hãy tìm thể tích khí oxi ( ở đktc) cần dùng đốt cháy hoàn toàn 24 gam cacbon. ( cho biết : C=12, O=16) 💞

Những câu hỏi liên quan
Hãy tìm thể tích khí oxi(đktc) cần dùng để đốt cháy hoàn toàn 24 g cacbon
tham khảo tại đây nka bn: https://hoc24.vn/cau-hoi/tinh-the-tich-khi-oxi-o-dktc-can-dung-de-dot-chay-het-24g-than-cacbon.1857970648802
Đúng 1
Bình luận (0)
C + \(O_2\) ➙ \(CO_2\)
Số mol của Cacbon là: \(n_C\) = \(\dfrac{24}{12}\) = 2 (mol)
Số mol của Oxi là: \(n_{O_2}\) = \(n_C\) = 2 (mol)
Thể tích Oxi cần dùng là: V = \(n_{O_2}\) x 22,4 = 44,8 (l)
Đúng 0
Bình luận (0)
\(TH1:n_C=\dfrac{m}{M}=\dfrac{24}{12}=2\left(mol\right)\\ PTHH:O_2+C\underrightarrow{t^o}CO_2\\ Theo.PTHH\Rightarrow n_{O_2}=n_C=2\left(mol\right)\\ V_{O_2\left(dktc\right)}=n.22,4=2.22,4=44,8\left(l\right)\)
\(TH2:n_C=\dfrac{m}{M}=\dfrac{24}{12}=2\left(mol\right)\\ PTHH:O_2+2C\underrightarrow{t^o}2CO\\ Theo.PTHH:n_{O_2}=\dfrac{1}{2}n_C=\dfrac{1}{2}.2=1\left(mol\right)\\ V_{O_2\left(dktc\right)}=n.22,4=1.22,4=22,4\left(l\right)\)
Đúng 0
Bình luận (4)
Đốt cháy hoàn toàn 5,6 lít khí metan hãy tính Thể tích khí oxi cần dùng và thể tích khí cacbon tạo thành biết các thể tích đó ở đktc ( biết C=12, H=1 S=32)
\(n_{CH_4}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,25-->0,5-------->0,25
=> \(V_{O_2}=0,5.22,4=11,2\left(l\right)\)
\(V_{CO_2}=0,25.22,4=5,6\left(l\right)\)
Đúng 4
Bình luận (1)
thể tích không khí tối thiểu (ở đktc, oxi chiếm 80% thể tích không khí) cần dùng để đốt cháy hoàn toàn 24 gam cacbon (tạo khí cacbonic) là bao nhiêu?
đốt cháy hoàn toàn 48g cacbon gam ko khí theo phản ứng hóa học sau .Lập phương trình hóa học .tính khối lượng của cacbon đioxit(CO2) tạo thành.tính thể tích khí oxi dùng ở đktc. khí CO2 nặng hay nhẹ hơn ko khí bằng bao nhiêu lân(cho biết C=12,O=16)
Xem chi tiết
nC= 48/12=4(mol)
C+ O2 -to-> CO2
nCO2=nO2=nC=4(mol)
=> mCO2=4.44=176(g)
V(O2,đktc)=4.22,4=89,6(l)
V(CO2/kk)= M(CO2)/29= 44/29=1,517(lần)
=> CO2 nặng hơn không khí 1,517 lần.
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 0.3 mol khí metan ( CH4 ) trong không khí sinh ra 13.2 gam khí cacbon dioxit và 10.8 gam nước. Hãy tính thể tích không khí cần dùng ở đktc? ( Biết rằng khí metan cháy trong không khí là tác dụng với khí oxi. Và oxi chiếm 1/5 thể tích không khí). Giúp mình với:
\(m_{CH_4}=0,3.16=4,8(g)\)
Bảo toàn KL: \(m_{CH_4}+m_{O_2}=m_{CO_2}+m_{H_2O}\)
\(\Rightarrow m_{O_2}=10,8+13,2-4,8=19,2(g)\\ \Rightarrow V_{O_2}=\dfrac{19,2}{32}.22,4=13,44(l)\\ \Rightarrow V_{kk}=13,44.5=67,2(l)\)
Đúng 1
Bình luận (0)
đốt cháy hoàn toàn 5,6 lít khí axetilen a) tính thể tích khí CO2 tạo ra ở (đktc) b) tính thể tích không khí cần dùng cho phản ứng trên. Biết oxi chiếm 20% thể tích của không khí (các khí do ở đktc). cho C=12 H=1 O=16
Xem chi tiết
\(2C_2H_2+5O_2\rightarrow\left(t^o\right)4CO_2+2H_2O\\ n_{C_2H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\\ n_{CO_2}=2.0,25=0,5\left(mol\right)\\ a,V_{CO_2\left(đktc\right)}=0,5.22,4=11,2\left(l\right)\\ b,n_{O_2}=\dfrac{5}{2}.0,25=0,625\left(mol\right)\\ V_{O_2\left(đktc\right)}=0,625.22,4=14\left(l\right)\\ V_{kk\left(đkct\right)}=\dfrac{100}{20}.14=70\left(lít\right)\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 12 gam hỗn hợp bột lưu huỳnh và cacbon trong không khí thu được 28 gam hỗn hợp khí lưu huỳnh đioxit và cacbon đioxit. Thể tích oxi (ở đktc) cần dùng trong phản ứng trên là .
Gọi nC = a (mol); nS = b (mol)
12a + 32b = 12 (1)
PTHH:
C + O2 -> (t°) CO2
a ---> a ---> a
S + O2 -> (t°) SO2
b ---> b ---> b
44a + 64b = 28 (2)
Từ (1)(2) => a = 0,2 (mol); b = 0,3 (mol)
nO2 = 0,2 + 0,3 = 0,5 (mol)
VO2 = 0,5 . 22,4 = 11,2 (l)
Đúng 4
Bình luận (0)
Câu: biết rằng Oxi chiếm 20% thể tích không khí. Đốt cháy hoàn toàn 6,4 gam Cu bằng khí oxi
a) tính thể tích không khí cần dùng (đktc)
b) tính số gam KClO3 cần dùng để điều chế lượng oxi trên ( Cho Cu=64, K=39, Cl=35,5. O=16)
a.\(n_{Cu}=\dfrac{6,4}{64}=0,1mol\)
\(2Cu+O_2\rightarrow\left(t^o\right)2CuO\)
0,1 0,05 ( mol )
\(V_{kk}=\left(0,05.22,4\right).5=5,6l\)
b.\(2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\)
1/30 0,05 ( mol )
\(m_{KClO_3}=\dfrac{1}{30}.122,5=4,08g\)
Đúng 2
Bình luận (0)
Đốt cháy hòan tòan một thể tích khí thiên nhiên gồm metan,etan,propan bằng oxi không khí (trong không khí, oxi chiếm 20% thế tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thế tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn tòan lượng khí thiên nhiên trên 1à (Cho H1; C12; O16) A. 70,0 lít. B. 7,84 lít. C. 84,0 lít. D. 56,0 lít.
Đọc tiếp
Đốt cháy hòan tòan một thể tích khí thiên nhiên gồm metan,etan,propan bằng oxi không khí (trong không khí, oxi chiếm 20% thế tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thế tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn tòan lượng khí thiên nhiên trên 1à (Cho H=1; C=12; O=16)
A. 70,0 lít.
B. 7,84 lít.
C. 84,0 lít.
D. 56,0 lít.
Đáp án A
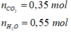
Áp dụng bảo toàn nguyên tố oxi ta có:

Đúng 0
Bình luận (0)