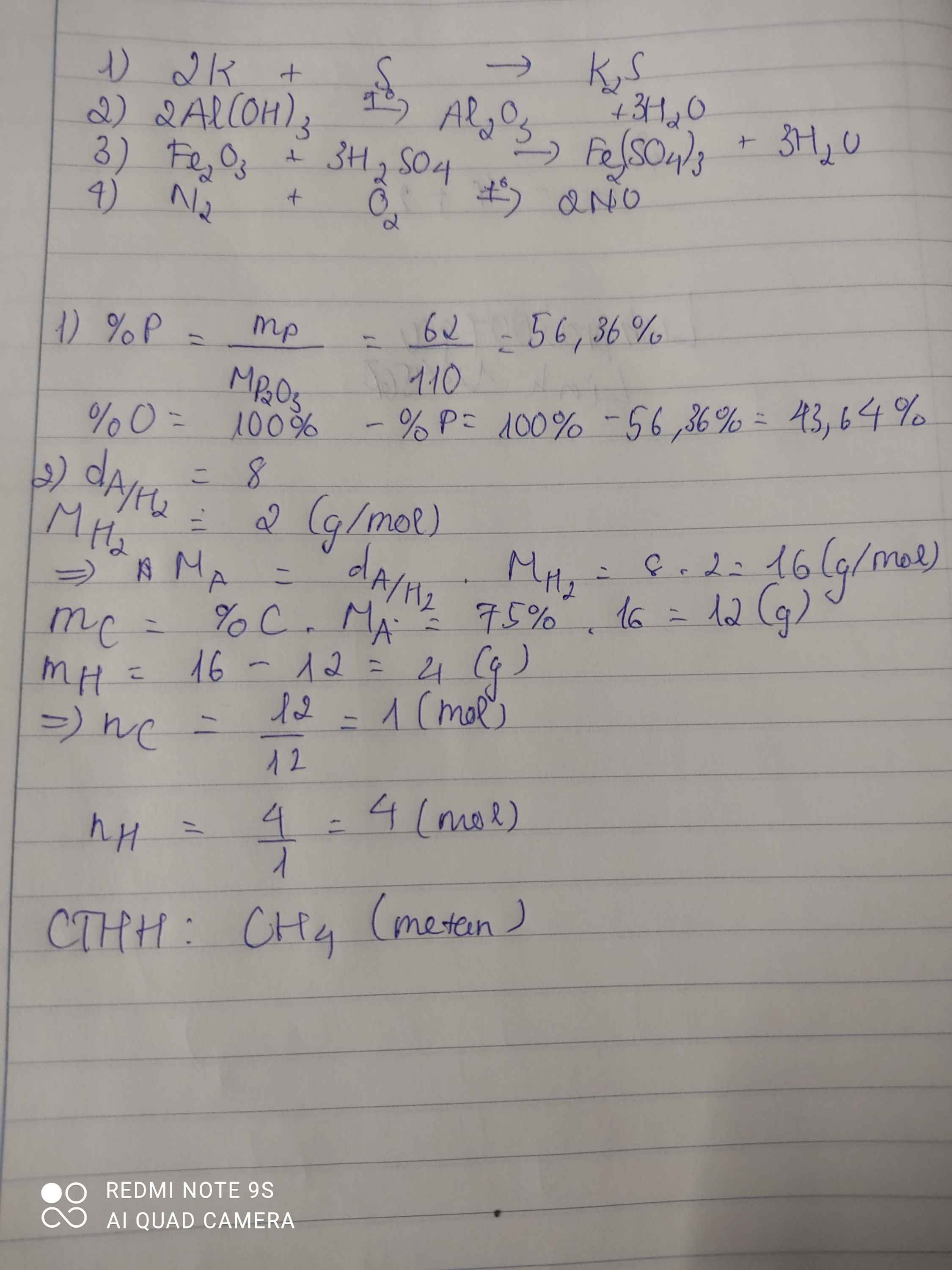Một hợp chất khí, thành phần có 75%C, còn lại là H và có khối lượng phân tử bằng 1/2 khối lượng phân tử của khí oxy. Xác định CTHH của hợp chất khí

Những câu hỏi liên quan
Câu 1: Hãy tính:- Số mol CO2 có trong 11g khí CO2 (đktc)- Thể tích (đktc) của 9.1023 phân tử khí H2Câu 2: Hãy cho biết 67,2 lít khí oxi (đktc)- Có bao nhiêu mol oxi?- Có bao nhiêu phân tử khí oxi?- Có khối lượng bao nhiêu gam?- Cần phải lấy bao nhiêu gam khí N2 để có số phan tử gấp 4 lần số phân tử có trong 3.2 gkhí oxi.Câu 3: Một hỗn hợp gồm 1,5 mol khí O2; 2,5 mol khí N2; 1,2.1023 phân tử H2 và 6,4 g khó SO2.- Tính thể tích của hỗn hợp khí đó ở đktc.- Tính khối lượng của hỗn hợp khí trên.Câu 1...
Đọc tiếp
Câu 1: Hãy tính:
- Số mol CO2 có trong 11g khí CO2 (đktc)
- Thể tích (đktc) của 9.1023 phân tử khí H2
Câu 2: Hãy cho biết 67,2 lít khí oxi (đktc)
- Có bao nhiêu mol oxi?
- Có bao nhiêu phân tử khí oxi?
- Có khối lượng bao nhiêu gam?
- Cần phải lấy bao nhiêu gam khí N2 để có số phan tử gấp 4 lần số phân tử có trong 3.2 g
khí oxi.
Câu 3: Một hỗn hợp gồm 1,5 mol khí O2; 2,5 mol khí N2; 1,2.1023 phân tử H2 và 6,4 g khó SO2.
- Tính thể tích của hỗn hợp khí đó ở đktc.
- Tính khối lượng của hỗn hợp khí trên.
Câu 1: Tính phần trăm khối lượng của các nguyên tố trong hợp chất: NaNO3; K2CO3 , Al(OH)3,
SO2, SO3, Fe2O3.
Câu 2: Xác định CTHH của hợp chất giữa nguyên tố X với O có %X = 43,67%. Biết X có hóa
trị V trong hợp chất với O. (ĐS: P2O5)
Câu 3: Hợp chất B có %Al = 15,79%; %S = 28,07%, còn lại là O. Biết khối lượng mol B là
342.Viết CTHH dưới dạng Alx(SO4)y .Xác định CTHH. (ĐS: Al2(SO4)3 )
Câu 4:Một hợp chất khí X có tỉ khối đối với hidro là 8,5. Hãy xác định công thức hóa học của
X biết hợp chất khí có thành phần theo khối lượng là 82,35% N và 17,65% H.(ĐS: NH3)
Câu 5: Một hợp chất X của S và O có tỉ khối đối với không khí là 2,207.
a. Tính MX (ĐS: 64 đvC)
b. Tìm công thức hóa học của hợp chất X biết nguyên tố S chiếm 50% khối lượng, còn lại
là O. (ĐS: SO2)
Câu1) nCO2 =m/M=11/44=0,25(mol)
nH2= 9.1023/6.1023=1,5(mol)
VH2 =n.22,4=1,5.22,4=33,6(l)
Câu 1 : Hợp chất A có thành phần % về khối lượng là : 85,7% C, còn lại là H. Hãy xác định CTHH của A, biết tỉ khối của khí A so với hidro là 14. Tìm CTHH của hợp chất ? Câu 2 : Một hợp chất khí có tỉ khối đối với không khí là 0,582 và trong đó N là 82,35%, còn lại là H a. Lập CTHH của hợp chất khíb,Tính thể tích ở điều kiện tiêu chuẩn của 3,4 gam hợp khí trên Câu 3 : Cho 4,8g Magie bằng dung dịch 14,6g axit clohidric HCl, thu được muối magie clorua và 0,4g khí hidro. a, viết PTHH của phản ứngb,...
Đọc tiếp
Câu 1 : Hợp chất A có thành phần % về khối lượng là : 85,7% C, còn lại là H. Hãy xác định CTHH của A, biết tỉ khối của khí A so với hidro là 14. Tìm CTHH của hợp chất ?
Câu 2 : Một hợp chất khí có tỉ khối đối với không khí là 0,582 và trong đó N là 82,35%, còn lại là H a. Lập CTHH của hợp chất khí
b,Tính thể tích ở điều kiện tiêu chuẩn của 3,4 gam hợp khí trên
Câu 3 : Cho 4,8g Magie bằng dung dịch 14,6g axit clohidric HCl, thu được muối magie clorua và 0,4g khí hidro. a, viết PTHH của phản ứng
b, tính khối lượng và số mol của MgCl2
một hợp chất X gồm 2 nguyên tố C và H, có tỉ khối với hidro là 8a,Hãy xác định CTHH của X biết hợp chất khí có thành phần phần trăm theo khối lượng của C bằng 75%.b,Hãy cho biết khí X ở điều kiện tiêu chuẩn có khối lượng là bao nhiêu?
Gọi CTHH của X là CxHy
Tỉ khối X so với H2 = 8 => Mx = 8.2 = 16(g/mol)
%mC = 75% , X chỉ chứa C và H => %mH = 100 - 75 = 25%
=> %mC = \(\dfrac{12.x}{16}\).100% = 75% <=> x = 1
%mH = \(\dfrac{y.1}{16}.100\)% = 25% <=> y = 4
Vậy CTHH của X là CH4.
Đúng 2
Bình luận (0)
1.Tính thành phần phần trăm khối lượng các nguyên tố hoá học có trong hợp chất P2O3 2. Hợp chất A có chứa 75%C và 25%H về khối lượng, biết tỉ khối của A so với khí hiđrô bằng 8. Xác định CTHH của chất A
1
\(MP_2O_3=110g/mol\)
\(\%P=\dfrac{31.2.100}{110}=58,2\%\)
\(\%O=100-58,2=41,8\%\)
2
\(MA=8.2=16g/mol\)
Tính theo hoá trị
=> cthh của A là CH\(_4\)
Đúng 1
Bình luận (1)
thành phần chính của khí thiên nhiên là hợp chất x.phân tử (x) có 75% khối lượng là carbon,còn lại là hydro.khối lượng của phân tử x là 16amu.xác định công thức hóa học của (x)
Câu 4: Khí X có tỉ khối đối với khí oxi là 0,5.Biết rằng X tạo bởi 75% khối lượng là C, còn lại là H. Hãy xác định CTHH của X. Câu 3: Lập các PTHH theo các sơ đồ sau và cho biết tỉ lệ số nguyên tử, phân tử giữa các chất trong phản ứng.a) Cu(OH)2 + Fe(NO3)3 ------- Cu(NO3)2 + Fe(OH)3b) Cu(NO3)2 + Zn ------- Zn(NO3)2 + Cu
Đọc tiếp
Câu 4: Khí X có tỉ khối đối với khí oxi là 0,5.Biết rằng X tạo bởi 75% khối lượng là C, còn lại là H. Hãy xác định CTHH của X.
Câu 3: Lập các PTHH theo các sơ đồ sau và cho biết tỉ lệ số nguyên tử, phân tử giữa các chất trong phản ứng.
a) Cu(OH)2 + Fe(NO3)3 -------> Cu(NO3)2 + Fe(OH)3
b) Cu(NO3)2 + Zn -------> Zn(NO3)2 + Cu
Câu 1 Hợp chất oxit B có khối lượng mol phân tử là 142g/mol thành phần % các nguyên tố theo khối lượng là 43,66% P còn lại là oxi Xác định CTPT Câu 2 Tìm công thức hóa học của khí A biết a Khí A nặng hơn khí hidro là 22 lần b thành phần theo khối lượng khí A là 27,3% C còn lại là O câu 3 Hòa tan hoàn toàn 4g oxit(A là kim loại hóa trị II) cần 146g dung dịch HCl 10% Xác định công thức hóa học của oxit
Đọc tiếp
Câu 1 Hợp chất oxit B có khối lượng mol phân tử là 142g/mol thành phần % các nguyên tố theo khối lượng là 43,66% P còn lại là oxi Xác định CTPT Câu 2 Tìm công thức hóa học của khí A biết a Khí A nặng hơn khí hidro là 22 lần b thành phần theo khối lượng khí A là 27,3% C còn lại là O câu 3 Hòa tan hoàn toàn 4g oxit(A là kim loại hóa trị II) cần 146g dung dịch HCl 10% Xác định công thức hóa học của oxit
Câu 1 :
\(CT:P_xO_y\)
\(\%P=\dfrac{31x}{142}\cdot100\%=43.66\%\)
\(\Rightarrow x=2\)
\(M_B=31\cdot2+16\cdot y=142\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow y=5\)
\(CTPT:P_2O_5\)
Đúng 3
Bình luận (0)
Câu 2 :
\(a.\)
\(M_A=22\cdot2=44\left(\dfrac{g}{mol}\right)\)
\(CT:C_xO_y\)
\(\%C=\dfrac{12x}{44}\cdot100\%=27.3\%\)
\(\Rightarrow x=1\)
\(M_A=12+32\cdot y=44\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow y=2\)
\(CT:CO_2\)
Đúng 3
Bình luận (0)
Câu 3 :
\(n_{HCl}=\dfrac{146\cdot10\%}{36.5}=0.4\left(mol\right)\)
\(AO+2HCl\rightarrow ACl_2+H_2O\)
\(0.2.........0.4\)
\(M_{AO}=A+16=\dfrac{4}{0.2}=20\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow A=4\)
=> Đề sai
Đúng 2
Bình luận (0)
một hợp chất khí có thành phần % theo khối lượng 82,35% N và 17,65% H . Xác định CTHH cảu chất đó , biết tỉ khối của hợp chất hidro bằng 8,5 gam
Gọi CTHH cần tìm là NxHy.
\(\Rightarrow x:y=\dfrac{82,35}{14}:\dfrac{17,65}{1}\approx1:3\)
→ CTHH cần tìm có dạng (NH3)n
Mà: \(d_{N_xH_y/H_2}=8,5\Rightarrow M_{N_xH_y}=8,5.2=17\left(g/mol\right)\)
\(\Rightarrow n=\dfrac{17}{14+1.3}=1\)
Vậy: CTHH cần tìm là NH3.
Đúng 3
Bình luận (0)
Một hợp chất khí A trong phân tử có một nguyên tử X liên kết với ba nguyên tử oxygen biết tỉ khối hơi của khí A so với khí hydrogen là 40.
a/Xác định khối lượng mol của khí A cho biết tên nguyên tố X
b/Tính thành phần trăm theo khối lượng của X có trong hợp chất A
Gọi CTTQ là : XO3
\(a,\rightarrow M_A=80\)
\(\rightarrow M_X=80-\left(16.3\right)=32\left(\dfrac{g}{mol}\right)\)
Vậy X là S ( lưu huỳnh )
\(\%m_{S\left(SO_3\right)}=\dfrac{32}{80}.100\%=40\%\)
Đúng 0
Bình luận (0)