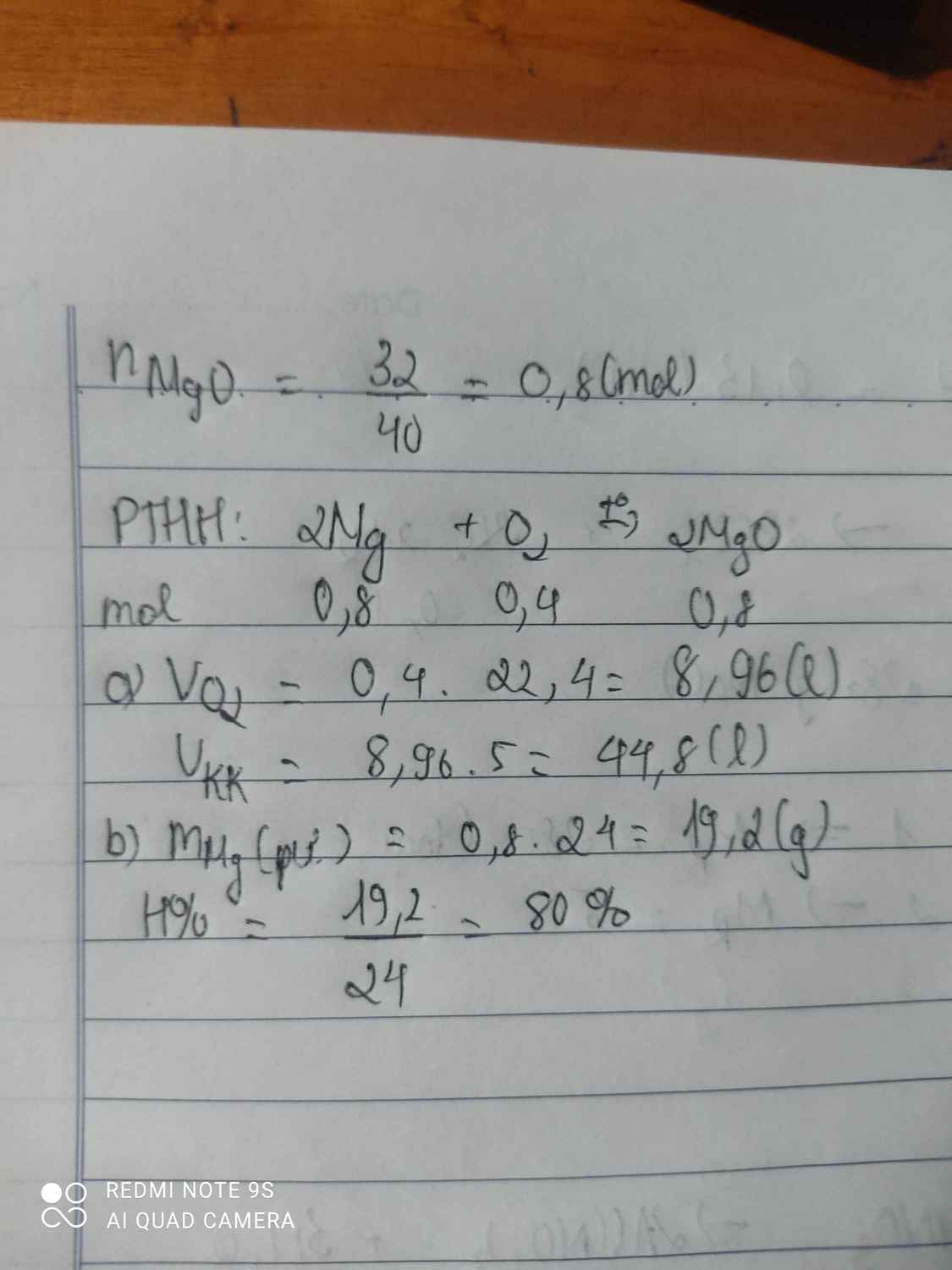Đốt cháy 51,2g Cu trong oxi a) tính thể tích oxi thu được. b) tính hiệu suất của phản ứng. Biết sau phản ứng thu được 48g CuO

Những câu hỏi liên quan
Đốt cháy 12,8g Cu trong không khí. Sau phản ứng thu được 12g Cuo
a, Tính thể tích khí Oxi cần dùng thêm để đốt cháy hết
Xem chi tiết
PTHH: \(2Cu+O_2\underrightarrow{t^o}2CuO\)
Ta có: \(n_{CuO}=\dfrac{12}{80}=0,15\left(mol\right)=n_{Cu\left(p/ư\right)}\)
\(\Rightarrow n_{Cu\left(dư\right)}=\dfrac{12,8}{64}-0,15=0,05\left(mol\right)\)
\(\Rightarrow n_{O_2\left(cầnthêm\right)}=0,025mol\) \(\Rightarrow V_{O_2\left(thêm\right)}=0,025\cdot22,4=0,56\left(l\right)\)
Đúng 1
Bình luận (0)
\(n_{Cu} = \dfrac{12,8}{64} = 0,2(mol)\\ n_{CuO} = \dfrac{12}{80} = 0,15(mol)\\ 2Cu + O_2 \xrightarrow{t^o} 2CuO\)
Ta thấy : nCu = 0,2 > nCuO = 0,15 nên Cu dư.
Theo PTHH : \(n_{O_2\ } = \dfrac{1}{2}n_{CuO} = 0,075(mol)\)
Nếu đốt cháy hết lượng Cu ban đầu thì cần \(n_{O_2} = \dfrac{1}{2}n_{Cu} = 0,1(mol)\)
Suy ra :
\(n_{O_2\ cần\ thêm} = 0,1 - 0,075 = 0,025(mol)\\ \Rightarrow V_{O_2} = 0,025.22,4 = 0,56(lít)\)
Đúng 0
Bình luận (0)
Câu 5.Đốt cháy hoàn toàn 1,92 g lưu huỳnh trong bình khí oxi. Tính thể tích khí SO2 (đktc) thu được sau phản ứng, biết hiệu suất phản ứng là 90%.
nS = 1,92/32 = 0,06 (mol)
PTHH: S + O2 -> (t°) SO2
Mol: 0,06 ---> 0,06 ---> 0,06
VSO2 (LT) = 0,06 . 22,4 = 1,344 (l)
VSO2 (TT) = 1,344 . 90% = 1,2096 (l)
Đúng 2
Bình luận (0)
nS= 0.06 mol
S + O2 -to-> SO2
Từ PTHH:
nSO2= 0.06 mol
VSO2= 1.344l
VSO2 thực = 1.344*90/100=1.2096l
Đúng 1
Bình luận (0)
đốt cháy 51,2 g Cu trong oxi, sau phản ứng thu được m gam CuO. a) Viết PTHH b) Tính m
\(n_{Cu}=\dfrac{51,2}{64}=0,8\left(mol\right)\\ PTHH:2Cu+O_2\underrightarrow{t^o}2CuO\\ \left(mol\right)....0,8\rightarrow..0,4.....0,8\\ m_{CuO}=0,8.80=64\left(g\right)\)
Đúng 4
Bình luận (0)
đốt cháy hết 12,8g Cu trong bình khí 02 thì thu được CuO a)Viết pthh b) tính thể tích khí oxi cần dùng (đktc)c) dùng lượng oxi nói trên cho phản ứng với 16,8g sắt thì thu được bao nhiêu g sắt từ oxi
Cho khí Hidro qua ống nghiệm có chứa 16g CuO đun nóng, sau khi phản ứng thấy thu được Cu và H2O
a) Tính khối lượng Cu thu được
b) Tính thể tích H2 (đo ở đktc) tham gia phản ứng CuO
c) Với lượng khí H2 trên có thể bị đốt cháy trong bao nhiêu lít khí Oxi
a) \(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
PTHH: \(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
0,2--->0,2---->0,2
\(\Rightarrow m_{Cu}=0,2.64=12,8\left(g\right)\)
b) \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
c) \(2H_2+O_2\xrightarrow[]{t^o}2H_2O\)
0,2--->0,1
\(\Rightarrow V_{O_2}=0,1.22,4=2,24\left(l\right)\)
Đúng 1
Bình luận (0)
a: CuO+H2->Cu+H2O
0,2 0,2 0,2 0,2
mCu=0,2*64=12,8(g)
b: V=0,2*22,4=4,48(lít)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 3,1g photpho trong bình đựng khí Oxi dư. Sau phản ứng thu được m(g) chất rắn.
a) Tính khối lượng chất rắn thu được sau phản ứng?
b) Tính thể tích khí Oxi (ở đktc) đã dùng trong phản ứng này?
nP = 3.1/31 = 0.1 (mol)
4P + 5O2 -to-> 2P2O5
0.1__0.125_____0.05
mP2O5 = 0.05*142 = 7.1 (g)
VO2 = 0.125 * 22.4 = 2.8 (l)
Đúng 2
Bình luận (0)
Bài 16: Đốt cháy 24 gam kim loại Magie trong không khí, sau khi phản ứng thu được 32 gam magie oxit. Giả sử oxi chiếm 20% thể tích không khí, còn lại là nitơ.
a) Tính thể tích không khí (ở đktc) dùng để đốt cháy Magie.
b) Tính hiệu suất phản ứng.
giúp mình
Đốt cháy hoàn toàn hỗn hợp X gồm Cu và Fe trong khí Oxi dư ở nhiệt độ cao thấy thể tích oxi phản ứng là 6,72 lít(đktc). Sau phản ứng thu được 16g đồng Oxi.
a)Tính khối lượng từng chất trong X.
b) Tính phần trăm khối lượng từng chất trong x
Gọi x, y lần lượt là số mol của Cu và Fe.
Ta có: \(n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
a. PTHH: 2Cu + O2 ---to---> 2CuO (1)
3Fe + 2O2 ---to---> Fe3O4 (2)
Ta có: \(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
Theo PT(1): \(n_{Cu}=n_{CuO}=0,2\left(mol\right)\)
Theo PT(1): \(n_{O_2}=\dfrac{1}{2}.n_{Cu}=\dfrac{1}{2}x\left(mol\right)\)
Theo PT(2): \(n_{O_2}=\dfrac{2}{3}.n_{Fe}=\dfrac{2}{3}y\left(mol\right)\)
=> \(\dfrac{1}{2}x+\dfrac{2}{3}y=0,3\)
Mà nCu = 0,2(mol)
Thay vào, ta được: \(\dfrac{1}{2}.0,2+\dfrac{2}{3}y=0,3\)
=> y = 0,3(mol)
=> \(m_{Cu}=0,2.64=12,8\left(g\right)\)
\(m_{Fe}=0,3.56=16,8\left(g\right)\)
b. \(\%_{Cu}=\dfrac{12,8}{12,8+16,8}.100\%=43,24\%\)
\(\%_{Fe}=100\%-43,24\%=56,76\%\)
Đúng 1
Bình luận (0)
Trong phòng thí nghiệm, bạn Minh nung 63,2 gam KMnO4.
a/ Tính thể tích khí oxi thu được ở đktc biết hiệu suất phản ứng đạt 90%.
b/ Lượng oxi thu được ở câu a vừa đủ để đốt cháy 6,48 gam kim loại R hóa trị III. Tìm kim loại R.
\(n_{KMnO_4}=\dfrac{63,2}{158}=0,4\left(mol\right)\\
pthh:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
0,4 0,2
=> \(V_{O_2\left(lt\right)}=0,2.22,4=4,48\left(l\right)\\
V_{O_2\left(tt\right)}=\dfrac{90.4,48}{100}=4,032\left(l\right)\)
Đúng 3
Bình luận (0)