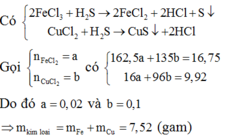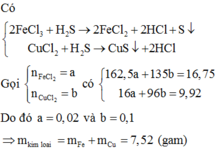Từ hỗn hợp rắn có chứa CuCl2, AlCl3. Hãy điều chế 2 kim loại Cu, Al ra riêng biệt

Những câu hỏi liên quan
Từ hỗn hợp chất rắn chứa CuCl2 NaCl , dụng cụ cần thiết có đủ hãy điều chế kim loại Na riêng biệt
Cho NaOH vào hh
+Tạo kết tủa trắng là CuCl2--->Lọc dc NaCl tinh khiết
Điện phân dd có màng ngăn NaCl
2NaCl------->2Na+Cl2
1.Không dùng thêm thuốc thử nào khác hãy nhận ra 4 dd riêng biệt: MgCl2, NaOH, NaCl, HCl
2.Từ hỗn hợp CuO và Fe2O3.Chỉ dùng thêm Al và HCl viết ptpu điều chế kim loại Cu theo 3 cách.
bài 2 :cách 1:
Al + HCl -> H2.
H2 khử hh.
cho hh kloại thu đc vào HCl ;lại thấy Cu k tan
PTPƯ:
2Al+ 6HCl-------> 2AlCl3 + 3H2
H2 + CuO ---- xt nhiệt độ--------> Cu+ H2O
3H2+ Fe2O3------- xt nhiệt độ----> 2Fe+ 3H2O
Fe+HCl -------> FeCl2
cách 2; dùng pư nhiệt nhôm để thu đc hh 2kloại Cu và fe.
sau đó cho vào dd HCl
3CuO + 2Al ----- xt nhiệt độ------> Al2O3 + 3Cu
Fe2O3+ 2Al --------xt nhiệt độ-------> Al2O3+ 2Fe
cách 3: cho hh oxit vào dd HCl. thu đc 2 m' là CuCl2 và FeCl3.
cho Al vào dd để đẩy 2 m'
thu đc hh 2 kloại Cu và Fe. còn lại làm giống ở trên :d
CuO + 2HCl -------> CuCl2 + H2O
Fe2O3 +6 HCl -------> 2FeCl3 +3 H2O
Al + FeCl3------> AlCl3 + Fe
2Al+ 3CuCl2-------> 2AlCl3+ 3Cu
Bài 1 bạn kẻ bảng cho từng chất tác dụng với nhau rồi nhận biết sự có mặt từng chất qua hiện tượng .
Đúng 0
Bình luận (0)
1 Từ các chất rắn ban đầu: Al2O3, NaCl, PbO, Cu(NO3)2 . Hãy viết các phương trình phản ứng để điều chế các kim loại tương ứng: Al, Na, Pb, Cu bằng các phương pháp thích hợp, ghi rõ điều kiện phản ứng nếu có. 2. Hòa tan hoàn toàn m gam hỗn hợp gồm Al và Al2O3 cần vừa đủ 250ml dung dịch KOH 2M. Nếu cũng cho m gam hỗn hợp trên vào dung dịch HNO3 loãng, dư thì thu được 0,56 lít khí N2O (đktc) và dung dịch X. Cô cạn X thu được 107,5 gam muối khan. Tìm giá trị của m?
Đọc tiếp
1 Từ các chất rắn ban đầu: Al2O3, NaCl, PbO, Cu(NO3)2 . Hãy viết các phương trình phản ứng để điều chế các kim loại tương ứng: Al, Na, Pb, Cu bằng các phương pháp thích hợp, ghi rõ điều kiện phản ứng nếu có.
2. Hòa tan hoàn toàn m gam hỗn hợp gồm Al và Al2O3 cần vừa đủ 250ml dung dịch KOH 2M. Nếu cũng cho m gam hỗn hợp trên vào dung dịch HNO3 loãng, dư thì thu được 0,56 lít khí N2O (đktc) và dung dịch X. Cô cạn X thu được 107,5 gam muối khan. Tìm giá trị của m?
1. \(Al_2O_3\underrightarrow{^{đpnc}}2Al+\dfrac{3}{2}O_2\)
\(NaCl\underrightarrow{^{đpnc}}Na+\dfrac{1}{2}Cl_2\)
\(PbO+H_2\underrightarrow{t^o}Pb+H_2O\)
\(Fe+Cu\left(NO_3\right)_2\rightarrow Fe\left(NO_3\right)_2+Cu\)
Đúng 2
Bình luận (0)
2. Gọi: \(\left\{{}\begin{matrix}n_{Al}=a\left(mol\right)\\n_{Al_2O_3}=b\left(mol\right)\\n_{NH_4NO_3}=c\left(mol\right)\end{matrix}\right.\)
- Cho pư với KOH: \(n_{KOH}=0,25.2=0,5\left(mol\right)\)
BTNT K, có: nKAlO2 = nKOH = 0,5 (mol)
BTNT Al, có: nAl + 2nAl2O3 = nKAlO2 ⇒ a + 2b = 0,5 (1)
- Cho pư với HNO3: \(n_{N_2O}=\dfrac{0,56}{22,4}=0,025\left(mol\right)\)
BTNT Al có: nAl(NO3)3 = nAl + 2nAl2O3 = a + 2b (mol)
Mà: mAl(NO3)3 + mNH4NO3 = 107,5 (g)
⇒ 213(a+2b) + 80c = 107,5
⇒ 213a + 426b + 80c = 107,5 (2)
BT e, có: 3nAl = 8nN2O + 8nNH4NO3 ⇒ 3a = 8.0,025 + 8c (3)
Từ (1), (2) và (3) \(\Rightarrow\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,2\left(mol\right)\\c=0,0125\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m=m_{Al}+m_{Al_2O_3}=0,1.27+0,2.102=23,1\left(g\right)\)
Đúng 2
Bình luận (0)
Hỗn hợp X chứa các kim loại: Al, Mg, Cu. Hãy trình bày phương pháp hóa học để tách riêng hoàn toàn từng kim loại ra khỏi hỗn hợp X
- Hòa tan hỗn hợp vào dd NaOH dư, thu được:
+ dung dịch chứa NaAlO2, NaOH
\(2NaOH+2Al+2H_2O\rightarrow2NaAlO_2+3H_2\)
+ phần rắn không tan: Mg, Cu
- Dẫn khí CO2 dư đi qua dung dịch, thu được phân két tủa là Al(OH)3, nung kết tủa thu được Al2O3, nhiệt phân nóng chảy thu được Al
\(NaAlO_2+CO_2+2H_2O\rightarrow NaHCO_3+Al\left(OH\right)_3\downarrow\)
\(2Al\left(OH\right)_3\underrightarrow{t^o}Al_2O_3+3H_2O\)
\(2Al_2O_3\underrightarrow{npnc}4Al+3O_2\)
- Hòa tan phân chất rắn vào dd HCl dư, thu được
+ phần dung dịch: HCl, MgCl2
Mg + 2HCl --> MgCl2 + H2
+ phần rắn không tan: Cu
- Cô cạn dung dịch, thu được MgCl2, nhiệt phân nóng chảy thu được Mg
\(MgCl_2\underrightarrow{npnc}Mg+Cl_2\)
Đúng 2
Bình luận (0)
Từ hỗn hợp gồm CuCO3, MgCO3, Al2O3 và BaCO3 hãy điều chế từng kim loại riêng biệt với điều kiện không làm thay đổi khối lượng của từng kim loại trong hỗn hợp
Yêu cầu bài toán điều chế Cu, Mg, Al, Ba mà không làm thay đổi khối lượng kim loại của chúng
Các phương trình hóa học xảy ra là:
Al2O3 + NaOH → NaAlO2 + H2O
NaAlO2 + CO2 + 2H2O → Al(OH)3↓ + NaHCO3
2Al(OH)3 → t ∘ Al2O3 + 3H2O
2Al2O3 → d p n c 4Al + 3O2↑
CuCO3 → t ∘ CuO + CO2↑
MgCO3 → t ∘ MgO + CO2↑
BaCO3 BaO + CO2↑
BaO + H2O → Ba(OH)2
Ba(OH)2 + 2HCl → BaCl2 + H2O
BaCl2 → d p n c Ba + Cl2
CuO + H2 → t ∘ Cu↓ + H2O
MgO + 2HCl → MgCl2 + H2O
MgCl2 → d p n c Mg + Cl2
Chú ý:
Khi cô cạn HCl dễ bay hơi nên không còn mặt HCl trong dung dịch thu được
Đúng 0
Bình luận (0)
Giúp em với ạ
Tách chất từ hỗn hợp chứa đồng thời
a)Ca(HCO3)2; CaCl2
b)CaCO3; CaCl2
c)Al; Ag
d)AlCl3; CuCl2; AgCl
e)Cu; Zn; Fe; Ag
f)CuO; AlCl3; CuCl2; Al2O3
g)Al(NO3)3; NaNO3; Mg(NO3)2
Cho 16,75 gam hỗn hợp X gồm FeCl3, CuCl2 vào dung dịch H2S dư, sau khi phản ứng xảy ra hoàn toàn thu được 9,92 gam chất rắn (bỏ qua sự thủy phân của các ion kim loại). Từ hỗn hợp X có thể điều chế được tối đa bao nhiêu gam kim loại? A. 9,23 gam. B. 7,52 gam C. 6,97 gam. D. 5,07 gam.
Đọc tiếp
Cho 16,75 gam hỗn hợp X gồm FeCl3, CuCl2 vào dung dịch H2S dư, sau khi phản ứng xảy ra hoàn toàn thu được 9,92 gam chất rắn (bỏ qua sự thủy phân của các ion kim loại). Từ hỗn hợp X có thể điều chế được tối đa bao nhiêu gam kim loại?
A. 9,23 gam.
B. 7,52 gam
C. 6,97 gam.
D. 5,07 gam.
Cho 16,75 gam hỗn hợp X gồm FeCl3, CuCl2 vào dung dịch H2S dư, sau khi phản ứng xảy ra hoàn toàn thu được 9,92 gam chất rắn (bỏ qua sự thủy phân của các ion kim loại). Từ hỗn hợp X có thể điều chế được tối đa bao nhiêu gam kim loại? A. 9,23 gam. B. 7,52 gam C. 6,97 gam. D. 5,07 gam.
Đọc tiếp
Cho 16,75 gam hỗn hợp X gồm FeCl3, CuCl2 vào dung dịch H2S dư, sau khi phản ứng xảy ra hoàn toàn thu được 9,92 gam chất rắn (bỏ qua sự thủy phân của các ion kim loại). Từ hỗn hợp X có thể điều chế được tối đa bao nhiêu gam kim loại?
A. 9,23 gam.
B. 7,52 gam
C. 6,97 gam.
D. 5,07 gam.
Cho hỗn hợp kim loại Mg, Fe vào dung dịch chứa hỗn hợp muối Cu(NO3)2, AgNO3. Phản ứng xảy ra hoàn toàn, thu được hỗn hợp rắn A gồm 3 kim loại và dung dịch chứa 2 muối. Trình bày phương pháp tách riêng từng kim loại ra khỏi hỗn hợp A mà không làm thay đổi lượng của chúng có trong A. Viết các phương trình phản ứng.
Tính hoạt động kim loại: Mg > Fe > Cu > Ag
=> Hỗn hợp A:
+ 3 kim loại: Ag, Cu, Fe(dư)
+ 2 dung dịch: Mg(NO3)2 và Fe(NO3)2
\(Mg+2AgNO_3\rightarrow Mg\left(NO_3\right)_2+2Ag\\ Mg+Cu\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Cu\\ Fe+2AgNO_3\rightarrow Fe\left(NO_3\right)_2+2Ag\\ Fe+Cu\left(NO_3\right)_2\rightarrow Fe\left(NO_3\right)_2+Cu\)
Tách riêng kim loại: Cho hỗn hợp tác dụng với dung dịch HCl dư, lấy phần dung dịch tác dụng hết với dung dịch NaOH dư, lọc lấy kết tủa đem nung ngoài không khí tới khối lượng không đổi.
Cho luồng H2 nóng dư đi qua thu được Fe tinh khiết
\(Fe+2HCl\rightarrow FeCl_2+H_2\\ NaOH+HCl\rightarrow NaCl+H_2O\\ 2NaOH+FeCl_2\rightarrow Fe\left(OH\right)_2\downarrow+2NaCl\\ 4Fe\left(OH\right)_2+O_2\rightarrow2Fe_2O_3+4H_2O\\ 3H_2+Fe_2O_3\rightarrow2Fe+3H_2O\)
(Tách Fe)
Phần chất rắn nung trong không khí tới khối lượng không đổi, cho tác dụng với dung dịch HCl dư lọc lấy kết tủa sấy khô thu được Ag tinh khiết.
\(2Cu+O_2\underrightarrow{^{to}}2CuO\\ CuO+2HCl\rightarrow CuCl_2+H_2O\)
Phần dung dịch cho tác dụng với dung dịch NaOH dư lấy kết tả nung trong không khí tới khối lượng không đổi thu được chất rắn rồi cho luồng H2 nóng dư đi qua thu được Cu tinh.
\(NaOH+HCl\rightarrow NaCl+H_2O\\ 2NaOH+CuCl_2\rightarrow Cu\left(OH\right)_2\downarrow+2NaCl\\ H_2+CuO\underrightarrow{^{to}}Cu+H_2O\)
Đúng 0
Bình luận (0)
Cho hỗn hợp bột Al, Fe vào dung dịch chứa Cu(NO3)2 và AgNO3. Sau khi các phản ứng xảy ra hoàn toàn, thu được hỗn hợp rắn gồm ba kim loại. Ba kim loại đó là: A. Fe, Cu, Ag B. Al, Cu, Ag C. Al, Fe, Cu D. Al, Fe, Ag
Đọc tiếp
Cho hỗn hợp bột Al, Fe vào dung dịch chứa Cu(NO3)2 và AgNO3. Sau khi các phản ứng xảy ra hoàn toàn, thu được hỗn hợp rắn gồm ba kim loại. Ba kim loại đó là:
A. Fe, Cu, Ag
B. Al, Cu, Ag
C. Al, Fe, Cu
D. Al, Fe, Ag