Câu 9: Có 6 lọ mất nhãn đựng các dung dịch không màu là: Na2SO4 , Na2CO3 , BaCl2 , Ba(NO3)2 , AgNO3 , MgCl2 không dùng thêm các chất khác, hãy trình bày cách nhận biết các dung dịch trên,

Những câu hỏi liên quan
Có 5 lọ không nhãn đựng các dung dịch không màu là NaCl, H2SO4, CuSO4, BaCl, NaOH. Bằng phương pháp hóa học và không dùng thêm các hóa chất khác hãy trình bày cách nhận biết các dung dịch trên.
trích mẫu thử đánh số thứ tự
cho quỳ tím vào từng mẫu thử, mẫu nào làm quỳ tím chuyển đỏ là axit: H2SO4
-mẫu nào làm quỳ tím chuyển xanh là: NaOH
-mẫu nào không làm đổi màu quỳ tím là: NaCl,CuSo4,BaCL2-nhóm A
cho H2SO4 vào nhóm A
\(BaCL2+H2SO4->BaSO4+2HCL\)
BaCL2 tạo kết tủa trắng
-CuSO4 và NaCL không hiện tượng-nhóm B
cho BaCL2 vào nhóm B
\(CuSO4+BaCL2->CuCL2+BáSO4\)
CuSO4 tạo kết tủa trắng
NaCL không hiện tượng
Đúng 2
Bình luận (0)
Bài 14. Phân biệt các dung dịch chứa trong các lọ bị mất nhãn sau chỉ bằng dung dịch phenol phtalein: Na2SO4, H2SO4, BaCl2, NaOH, MgCl2.Bài 15: Không được dùng thêm thuốc thử nào khác, hãy nhận biết các dung dịch bằng phương pháp hoá học.a) Na2CO3, HCl, BaCl2b) HCl, H2SO4, Na2CO3, BaCl2c) MgCl2, NaOH, NH4Cl, BaCl2, H2SO4Bài 16: Hãy phân biệt các chất sau chứa trong các lọ bị mất nhãn mà không dùng thuốc thử nào: NaHCO3, HCl, Ba(HCO3)2, MgCl2, NaCl.Bài 17: Có 4 lọ mất nhãn đựng 4 dung dịch HCl,...
Đọc tiếp
Bài 14. Phân biệt các dung dịch chứa trong các lọ bị mất nhãn sau chỉ bằng dung dịch phenol phtalein: Na2SO4, H2SO4, BaCl2, NaOH, MgCl2.
Bài 15: Không được dùng thêm thuốc thử nào khác, hãy nhận biết các dung dịch bằng phương pháp hoá học.
a) Na2CO3, HCl, BaCl2
b) HCl, H2SO4, Na2CO3, BaCl2
c) MgCl2, NaOH, NH4Cl, BaCl2, H2SO4
Bài 16: Hãy phân biệt các chất sau chứa trong các lọ bị mất nhãn mà không dùng thuốc thử nào: NaHCO3, HCl, Ba(HCO3)2, MgCl2, NaCl.
Bài 17: Có 4 lọ mất nhãn đựng 4 dung dịch HCl, H2SO4, BaCl2, Na2CO3. Hãy phân biệt các dung dịch mà không dùng bất kỳ thuốc thử nào.
Bài 18: Không được dùng thêm thuốc thử , hãy phân biệt 3 dung dịch chứa trong 3 lọ mất nhãn: NaCl, AlCl3, NaOH.
Bài 19. Trình bày phương pháp phân biệt các dung dịch chứa trong các lọ bị mất nhãn sau mà không dùng thuốc thử nào:
a. HCl, AgNO3, Na2CO3, CaCl2.
b.HCl, H2SO4, BaCl2, Na2CO3.
Bài 20. Không dùng thuốc thử hãy phân biệt các chất sau chứa trong các lọ riêng biệt bị mất nhãn: NaOH, NH4Cl, BaCl2, MgCl2, H2SO4.
Từ bài 16 các bạn tham khảo để làm sau.
Câu 8: Có 5 lọ mất nhãn đựng 5 dung dịch : NaOH, KCl, MgCl2 , CuCl2, AlCl3. Hãy nhận biết các dung dịch trên mà không cần dùng thêm hoá chất khác.
- Trích một ít các chất làm mẫu thử
- Chọn 1 trong các dd, cho tác dụng với lượng dư các dd còn lại, ta có bảng kết quả:
| NaOH | KCl | MgCl2 | CuCl2 | AlCl3 | |
| NaOH(dư) | x | - | Kết tủa trắng, không tan | Kết tủa xanh | Kết tủa trắng, tăng dần đến cực đại rồi tan dần trong dd |
| KCl(dư) | - | x | - | - | - |
| MgCl2(dư) | Kết tủa trắng, không tan | - | x | - | - |
| CuCl2(dư) | Kết tủa xanh | - | - | x | - |
| AlCl3(dư) | Kết tủa trắng, không tan | - | - | - | x |
+ dd làm xuất hiện 2 lần kết tủa trắng, không tan; 1 lần kết tủa xanh: NaOH
+ dd không làm xuất hiện hiện tượng: KCl
+ dd làm xuất hiện 1 lần kết tủa trắng không tan: MgCl2
+ dd làm xuất hiện 1 lần kết tủa xanh: CuCl2
+ dd làm xuất hiện 1 lần kết tủa trắng, tăng dần đến cực đại rồi tan dần trong dd: AlCl3
\(2NaOH+MgCl_2\rightarrow2NaCl+Mg\left(OH\right)_2\downarrow\)
\(2NaOH+CuCl_2\rightarrow Cu\left(OH\right)_2\downarrow+2NaCl\)
\(3NaOH+AlCl_3\rightarrow Al\left(OH\right)_3\downarrow+3NaCl\)
\(Al\left(OH\right)_3+NaOH\rightarrow NaAlO_2+2H_2O\)
Đúng 1
Bình luận (0)
Không dùng thêm hóa chất nào khác, hãy nhận biết các dung dịch sau đựng trong các lọ mất nhãn: dd HCl; AgNO3; Na2CO3; CaCl2
Nhận biết các dung dịch sau bằng phương pháp hóa học:
a, Có 4 lọ không nhãn, mỗi lọ đựng một dung dịch không màu sau: NaOH, BaCl2, K2SO4, H2SO4.
b, Có 4 lọ không nhãn, mỗi lọ đựng một dung dịch không màu sau: HCl, KCl, Na2SO4, Ca(OH)2.
Hãy trình bày phương pháp nhận biết dung dịch đựng trong mỗi lọ? Viết các phương trình hóa học xảy ra (nếu có). Dụng cụ hóa chất coi như có đủ.
c, Bằng phương pháp hóa học hãy nhận biết các dung dịch mất nhãn sau:
HCl, K2SO4, KNO3
d, Nhận biết các chất rắn: Na2O,...
Đọc tiếp
Nhận biết các dung dịch sau bằng phương pháp hóa học: a, Có 4 lọ không nhãn, mỗi lọ đựng một dung dịch không màu sau: NaOH, BaCl2, K2SO4, H2SO4. b, Có 4 lọ không nhãn, mỗi lọ đựng một dung dịch không màu sau: HCl, KCl, Na2SO4, Ca(OH)2. Hãy trình bày phương pháp nhận biết dung dịch đựng trong mỗi lọ? Viết các phương trình hóa học xảy ra (nếu có). Dụng cụ hóa chất coi như có đủ. c, Bằng phương pháp hóa học hãy nhận biết các dung dịch mất nhãn sau: HCl, K2SO4, KNO3 d, Nhận biết các chất rắn: Na2O, Fe2O3, Al. Chỉ được dùng nước hãy nhận ra mỗi chất
a, _ Trích mẫu thử.
_ Nhỏ vài giọt từng mẫu thử vào giấy quỳ tím.
+ Nếu quỳ tím chuyển xanh, đó là NaOH.
+ Nếu quỳ tím chuyển đỏ, đó là H2SO4.
+ Nếu quỳ tím không chuyển màu, đó là BaCl2 và K2SO4. (1)
_ Nhỏ vài giọt từng mẫu thử nhóm (1) vào ống nghiệm chứa dd BaCl2.
+ Nếu xuất hiện kết tủa trắng, đó là K2SO4.
PT: \(K_2SO_4+BaCl_2\rightarrow2KCl+BaSO_{4\downarrow}\)
+ Nếu không có hiện tượng, đó là BaCl2.
_ Dán nhãn.
b, _ Trích mẫu thử.
_ Nhỏ vài giọt từng mẫu thử vào giấy quỳ tím.
+ Nếu quỳ tím chuyển đỏ, đó là HCl.
+ Nếu quỳ tím chuyển xanh, đó là Ca(OH)2.
+ Nếu quỳ tím không đổi màu, đó là KCl, Na2SO4. (1)
_ Nhỏ một lượng mẫu thử nhóm (1) vào ống nghiệm chứa dd BaCl2.
+ Nếu xuất hiện kết tủa trắng, đó là Na2SO4.
PT: \(BaCl_2+Na_2SO_4\rightarrow2NaCl+BaSO_{4\downarrow}\)
+ Nếu không hiện tượng, đó là KCl.
_ Dán nhãn.
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
a, _ Trích mẫu thử.
_ Nhỏ vài giọt từng mẫu thử vào giấy quỳ tím.
+ Nếu quỳ tím hóa đỏ, đó là HCl.
+ Nếu quỳ tím không đổi màu, đó là K2SO4 và KNO3. (1)
_ Nhỏ một lượng mẫu thử nhóm (1) vào ống nghiệm chứa dd BaCl2.
+ Nếu xuất hiện kết tủa trắng, đó là K2SO4.
PT: \(BaCl_2+K_2SO_4\rightarrow2KCl+BaSO_{4\downarrow}\)
+ Nếu không có hiện tượng, đó là KNO3.
_ Dán nhãn.
d, _ Trích mẫu thử.
_ Hòa tan từng mẫu thử vào nước.
+ Nếu tan, đó là Na2O.
PT: \(Na_2O+H_2O\rightarrow2NaOH\)
+ Nếu không tan, đó là Fe2O3 và Al. (1)
_ Tiếp tục đem mẫu thử nhóm (1) hòa tan trong dd NaOH vừa thu được.
+ Nếu tan, có khí thoát ra, đó là Al.
PT: \(2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2\)
+ Nếu không tan, đó là Fe2O3.
_ Dán nhãn.
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
Có 6 dung dịch đựng trong 6 lọ mất nhãn : Mg
(
N
O
3
)
2
, Zn, Pb
(
N
O
3
)
2
, Al
C
l
3
, KOH và NaCl. Chỉ dùng thêm dung dịch
A...
Đọc tiếp
Có 6 dung dịch đựng trong 6 lọ mất nhãn : Mg ( N O 3 ) 2 , Zn, Pb ( N O 3 ) 2 , Al C l 3 , KOH và NaCl. Chỉ dùng thêm dung dịch A g N O 3 và một thuốc thử nữa, hãy trình bày cách nhận biết từng dung dịch. Viết các phương trình hoá học dưới dạng phân tử và ion rút gọn của các phản ứng nhận biết đó.
Dùng dung dịch phenolphtalein nhận ra dung dịch KOH.
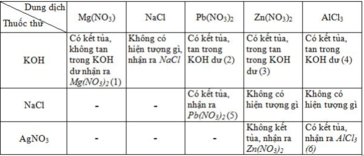
Các phương trình hoá học :
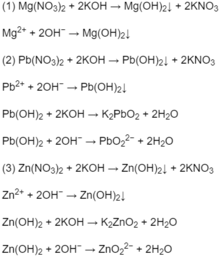
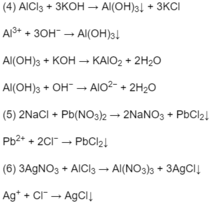
Đúng 0
Bình luận (0)
Chỉ dùng một thuốc thử, trình bày cách nhận biết các dung dịch không màu đựng riêng biệt bị mất nhãn: HCl, NaCl, MgCl2, Na2SO4.
- Dùng quỳ tím
+) Hóa đỏ: HCl
+) Không đổi màu: NaCl, MgCl2 và Na2SO4
- Đổ dd BaCl2 vào từng dd còn lại
+) Xuất hiện kết tủa trắng: Na2SO4
PTHH: \(BaCl_2+Na_2SO_4\rightarrow2NaCl+BaSO_4\downarrow\)
+) Không hiện tượng: NaCl và MgCl2
- Đổ dd KOH vào 2 dd còn lại
+) Xuất hiện kết tủa: MgCl2
PTHH: \(MgCl_2+2KOH\rightarrow2KCl+Mg\left(OH\right)_2\downarrow\)
+) Không hiện tượng: NaCl
Đúng 2
Bình luận (0)
Chỉ dùng một thuốc thử, trình bày cách nhận biết các dung dịch không màu đựng riêng biệt bị mất nhãn: HCl, NaCl, MgCl2, Na2SO4.
- Dùng quỳ tím
+) Hóa đỏ: HCl
+) Không đổi màu: NaCl, MgCl2 và Na2SO4
- Đổ dd BaCl2 vào từng dd còn lại
+) Xuất hiện kết tủa trắng: Na2SO4
PTHH: BaCl2+Na2SO4→2NaCl+BaSO4↓
+) Không hiện tượng: NaCl và MgCl2
- Đổ dd KOH vào 2 dd còn lại
+) Xuất hiện kết tủa: MgCl2
PTHH: MgCl2+2KOH→2KCl+Mg(OH)2↓
+) Không hiện tượng: NaCl
Đúng 2
Bình luận (1)
Không dùng thêm hóa chất nào khác, bằng phương pháp hóa học hãy phân biệt các dung dịch sau đựng trong các lọ riêng biệt bị mất nhãn là: HCl;Ba(OH)2;Na2CO3;MgCl2
| $HCl$ | $Ba(OH)_2$ | $Na_2CO_3$ | $MgCl_2$ | |
| $HCl$ | không hiện tượng | không hiện tượng | Khí không màu | không hiện tượng |
| $Ba(OH)_2$ | không hiện tượng | không hiện tượng | Kết tủa trắng | Kết tủa trắng |
| $Na_2CO_3$ | Khí không màu | Kết tủa trắng | không hiện tượng | Kết tủa trắng |
| $MgCl_2$ | không hiện tượng | Kết tủa trắng | Kết tủa trắng | không hiện tượng |
| Kết quả : | (1 khí) | (2 kết tủa) | (1 khí 2 kết tủa) | (2 kết tủa) |
- mẫu thử tạo 1 khí là HCl
- mẫu thử tạo 2 kết tủa là $Ba(OH)_2,MgCl_2$ - gọi là nhóm 1
- mẫu thử tạo 1 khí và 2 kết tủa là $Na_2CO_3$
Cho dung dịch $Na_2CO_3$ vào nhóm 1, lọc lấy kết tủa rồi nung đến khối lượng không đổi rồi cho vào dd $Na_2CO_3$
- mẫu thử nào tan là $Ba(OH)_2$
$Ba(OH)_2 + Na_2CO_3 \to BaCO_3 + 2NaOH$
$BaCO_3 \xrightarrow{t^o} BaO + CO_2$
$BaO + H_2O \to Ba(OH)_2$
- mẫu thử không tan là $MgCl_2$
$MgCl_2 + Na_2CO_3 \to MgCO_3 + 2NaCl$
$MgCO_3 \xrightarrow{t^o} MgO + CO_2$
Đúng 1
Bình luận (0)





















