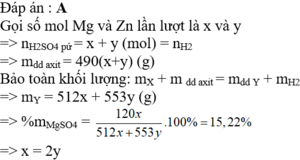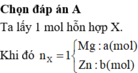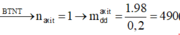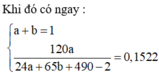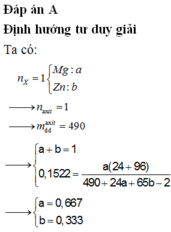Hòa tan hoàn toàn hỗn hợp X gồm Fe và Zn bằng 1 lượng vừa đủ dung dịch H2SO4 10%. Thu đc dung dịch Y và 2,24 lít khí H2 ở đktc. Nồng độ mol của ZnSO4 trong dung dịch Y là 11,6022%. Tính khối lượng của mỗi kim loại trong hỗn hợp X.

Những câu hỏi liên quan
Câu 2: Hòa tan hoàn toàn 20 gam hỗn hợp và FeO bằng lượng vừa đủ dung dịch H2SO4 gồm Fe 10%, thu được 2,24 lít khí H2 (ở đktc) và dung dịch Y. a) Viết các phương trình phản ứng xảy ra. b) Tính khối lượng dung dịch Y và C% của chất tan trong dung dịch Y. (45,6g và 14,53%)
Hòa tan hoàn toàn hỗn hợp X gồm Fe và Zn bằng một lượng vừa đủ dung dịch H2SO4 10% thu được
dung dịch Y và 22,4 lít khí hidro (đktc). Nồng độ của ZnSO4 trong dung dịch Y là 11,6022%. Tính khối
lượng mỗi kim loại trong X.
có nè bn lên học 24h câu hỏi của gấu teddy![]()
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn hỗn hợp X gồm Mg và Zn bằng một lượng vừa đủ dung dịch H2SO4 20% loãng thu được dung dịch Y. Nồng độ của MgSO4 trong dung dịch Y là 15,22%. Nồng độ % của ZnSO4 trong dung dịch Y là : A. 10,21% B. 15,22% C. 18,21% D. 15,16%
Đọc tiếp
Hòa tan hoàn toàn hỗn hợp X gồm Mg và Zn bằng một lượng vừa đủ dung dịch H2SO4 20% loãng thu được dung dịch Y. Nồng độ của MgSO4 trong dung dịch Y là 15,22%. Nồng độ % của ZnSO4 trong dung dịch Y là :
A. 10,21%
B. 15,22%
C. 18,21%
D. 15,16%
Hòa tan hoàn toàn hỗn hợp X gồm Mg và Zn bằng một lượng vừa đủ dung dịch H2SO4 20% (loãng) thu được dung dịch Y. Nồng độ của MgSO4 trong dung dịch Y là 15,22%. Nồng độ % của ZnSO4 trong dung dịch Y là :
A. 10,21%.
B. 18,21%.
C. 15,22%.
D. 15,16%.
Hòa tan hoàn toàn hỗn hợp X gồm Mg và Zn bằng một lượng vừa đủ dung dịch H2SO4 20% (loãng), thu được dung dịch Y. Nồng độ của MgSO4 trong dung dịch Y là 15,22%. Nồng độ phần trăm của ZnSO4 trong dung dịch Y là: A. 15,22% B. 18,21% C. 10,21% D. 15,16%
Đọc tiếp
Hòa tan hoàn toàn hỗn hợp X gồm Mg và Zn bằng một lượng vừa đủ dung dịch H2SO4 20% (loãng), thu được dung dịch Y. Nồng độ của MgSO4 trong dung dịch Y là 15,22%. Nồng độ phần trăm của ZnSO4 trong dung dịch Y là:
A. 15,22%
B. 18,21%
C. 10,21%
D. 15,16%
Đáp án C
Chọn số mol Mg trong hỗn hợp ban đầu là 1. Khi đó gọi số mol Zn ban đầu là x.
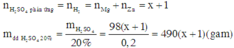
Theo định luật bảo toàn khối lượng ta có:
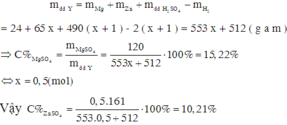
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn hỗn hợp X gồm Mg và Zn bằng một lượng vừa đủ dung dịch H2SO4 20% (loãng), thu được dung dịch Y. Nồng độ của MgSO4 trong dung dịch Y là 15,22%. Nồng độ phần trăm của ZnSO4 trong dung dịch Y là A. 10,21% B. 15,16% C. 18,21% D. 15,22%
Đọc tiếp
Hòa tan hoàn toàn hỗn hợp X gồm Mg và Zn bằng một lượng vừa đủ dung dịch H2SO4 20% (loãng), thu được dung dịch Y. Nồng độ của MgSO4 trong dung dịch Y là 15,22%. Nồng độ phần trăm của ZnSO4 trong dung dịch Y là
A. 10,21%
B. 15,16%
C. 18,21%
D. 15,22%
Hòa tan hoàn toàn hh X gồm Fe và Zn bằng 1 lượng vừa đủ h2so4 10% thu được dd Y và 22,4l h2 ( đktc). nồng đọ của znso4 trong dd Y là 11,6022%. tính khối lượng mỗi kl trong X.
Số mol H2 = 22,4: 22,4 = 1 mol. Goi số mol Fe là x và số mol Zn là y
Fe + H2SO4 → FeSO4 + H2 (1)
Mol x→ x→ x→ x
Zn + H2SO4 → ZnSO4 + H2 (2)
Mol y→ y→ y→ y
=>Số mol H2SO4 = số mol H2 = (x+y) = 1 (*)
Khối lượng dung dịch H2SO4 = 98 . 100/10 = 980 gam
mdd = 56x +65y + 980 – 2 = (56x + 65y +978)
C%(ZnSO4) = 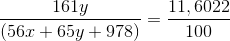
=>15345,857y – 649,7232x = 11346,9516 (**)
Giải hệ PT (*) và (**): x = 0,25; y = 0,75
=>mFe = 0,25.56 = 14g; mZn = 0,75.65 = 48,75g
Đúng 0
Bình luận (0)
Cho 22,7 gam hỗn hợp A gồm Zn và ZnO tác dụng với dung dịch
H2SO4 (dư) thu được 2,24 lít khí (ở đktc).
a. Viết PTHH của phản ứng.
b. Tính khối lượng mỗi chất trong hỗn hợp A.
c. Tính nồng độ mol/l của 200ml dung dịch H2SO4 vừa đủ để hòa tan hoàn toàn 22,7g hỗn hợp A.
a) PTHH : \(Zn+H_2SO_4-->ZnSO_4+H_2\uparrow\) (1)
\(ZnO+H_2SO_4-->ZnSO_4+H_2O\) (2)
b) Theo pthh (1) : \(n_{Zn}=n_{H2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
=> \(m_{Zn}=0,1.65=6,5\left(g\right)\)
=> \(m_{ZnO}=22,7-6,5=16,2\left(g\right)\)
c) \(ZnO=\dfrac{16,2}{81}=0,2\left(mol\right)\)
Theo pthh (1) và (2) : \(\Sigma n_{H2SO4}=n_{Zn}+n_{ZnO}=0,1+0,2=0,3\left(mol\right)\)
=> \(C_{M\left(ddH2SO4\right)}=\dfrac{0,3}{0,1}=1,5M\)
Đúng 0
Bình luận (0)
a) PTHH : Zn+H2SO4−−>ZnSO4+H2↑Zn+H2SO4−−>ZnSO4+H2↑ (1)
ZnO+H2SO4−−>ZnSO4+H2OZnO+H2SO4−−>ZnSO4+H2O (2)
b) Theo pthh (1) : ZnO=16,281=0,2(mol)ZnO=16,281=0,2(mol)
Theo pthh (1) và (2) : ΣnH2SO4=nZn+nZnO=0,1+0,2=0,3(mol)ΣnH2SO4=nZn+nZnO=0,1+0,2=0,3(mol)
=> tích đúng đê
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn hỗn hợp X gồm Mg và Zn bằng một lượng vừa đủ dung dịch H2SO4 20% (loãng), thu được dung dịch Y. Nồng độ của MgSO4 trong dung dịch Y là 15,22%. Nồng độ phần trăm của ZnSO4 trong dung dịch Y gần nhất với giá trị nào sau đây? A. 10,21%. B. 15,16%. C. 18,21%. D. 15,22%.
Đọc tiếp
Hòa tan hoàn toàn hỗn hợp X gồm Mg và Zn bằng một lượng vừa đủ dung dịch H2SO4 20% (loãng), thu được dung dịch Y. Nồng độ của MgSO4 trong dung dịch Y là 15,22%. Nồng độ phần trăm của ZnSO4 trong dung dịch Y gần nhất với giá trị nào sau đây?
A. 10,21%.
B. 15,16%.
C. 18,21%.
D. 15,22%.