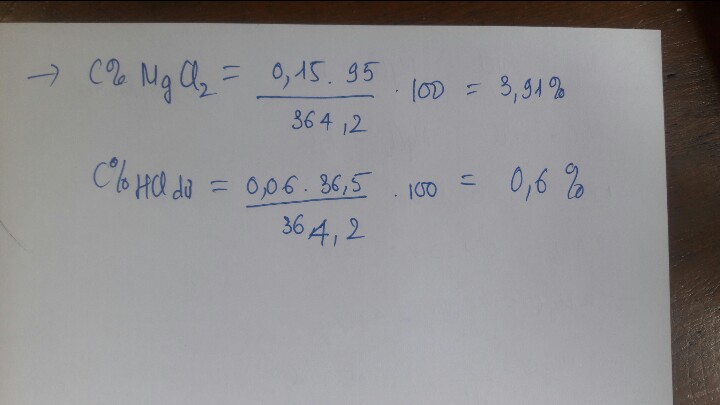cho dung dịch ch3cooh 9% tác dụng hết với 8,4g hỗn hợp A gồm Mg và MgO thu được dung dịch B và 2,24 lít khí C
a, tính % khối lượng các chất
b, Tính C% dung dịch B

Những câu hỏi liên quan
Cho 10g hỗn hợp gồm MgO và Ca tác dụng hết với 390,2g dung dịch HCl 7,3%, thu được 2,24 lít khí ở đktc.
a. Tính phần trăm khối lượng của MgO và Ca trong hỗn hợp.
b. Tính nồng độ phần trăm các chất trong dung dịch sau phản ứng.
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\)
\(Ca+2HCl\rightarrow CaCl_2+H_2\)
0,1 0,1 ( mol )
\(\rightarrow\left\{{}\begin{matrix}\%m_{Ca}=\dfrac{0,1.40}{10}.100=40\%\\\%m_{MgO}=100\%-40\%=60\%\end{matrix}\right.\)
\(\left\{{}\begin{matrix}C\%_{CaCl_2}=\dfrac{0,1.111}{10+390,2-0,1.2}.100=2,775\%\\C\%_{MgO}=\dfrac{4}{10+390,2-0,1.2}.100=1\%\end{matrix}\right.\)
Đúng 3
Bình luận (2)
Cho 4,4 g hỗn hợp gồm Mg và MgO tác dụng vừa đủ với dung dịch HCl 7,3% thu được 2,24 lít khí (đkc) A) viết các phương trình phản ứng xảy ra b) tính khối lượng mỗi chất trong hỗn hợp ban đầu C) tính khối lượng dung dịch HCl phản ứng D) tính c% của dung dịch muối thu được sau phản ứng Ghi rõ ra để mình biết các câu để mình ghi nha
Cho 4,4 gam hỗn hợp X gồm Mg và MgO tác dụng với dung dịch HCl 3,65% (dư 20% so với lượng phản ứng) thu được dung dịch Y và 2,24 lít khí H2 (đktc). (a) Viết PTHH xảy ra và tính phần trăm khối lượng mỗi chất trong hỗn hợp X. (b) Tính nồng độ phần trăm các chất có trong dung dịch Y.
Cho 10,4 g hỗn hợp gồm Mg và MgO tác dụng với axit H2SO4 loãng dư thấy giải phóng 2,24 lít khí (đktc) và dung dịch A.
a. Tính khối lượng mỗi chất trong hỗn hợp ban đầu.
b. Cho dung dịch A tác dụng với dụng NaOH dư được kết tủa B. Lọc lấy kết tủa B nung trong không khí tới khối lượng không đổi được chất rắn C. Tính khối lượng chất rắn C.
a,\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: Mg + H2SO4 → MgSO4 + H2
Mol: 0,1 0,1 0,1
PTHH: MgO + H2SO4 → MgSO4 + H2O
Mol: 0,2 0,2
\(m_{Mg}=0,1.24=2,4\left(g\right)\)
\(m_{MgO}=10,4-2,4=8\left(g\right)\Rightarrow n_{MgO}=\dfrac{8}{40}=0,2\left(mol\right)\)
b,\(n_{MgSO_4}=0,1+0,2=0,3\left(mol\right)\)
PTHH: MgSO4 + 2NaOH → Mg(OH)2 ↓ + Na2SO4
Mol: 0,3 0,3
PTHH: Mg(OH)2 ---to→ MgO + H2O
Mol: 0,3 0,3
\(\Rightarrow m_{MgO}=0,3.40=12\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 14g hỗn hợp Mg và MgO tác dụng với 200g dung dịch H2SO4, sau phản ứng thu được 5,6 lít khí (đktc). a/ Tính % về khối lượng các chất trong hỗn hợp ? b/ Tính nồng độ % dung dịch H2SO4 cần dùng ?
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25(mol)\\ Mg+H_2SO_4\to MgSO_4+H_2\\ MgO+H_2SO_4\to MgSO_4+H_2O\\ \Rightarrow n_{Mg}=0,25(mol)\\ a,\begin{cases} \%_{Mg}=\dfrac{0,25.24}{14}.100\%=42,86\%\\ \%_{MgO}=100\%-42,86\%=57,14\% \end{cases}\\ b,n_{MgO}=\dfrac{14-0,25.24}{40}=0,2(mol)\\ \Rightarrow \Sigma n_{H_2SO_4}=0,2+0,25=0,45(mol)\\ \Rightarrow C\%_{H_2SO_4}=\dfrac{0,45.98}{200}.100\%=22,05\%\)
Đúng 1
Bình luận (0)
Cho 4,4 gam hỗn hợp gồm Mg và MgO tác dụng với dung dịch HCl dư, thu được 2,24 lít khí (đktc)
a. Viết các PTHH xảy ra?
b. Tính thành phần trăm mỗi chất trong hỗn hợp trên?
c. Phải dùng bao nhiêu ml dung dịch HCl 2M cho phản ứng?
a, PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
b, Giả sử: \(\left\{{}\begin{matrix}n_{Mg}=x\left(mol\right)\\n_{MgO}=y\left(mol\right)\end{matrix}\right.\)
⇒ 24x + 40y = 4,4 (1)
Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Mg}=x\left(mol\right)\)
⇒ x = 0,1 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,1.24}{4,4}.100\%\approx54,54\%\\\%m_{MgO}\approx45,46\%\end{matrix}\right.\)
c, Theo PT: \(\Sigma n_{HCl}=2n_{Mg}+2n_{MgO}=0,3\left(mol\right)\)
\(\Rightarrow V_{HCl}=\dfrac{0,3}{2}=0,15\left(l\right)=150\left(ml\right)\)
Bạn tham khảo nhé!
Đúng 7
Bình luận (0)
Cho 32g hỗn hợp gồm Mg và MgO tác dụng vừa đủ hết với dung dịch HCL 7,3%. Sau phản ứng ta thu được 22,4lít khí ở đktc.
a. tính phần trăm khối lượng mỗi chất trong hỗn hợp ban đầu.
b. Tính khối lượng dung dịch hcl cần dùng cho các phản ứng trên.
c. Tính nồng độ phần trăm của chất có trong dung dịch sau khi phản ứng kết thúc.
cho H=1. Cl=35,5. Al =27. O=16. Na=23. S=32
Xem chi tiết
PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\) (1)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\) (2)
a) Ta có: \(n_{H_2}=\dfrac{22,4}{22,4}=1\left(mol\right)=n_{Mg}\) \(\Rightarrow m_{Mg}=1\cdot24=24\left(g\right)\)
\(\Rightarrow\%m_{Mg}=\dfrac{24}{32}\cdot100\%=75\%\) \(\Rightarrow\%m_{MgO}=25\%\)
b) Theo 2 PTHH: \(\left\{{}\begin{matrix}n_{HCl\left(1\right)}=2n_{Mg}=2mol\\n_{HCl\left(2\right)}=2n_{MgO}=2\cdot\dfrac{32-24}{40}=0,4mol\end{matrix}\right.\)
\(\Rightarrow\Sigma n_{HCl}=2,4mol\) \(\Rightarrow m_{ddHCl}=\dfrac{2,4\cdot36,5}{7,3\%}=1200\left(g\right)\)
c) Theo PTHH: \(\Sigma n_{MgCl_2}=\dfrac{1}{2}\Sigma n_{HCl}=1,2mol\)
\(\Rightarrow\Sigma m_{MgCl_2}=1,2\cdot95=114\left(g\right)\)
Mặt khác: \(m_{H_2}=1\cdot2=2\left(g\right)\)
\(\Rightarrow m_{dd}=m_{hh}+m_{ddHCl}-m_{H_2}=1230\left(g\right)\)
\(\Rightarrow C\%_{MgCl_2}=\dfrac{114}{1230}\cdot100\%\approx9,27\%\)
Đúng 2
Bình luận (0)
Hoà tan hết 13 gam hỗn hợp bột A gồm Mg và Na2CO3 trong Vml dung dịch H2SO4 1M (loãng) thu được 4,48 lít hỗn hợp khí B (đktc) và dung dịch C. a) Tính % khối lượng mỗi chất có trong A. b) Cho dung dịch C tác dụng với dung dịch Ba(OH)2 dư, lọc kết tủa nung đến khối lượng không đổi được 62,25 gam chất rắn. Tính V.
a)
Gọi số mol Mg, Na2CO3 là a,b (mol)
=> 24a + 106.b = 13 (1)
\(n_{H_2}+n_{CO_2}=\dfrac{4,48}{33,4}=0,2\left(mol\right)\)
PTHH: Mg + H2SO4 --> MgSO4 + H2
______a------>a------------>a------->a________(mol)
Na2CO3 + H2SO4 --> Na2SO4 + CO2 + H2O
__b---------->b----------->b------>b______________(mol)
=> a + b = 0,2 (2)
(1)(2) => \(\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%Mg=\dfrac{0,1.24}{13}100\%=18,46\%\\\%Na_2CO_3=100\%-18,46\%=81,54\%\end{matrix}\right.\)
b)
PTHH: \(Ba\left(OH\right)_2+H_2SO_4->BaSO_4\downarrow+2H_2O\)
_________________k------------>k_______________(mol)
\(Ba\left(OH\right)_2+MgSO_4->BaSO_4\downarrow+Mg\left(OH\right)_2\downarrow\)
____________0,1---------->0,1---------->0,1_________(mol)
\(Ba\left(OH\right)_2+Na_2SO_4->BaSO_4\downarrow+2NaOH\)
____________0,1-------->0,1____________________(mol)
\(Mg\left(OH\right)_2\underrightarrow{t^o}MgO+H_2O\)
_0,1---------->0,1______________________________(mol)
=> \(\left\{{}\begin{matrix}n_{BaSO_4}=k+0,2\\n_{MgO}=0,1\end{matrix}\right.\)
=> \(233.\left(k+0,2\right)+40.0,1=62,25\)
=> k = 0,05 (mol)
=> nH2SO4 = 0,1 + 0,1 + 0,05 = 0,25 (mol)
=> \(V_{dd}=\dfrac{0,25}{1}=0,25\left(l\right)=250ml\)
Đúng 2
Bình luận (0)
1) Cho 4,4 gam hỗn hợp gồm Mg và MgO tác dụng với dung dịch HCl (dư) thu được 2,24 lít khí (đktc).
1. Viết các phương trình phản ứng xảy ra.
2. Tính khối lượng của mỗi chất trong hỗn hợp.
3. Phải dùng bao nhiêu ml dung dịch HCl 2M đủ để hoà tan 4,4 gam hỗn hợp
1)
$MgO + 2HCl to MgCl_2 + H_2O$
$Mg + 2HCl \to MgCl_2 + H_2$
2)
$n_{Mg} = n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol)$
$m_{Mg} = 0,1.24 = 2,4(gam)$
$m_{MgO} = 4,4 - 2,4 = 2(gam)$
3)
$n_{HCl} = 2n_{Mg} + 2n_{MgO} = 0,1.2 + \dfrac{2}{40}.2 = 0,3(mol)$
$V_{dd\ HCl} = \dfrac{0,3}{2} = 0,15(lít) = 150(ml)$
Đúng 2
Bình luận (0)