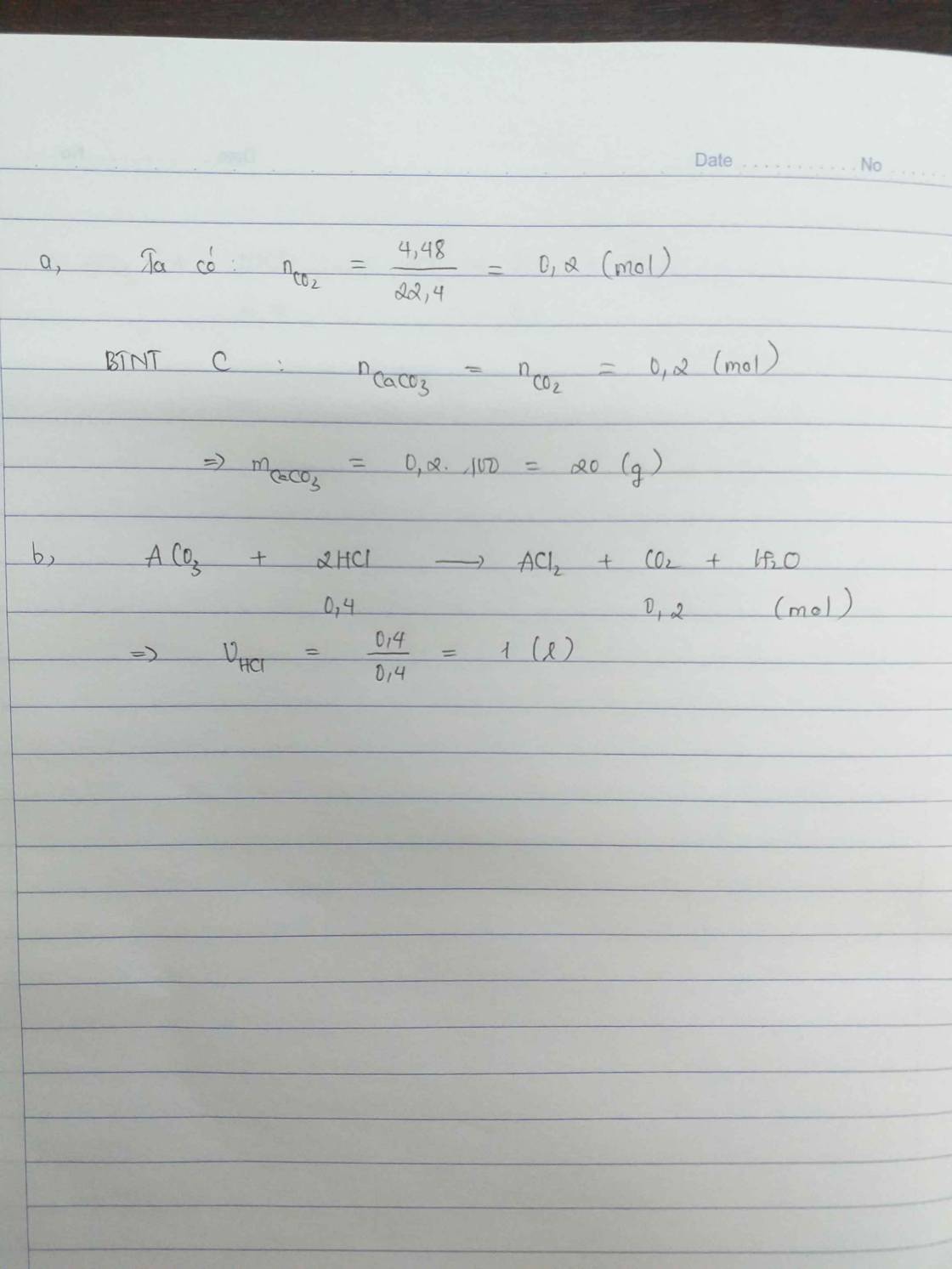Cho 0,5 mol hỗn hợp hai muối cacbonat của kim loại hoá trị II tác dụng hết với dd HCl. Dẫn khí thoát ra vào dd Ca(OH)2 dư thì khối lượng kết tủa thu được là: D. 60 gam C. 55 gam A. 50g B. 45 gam

Những câu hỏi liên quan
a) Hào tan hoàn toàn 0,1 mol hỗn hợp Na2CO3 và KHCO3 vào dd HCL dẫn khí thu đc vào bình đựng dd Ca(OH)2 dư thì lượng kết tủa tạo ra là bao nhiêu gam
b) Cho 14,5 g hỗn hợp Mg,Zn và Fe tác dụng hết với dd H2SO4 loãng thoát ra 6,72 lít H2 ở đktc. Cô cạn dd sau pứ, khối lượng muối khan là bao nhiêu gam?
cho 0,5 mol hh 2 muối cacbonat của kim loại hóa trị 2 tác dụng hết với dd HCl . Dẫn khí thoát ra vào dd Ca(OH)2 dư thì khối lượng kết tủa thu được là:
A. 50g
B. 45g
C. 55g
D. 60g
Gọi công thức chung của 2 muối là M CO3
ta có pthh: M CO3+2HCl-> M Cl2+ H2O+ CO2 (1)
CO2+ Ca(OH)2-> CaCO3+H2O (2)
Theo pt (1): nCO2=n muối= 0,5 mol
Theo pt (2); n CaCO3= nCO2= 0,5 mol
Suy ra: mCaCO3= 0,5.100=50g
Suy ra: đáp án A
Đúng 0
Bình luận (0)
Cho 1 mol hỗn hợp gồm NaCl và Na2CO3 tác dụng hết với dd HCl. Khí thoát ra sau phản ứng được dẫn vào dung dịch Ca(OH)2 dư thu được 50g kết tủa. Tính Tỉ lệ mol của 2 muối trong hỗn hợp ban đầu
\(n_{CaCO_3}=\dfrac{50}{100}=0,5\left(mol\right)\)
PTHH: CO2 + Ca(OH)2 ---> CaCO3↓ + H2O
0,5<-----------------------0,5
Na2CO3 + 2HCl ---> 2NaCl + CO2↑ + H2O
0,5<---------------------------------0,5
=> nNaCl = 1 - 0,5 = 0,5 (mol)
=> nNa2CO3 : nNaCl = 0,5 : 0,5 = 1 : 1
Đúng 2
Bình luận (0)
Cho A gam hỗn hợp Bari Cacbonat và Canxi Cacbonat tác dụng với V lít dd HCL 0,4M thấy giải phóng 4,48 lít CO2 (đktc), dẫn khí thu được vào dung dịch Ca(OH)2 dư. Tính
a/ Khối lượng kết tủa thu được
b/ Thể tích dd HCL cần dùng
\(a/n_{CO_2}=\dfrac{4,48}{22,4}=0,2mol\\ CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\\ n_{CO_2}=n_{CaCO_3}=0,2mol\\ m_{CaCO_3}=0,2.100=20g\\ b/BTNT\left(O\right):2n_{CO_2}=n_{H_2O}\\ \Rightarrow n_{H_2O}=0,2.2=0,4mol\\ BTNT\left(H\right):2n_{H_2O}=n_{HCl}\\ n_{HCl}=0,4.2=0,8mol\\ V_{HCl}=\dfrac{0,8}{0,4}=2l\)
Đúng 0
Bình luận (3)
Nung m gam hỗn hợp X gồm hai muối cacbonat trung tính của 2 kim loại A và B đều có hóa trị 2. Sau một thời gian thu được 3,36 lít CO2 đktc và còn lại hỗn hợp rắn Y. Cho Y tác dụng hết với dung dịch HCl dư rồi cho khí thoát ra hấp thụ hết bởi dung dịch Ca(OH)2 dư thu được 15 gam kết tủa, phần dung dịch đem cô cạn thu được 32,5 gam hỗn hợp muối khan. Giá trị của m là: A. 30,8 gam B. 29,2 gam C. 29,8 gam D. 30,2 gam
Đọc tiếp
Nung m gam hỗn hợp X gồm hai muối cacbonat trung tính của 2 kim loại A và B đều có hóa trị 2. Sau một thời gian thu được 3,36 lít CO2 đktc và còn lại hỗn hợp rắn Y. Cho Y tác dụng hết với dung dịch HCl dư rồi cho khí thoát ra hấp thụ hết bởi dung dịch Ca(OH)2 dư thu được 15 gam kết tủa, phần dung dịch đem cô cạn thu được 32,5 gam hỗn hợp muối khan. Giá trị của m là:
A. 30,8 gam
B. 29,2 gam
C. 29,8 gam
D. 30,2 gam
Đáp án B
Gọi công thức trung bình của hai muối ACO3 và BCO3 là MCO3
MCO3 → MO + CO2
n C O 2 = 3,36 /22,4 = 0,15 mol → n M C O 3 = 0,15 mol
Hỗn hợp Y gồm MCO3 dư và MO
MCO3 + 2HCl → MCl2 + CO2 + H2O
MO + 2HCl → MCl2 + H2O
CO2 + Ca(OH)2 dư → CaCO3 ↓ + H2O
n C a C O 3 = 15/100 = 0,15 mol
→ n M C O 3 dư = 0,15 mol
n M C O 3 ban đầu = 0,15 + 0,15 = 0,3 mol
Bảo toàn kim loại M có:
n M C O 3 = n M C l 2 = 0,3 (mol)
Bảo toàn khối lượng có:
m M C O 3 = m M C l 2 - 0,3.(71- 60) = 29,2 (gam)
Đúng 0
Bình luận (0)
Cho từ từ dung dịch HCl có pH 0 vào dung dịch chứa 5,25 gam hỗn hợp muối cacbonat của 2 kim loại kiềm kế tiếp đến khi có 0,015 mol khí thoát ra thì dừng lại. Cho dung dịch thu được tác dụng với dung dịch Ca(OH)2 dư sinh ra 3 gam kết tủa. Công thức của 2 muối và thể tích dung dịch HCl đã dùng là A. Li2CO3 và Na2CO3 ; 0,03 lít. B. Li2CO3 và Na2CO3 ; 0,06 lít. C. Na2CO3 và K2CO3 ; 0,03 lít. D. Na2CO3 và K2CO3 ; 0,06 lít.
Đọc tiếp
Cho từ từ dung dịch HCl có pH = 0 vào dung dịch chứa 5,25 gam hỗn hợp muối cacbonat của 2 kim loại kiềm kế tiếp đến khi có 0,015 mol khí thoát ra thì dừng lại. Cho dung dịch thu được tác dụng với dung dịch Ca(OH)2 dư sinh ra 3 gam kết tủa. Công thức của 2 muối và thể tích dung dịch HCl đã dùng là
A. Li2CO3 và Na2CO3 ; 0,03 lít.
B. Li2CO3 và Na2CO3 ; 0,06 lít.
C. Na2CO3 và K2CO3 ; 0,03 lít.
D. Na2CO3 và K2CO3 ; 0,06 lít.
Đáp án D
Thí nghiệm 1: Khi cho từ từ dung dịch HCl vào muối cacbonat xảy các phương trình theo thứ tự sau:
H+ + CO32- → HCO3- (1)
Sau khi (1) xảy ra nếu H+ dư thì HCO3- + H+ → CO2 + H2O (2)
Thí nghiệm 2: Nhận thấy khi cho dung dịch Ca(OH)2 vào dung dịch thu được của thí nghiệm 1 thấy tạo kết tủa → trong dung dịch còn ion HCO3- : 0,03 mol ( HCO3- + OH- → CO32- )
Bảo toàn nguyên tố C ta có : nmuối = nHCO3- + nCO2 = 0,03 + 0,015 = 0,045 mol
→ Mtb muối =
5
,
25
0
,
045
= 116,67→ 2 muối cacbonat của kim loại kiềm kế tiếp là Na2CO3 và K2CO3
Ta có nH+ = nCO32- + nCO2 = 0,045 + 0,015 = 0,06 mol
Dung dịch HCl có pH = 0 → CMHCl = 1 M → VHCl = 0,06 lít
Đúng 0
Bình luận (0)
: Cho 8,7 gam hỗn hợp X gồm hai muối cacbonat của hai kim loại nằm kế tiếp nhau trong nhóm IA, tác dụng với dung dịch HCl dư, toàn bộ khí CO2 sinh ra được dẫn vào dung dịch nước vôi trong, thu được 7 gam kết tủa. Khối lượng của muối cacbonat có nguyên tử khối lớn hơn trong X là: A. 3,46 gam. B. 4,13 gam. C. 3,18 gam. D. 5,52 gam.
Đọc tiếp
: Cho 8,7 gam hỗn hợp X gồm hai muối cacbonat của hai kim loại nằm kế tiếp nhau trong nhóm IA, tác dụng với dung dịch HCl dư, toàn bộ khí CO2 sinh ra được dẫn vào dung dịch nước vôi trong, thu được 7 gam kết tủa. Khối lượng của muối cacbonat có nguyên tử khối lớn hơn trong X là:
A. 3,46 gam. B. 4,13 gam. C. 3,18 gam. D. 5,52 gam.
Cho 7,2 gam hỗn hợp X gồm hai muối cacbonat của hai kim loại kế tiếp nhau M, R trong nhóm IIA (M R) tác dụng với dung dịch HCl dư. Hấp thụ toàn bộ khí CO2 sinh ra vào 450 ml dung dịch Ba(OH)2 0,2M thu được 15,76 gam kết tủa. Khối lượng mol lớn nhất có thể đạt của M là A. 9 (Be). B. 24 (Mg). C. 40 (Ca). D. 88 (Sr).
Đọc tiếp
Cho 7,2 gam hỗn hợp X gồm hai muối cacbonat của hai kim loại kế tiếp nhau M, R trong nhóm IIA (M < R) tác dụng với dung dịch HCl dư. Hấp thụ toàn bộ khí CO2 sinh ra vào 450 ml dung dịch Ba(OH)2 0,2M thu được 15,76 gam kết tủa. Khối lượng mol lớn nhất có thể đạt của M là
A. 9 (Be).
B. 24 (Mg).
C. 40 (Ca).
D. 88 (Sr).
Đáp án B
7,2 gam MCO3 + HCl → CO2 + 0,09 mol Ba(OH)2 → 0,08 mol BaCO3↓
• CO2 + Ba(OH)2 → BaCO3↓ + H2O(*)
BaCO3 + CO2 + H2O → Ba(HCO3)2 (**)
Theo (*) nCO2(*) = 0,09 mol; nBaCO3 (*) = 0,09 mol
Theo (**) nBaCO3 (**) dư = 0,08 mol → nBaCO3 (**) phản ứng = 0,09 - 0,08 = 0,01 mol
→ nCO2 (**) = 0,01 mol → ∑nCO2 = 0,1 mol
• MCO3 + 2HCl → MCl2 + CO2 + H2O
nMCO3 = nCO2 = 0,1 mol → MMCO3 = 7,2 : 0,1 = 72 → MM = 12 → Be và Mg (9 < 20 < 24)
Đúng 0
Bình luận (0)
Trong bình kín (không có không khí) chứa 65,76 gam hỗn hợp A gồm Al, Al2O3, Fe3O4 và FeCO3. Nung bình ở nhiệt độ cao đến khi phản ứng xảy ra hoàn toàn. Khí thoát ra khỏi bình được dẫn qua dung dịch Ca(OH)2 dư thu được 24,0 gam kết tủa. Hỗn hợp rắn B còn lại trong bình được chia làm 2 phần bằng nhau + Phần 1 cho vào dung dịch NaOH dư thấy thoát ra 0,06 mol khí H2. Sục khí CO2 đến dư vào dung dịch sau phản ứng thu được 21,84 gam kết tủa. + Phần 2 tác dụng hết với dung dịch chứa H2SO4 và 0,23 mol H...
Đọc tiếp
Trong bình kín (không có không khí) chứa 65,76 gam hỗn hợp A gồm Al, Al2O3, Fe3O4 và FeCO3. Nung bình ở nhiệt độ cao đến khi phản ứng xảy ra hoàn toàn. Khí thoát ra khỏi bình được dẫn qua dung dịch Ca(OH)2 dư thu được 24,0 gam kết tủa. Hỗn hợp rắn B còn lại trong bình được chia làm 2 phần bằng nhau
+ Phần 1 cho vào dung dịch NaOH dư thấy thoát ra 0,06 mol khí H2. Sục khí CO2 đến dư vào dung dịch sau phản ứng thu được 21,84 gam kết tủa.
+ Phần 2 tác dụng hết với dung dịch chứa H2SO4 và 0,23 mol HNO3 thu được dung dịch Z chỉ chứa các muối sunfat của kim loại có khối lượng 93,36 gam và hỗn hợp khí gồm a mol NO và b mol N2O. Tỉ lệ a:b là
A. 3,75.
B. 3,25
C. 3,50.
D. 3,45.
Chọn đáp án A
nCO2 = 0,24 mol. Bảo toàn khối lượng: mB = 65,76 - 0,24 × 44 = 55,2(g).
► Xét 1 phần ⇒ mB = 27,6(g). Có H2 ⇒ Al dư ⇒ B gồm Al dư, Al2O3 và Fe.
⇒ nAl = 0,06 ÷ 1,5 = 0,04 mol || nAl(OH)3 = 0,28 mol ⇒ nAl2O3 = 0,12 mol.
→ m b nFe = 0,255 mol ⇒ nSO42– = (93,36 - 0,28 × 27 - 0,255 × 56) ÷ 96 = 0,745 mol.
⇒ nH2SO4 = 0,745 mol ⇒ ∑nH+ = 0,745 × 2 + 0,23 = 1,72 mol.
● ∑nH+ = 4nNO + 10nN2O + 2nO ⇒ 4a + 10b = 1. Bảo toàn nguyên tố Nitơ:
a + 2b = 0,23 mol ||⇒ giải hệ có: a = 0,15 mol; b = 0,04 mol.
⇒ a : b = 3,75 ⇒ chọn A.
Đúng 0
Bình luận (0)