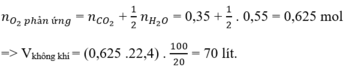Đốt cháy hoàn toàn 4,48 lit khí Etilen trong không khí. Hãy xác định:
a. Thể tích Không khí đã dùng
b. Thể tích khí CO2 và hơi nước thu được
Bài 16: Cho 4,48 lít khí etilen tác dụng hoàn toàn với 160g dung dịch Br2 15%. Hãy tính:
a) Khối lượng đibrom etan thu được sau phản ứng?
b) Đốt cháy hoàn toàn lượng khí etilen dư trong không khí. Hãy tính:
-Thể tích khí CO2 sinh ra?
-Thể tích không khí cần dùng?
Biết các thể tích khí đo ở đktc.
cho mk xin gấp đáp án vs ạkTT
a)
$n_{Br_2} = \dfrac{160.15\%}{160} = 0,15(mol)$
$C_2H_4 + Br_2 \to C_2H_4Br_2$
Ta thấy : $n_{C_2H_4} = 0,2 > n_{Br_2} = 0,15$ nên $C_2H_4$ dư
$n_{C_2H_4Br_2} = n_{Br_2} = 0,15(mol) \Rightarrow m_{C_2H_4Br_2} = 0,15.188 = 28,2(gam)$
b) $n_{C_2H_4\ dư} = 0,2 - 0,15 = 0,05(mol) \Rightarrow V_{C_2H_4} = 0,05.22,4 = 1,12(lít)$
$C_2H_4 + 3O_2 \xrightarrow{t^o} 2CO_2 + 2H_2O$
Theo PTHH :
$V_{CO_2} =2 V_{C_2H_4} = 2,24(lít)$
$V_{O_2} = 3V_{C_2H_4} = 3,36(lít) \Rightarrow V_{kk} = 5V_{O_2} = 16,8(lít)$
Đốt cháy hoàn toàn V etilen thu đuoecj 4,5g nước . Hãy tính : a, thể tích V etilen đã đốt cháy b, tính thể tích không khí cần dùng ở đktc ( biết O2 chiếm 20% thể túch không khí )
a)
\(n_{H_2O}=\dfrac{4,5}{18}=0,25\left(mol\right)\)
PTHH: C2H4 + 3O2 --to--> 2CO2 + 2H2O
0,125<-0,375<-------------0,25
=> V = 0,125.22,4 = 2,8 (l)
b) VO2 = 0,375.22,4 = 8,4 (l)
=> Vkk = 8,4 : 20% = 42 (l)
đốt cháy hoàn toàn 5,6 lít khí etilen(đktc)thu được khí co2 và nước. a)Hãy viết các phương trình hóa học xảy ra? b)Tính thể tích không khí cần dùng cho phản ứng cháy biết oxi chiếm 20% c)Tính khối lượng khí co2 thu được
\(n_{C_2H_4}=\dfrac{5.6}{22.4}=0.25\left(mol\right)\)
\(C_2H_4+3O_2\underrightarrow{^{t^0}}2CO_2+2H_2O\)
\(0.25.....0.75.......0.5\)
\(V_{kk}=5V_{O_2}=5\cdot0.75\cdot22.4=84\left(l\right)\)
\(m_{CO_2}=0.5\cdot44=22\left(g\right)\)
Bài 21: Đốt cháy hoàn toàn một lượng rượu etylic trong không khí, thu được 4,48 lít khí CO2 .
a) Tính khối lượng rượu đã cháy?
b) Thể tích không khí c hat a n dùng (biết oxi chiếm 20% thể tích không khí, thể tích các chất khí đều đo ở đktc)
c) Để có được lượng rượu trên cần lên men bao nhiêu gam glucozo?
\(n_{CO_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(C_2H_5OH+3O_2\underrightarrow{t^o}2CO_2+3H_2O\)
0,2 0,6 0,4 0,6
a)\(m_{C_2H_5OH}=0,2\cdot46=9,2g\)
b)\(V_{O_2}=0,6\cdot22,4=13,44l\)
\(\Rightarrow V_{kk}=5V_{O_2}=5\cdot13,44=67,2l\)
Khí A có tỉ khối đối với khí oxi là 1,8125 và trong A có 82,76 % C còn lại la H
a) Hãy xác định công thức phân tử của A
b) tính thể tích không khí cần dùng để đốt cháy hoàn toàn 4,48 lít khí A. Sau phản ứng thu được bao nhiêu lít khí CO2. Biết các khí đó ở đktc
\(M_A=1,8125.32=58\left(\dfrac{g}{mol}\right)\\ \rightarrow\left\{{}\begin{matrix}m_C=58.82,76\%=48\left(g\right)\\m_H=58-48=10\left(g\right)\end{matrix}\right.\\ \rightarrow\left\{{}\begin{matrix}n_C=\dfrac{48}{12}=4\left(mol\right)\\n_H=\dfrac{10}{1}=10\left(mol\right)\end{matrix}\right.\\ CTHH:C_4H_{10}\)
\(n_{C_4H_{10}}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: 2C4H10 + 13O2 --to--> 8CO2 + 10H2O
0,2 0,8
=> VCO2 = 0,8.22,4 = 17,92 (l)
Đốt cháy khí Metan (CH4) trong không khí tạo thành 4,4 gam khí CO2 và hơi nước. a/ Tính khối lượng khí metan đã dùng. b/ Tính thể tích hơi nước thu được (đktc). c/ Tính thể tích khí O2 đã tham gia phản ứng (đktc). d/ Tính thể tích không khí đã dùng (đktc). Biết rằng oxi chiếm 20% thể tích không khí câu cuối cùng :< mik lú luôn
\(n_{CO_2}=\dfrac{4.4}{44}=0.1\left(mol\right)\)
\(CH_4+2O_2\underrightarrow{^{^{t^0}}}CO_2+2H_2O\)
\(0.1.......0.2........0.1..........0.2\)
\(m_{CH_4}=0.1\cdot16=1.6\left(g\right)\)
\(V_{H_2O}=0.2\cdot22.4=4.48\left(l\right)\)
\(V_{kk}=5V_{O_2}=5\cdot0.2\cdot22.4=22.4\left(l\right)\)
Đốt cháy hoàn toàn 11,2 lit khí etilen ( C2H4 ) tạo ra sản phẩm CO2 và H2O
a) tính thể tích khí oxi cần dùng ở phản ứng trên
b) tính thể tích không khí cần dùng, biết khí oxi chiếm ⅕ thể tích không khí. Biết thể tích khi ở điều kiện tiêu chuẩn
a, \(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
Ta có: \(n_{C_2H_4}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
Theo PT: \(n_{O_2}=3n_{C_2H_4}=1,5\left(mol\right)\Rightarrow V_{O_2}=1,5.22,4=33,6\left(l\right)\)
b, \(V_{kk}=\dfrac{V_{O_2}}{20\%}=168\left(l\right)\)
Đốt cháy hoàn toàn 11,2 lit khí etilen ( C2H4 ) tạo ra sản phẩm CO2 và H2O
a) tính thể tích khí oxi cần dùng ở phản ứng trên
b) tính thể tích không khí cần dùng, biết khí oxi chiếm s thể tích không khí. Biết thể tích khi ở điều kiện tiêu chuẩn
PTHH: \(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
\(n_{C_2H_4}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
Theo PTHH: \(n_{O_2}=3.n_{C_2H_4}=3.0,5=1,5\left(mol\right)\)
=> \(V_{O_2\left(đktc\right)}=1,5.22,4=33,6\left(l\right)\)
câu b oxi chiếm bao nhiêu của kk vậy bạn
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là:
A. 70,0 lít
B. 78,4 lít
C. 84,0 lít
D. 56,0 lít
Đáp án A
Hỗn hợp khí gồm CH4, C2H6 và C3H8 là các hidrocacbon.
Mà khi đốt cháy 1 hidrocacbon bất kì ta luôn có: