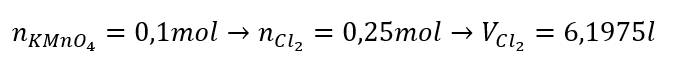Cho 15,8g KMnO4 tác dụng với dung dịch HCl đặc, tính thể tích khí Cl2 thu được ở đktc, biết quá trình thu khí Cl2 hao hụt 10 phần trăm

Những câu hỏi liên quan
Cho 15.8g KMnO4 tác dụng hoàn toàn với dung dịch HCL đậm đặc . Tính thể tích khí Cl2 thu được ở đkc
\(n_{KMnO_4}=\dfrac{15,8}{158}=0,1\left(mol\right)\\ 2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\\ n_{Cl_2}=\dfrac{5}{2}.0,1=0,25\left(mol\right)\\ V_{Cl_2\left(đkc\right)}=0,25.24,79=6,1975\left(l\right)\)
Đúng 0
Bình luận (0)
Cho 15.8g KMnO4 tác dụng hoàn toàn với dung dịch HCL đậm đặc . Tính thể tích khí Cl2 thu được ở đkc
Cho 15,8g KMn O 4 tác dụng hết với dung dịch HCl đậm đặc. Giả sử hiệu suất phản ứng là 100% thì thể tích (đktc) khí Cl 2 thu được là
A. 5,6 lít B. 0,56 lít
C. 2,8 lít D. 0,28 lít
Bài 8. a) Cho 200ml dung dịch HCl 2M tác dụng với lượng dư KMnO4 thu được dung dịch A, V1 lít khí Cl2 (đktc). b) Cho 200ml dung dịch HCl 2M tác dụng với lượng dư MnO2 thu được dung dịch B, V2 lít khí Cl2 (đktc). - Viết PTHH của phản ứng xảy ra. - Tính thể tích khí Cl2 thu được (V1, V2). Mọi người giúp mình với ạ mình thật sự rất cần
- PT: a, \(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\) (1)
\(MnO_2+4HCl_đ\underrightarrow{t^o}MnCl_2+Cl_2+2H_2O\) (2)
- Ta có: \(n_{HCl\left(1\right)}=n_{HCl\left(2\right)}=0,2.2=0,4\left(mol\right)\)
Theo PT (1): \(n_{Cl_2}=\dfrac{5}{16}n_{HCl\left(1\right)}=0,125\left(mol\right)\Rightarrow V_1=0,125.22,4=2,8\left(l\right)\)
(2): \(n_{Cl_2\left(2\right)}=\dfrac{1}{4}n_{HCl\left(2\right)}=0,1\left(mol\right)\Rightarrow V_2=0,1.22,4=2,24\left(l\right)\)
Đúng 2
Bình luận (0)
Nung 94.8g KMnO4 a)Tính thể tích khí oxi thu được ở đktc nếu quá trình hao hụt 10%b)Dùng thể tích oxi thu được ở phần a để đốt cháy nhôm, tính khối lượng sản phẩm thu được
PTHH: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
a) Ta có: \(n_{KMnO_4}=\dfrac{94,8}{158}=0,6\left(mol\right)\)
\(\Rightarrow n_{O_2\left(lýthuyết\right)}=0,3\left(mol\right)\) \(\Rightarrow n_{O_2\left(thực\right)}=0,3\cdot90\%=0,27\left(mol\right)\)
\(\Rightarrow V_{O_2\left(thực\right)}=0,27\cdot22,4=6,048\left(l\right)\)
b) PTHH: \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
Theo PTHH: \(n_{Al_2O_3}=\dfrac{2}{3}n_{O_2}=0,18\left(mol\right)\)
\(\Rightarrow m_{Al_2O_3}=0,18\cdot102=18,36\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 69,6 gam MnO2 tác dụng với HCl đặc, dư.(H%90%). Dẫn toàn bộ lượng khí sinh ra vào 500 ml dung dịch NaOH 4M thu được dung dịch A. Thể tích khí Cl2 thu được ở đktc sau phản ứng là: A. 17,92 B. 16,128 C. 19,9 D. 13,44
Đọc tiếp
Cho 69,6 gam MnO2 tác dụng với HCl đặc, dư.(H%=90%). Dẫn toàn bộ lượng khí sinh ra vào 500 ml dung dịch NaOH 4M thu được dung dịch A. Thể tích khí Cl2 thu được ở đktc sau phản ứng là:
A. 17,92
B. 16,128
C. 19,9
D. 13,44
Cho 34,175 gam hỗn hợp KMnO4 và KClO3 có tỉ lệ số mol KMnO4 : KClO3= 2:3 tác dụng với dung dịch HCl đặc dư thu được V lít khí Cl2. Cho V lít khí Cl2 vào 1,6 lít dung dịch KOH 1M thu được dung dịch X chứa m gam chất tan. Gía trị của m là
A. 126,70 B. 101,36 C. 139,37 D. 152,04
- Theo bài ra \(\Rightarrow\left\{{}\begin{matrix}n_{KMnO_4}=0,1\\n_{KClO_3}=0,15\end{matrix}\right.\) ( mol )
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
.......0,1..........................................................0,25...........
\(KClO_3+6HCl\rightarrow KCl+3Cl_2+3H_2O\)
....0,15................................0,45....................
\(\Rightarrow n_{HCl}=0,7\left(mol\right)\)
\(6KOH+3Cl_2\rightarrow KClO_3+5KCl+3H_2O\)
Ta có : \(m=m_{KOH}+m_{Cl_2}=139,3\left(g\right)\)
Vậy ...
Đúng 2
Bình luận (0)
cho 2,6 gam Zn áp dụng với 200 ml dung dịch hcl thu được ---------> Zn cl2 và khí cl2
a) tích khối lượng Zn thu được
b) tính nồng độ mol của 200 ml của dung dịch hcl
c) tính thể tích H2 ở ĐKTC
\(n_{Zn}=\dfrac{2,6}{65}=0,04\left(mol\right)\)
Pt : \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
a) Sửa đề : tính khối lượng ZnCl2 thu được
Theo Pt : \(n_{Zn}=n_{ZnCl2}=n_{H2}=0,04\left(mol\right)\)
\(\Rightarrow m_{ZnCl2}=0,04.136=5,44\left(g\right)\)
b) Theo Pt : \(n_{HCl}=2n_{Zn}=2.0,04=0,08\left(mol\right)\)\
\(C_{MddHCl}=\dfrac{0,08}{0,2}=0,4\left(M\right)\)
c) \(V_{H2\left(dktc\right)}=0,04.22,4=0,896\left(l\right)\)
Chúc bạn học tốt
Đúng 3
Bình luận (1)
Cho dung dịch chứa 14,6 gam HCl tác dụng hết với
K
M
n
O
4
, thu được V lít khí
C
l
2
(đktc). Giá trị của V là A. 4,48 B. 8,96 C. 2,80 D. 5,60
Đọc tiếp
Cho dung dịch chứa 14,6 gam HCl tác dụng hết với K M n O 4 , thu được V lít khí C l 2 (đktc). Giá trị của V là
A. 4,48
B. 8,96
C. 2,80
D. 5,60
Chọn đáp án C
2 K M n O 4 + 16HCl → 2KCl + 2 M n C l 2 + 5 C l 2 + 8 H 2 O
n H C l = 14 , 6 36 , 5 = 0,4 (mol) => n C l 2 = 14 36 , 5 = 0,125 (mol)
=> V = 0,125.22,4 = 2,8 (lít)
Đúng 0
Bình luận (0)