Khử hoàn toàn a gam một oxit săt bằng CO ở nhiệt độ cao người ta thu được 14,56 gam sắt và 8,736 lit CO2 ở đktc. Tìm CTHH của oxit sắt.

Những câu hỏi liên quan
Khử hoàn toàn một oxit sắt X ở nhiệt độ cao cần vừa đủ V lít khí CO (ở đktc), sau phản ứng thu được 0,84 gam Fe và 0,02 mol khí CO2. Oxit sắt X và giá trị của V lần lượt là: A. Fe3O4 và 0,224 B. Fe3O4 và 0,448 C. FeO và 0,224 D. Fe2O3 và 0,448
Đọc tiếp
Khử hoàn toàn một oxit sắt X ở nhiệt độ cao cần vừa đủ V lít khí CO (ở đktc), sau phản ứng thu được 0,84 gam Fe và 0,02 mol khí CO2. Oxit sắt X và giá trị của V lần lượt là:
A. Fe3O4 và 0,224
B. Fe3O4 và 0,448
C. FeO và 0,224
D. Fe2O3 và 0,448
Đáp án B
Đặt công thức oxit sắt là FexOy
FexOy+ yCO → xFe + yCO2
nFe= 0,84/56= 0,015 mol
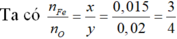
→Công thức oxit là Fe3O4
Ta có: nCO= nCO2= 0,02 mol
→ V= 0,02.22,4= 0,448 lít
Đúng 0
Bình luận (0)
Khử hoàn toàn một oxit sắt X ở nhiệt độ cao cần vừa đủ V lít khí CO (ở đktc), sau phản ứng thu được 1,12 gam Fe và 0,03 mol khí CO2. Công thức của X và giá trị V lần lượt là A. Fe3O4 và 0,224 B. Fe2O3 và 0,672 C. Fe3O4 và 0,448 D. FeO và 0,224
Đọc tiếp
Khử hoàn toàn một oxit sắt X ở nhiệt độ cao cần vừa đủ V lít khí CO (ở đktc), sau phản ứng thu được 1,12 gam Fe và 0,03 mol khí CO2. Công thức của X và giá trị V lần lượt là
A. Fe3O4 và 0,224
B. Fe2O3 và 0,672
C. Fe3O4 và 0,448
D. FeO và 0,224
Đáp án B.
Đặt công thức oxit sắt là FexOy
Ta có: nFe= 1,12/56= 0,02mol
FexOy+ yCO → xFe+ yCO2
Theo PTHH:
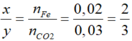
→ Oxit là Fe2O3
Ta có: nCO= nCO2= 0,03 mol→ V= 0,03.22,4= 0,672 lít
Đúng 0
Bình luận (0)
Khử hoàn toàn một oxit sắt X ở nhiệt độ cao cần vừa đủ V lít khí CO (ở đktc), sau phản ứng thu được 0,84 gam Fe và 0,02 mol khí
C
O
2
. Công thức của X và giá trị V lần lượt là A.
F
e
3
O
4
và 0,224. B.
F
e
3
O
4
và 0,448. C. FeO và 0...
Đọc tiếp
Khử hoàn toàn một oxit sắt X ở nhiệt độ cao cần vừa đủ V lít khí CO (ở đktc), sau phản ứng thu được 0,84 gam Fe và 0,02 mol khí C O 2 . Công thức của X và giá trị V lần lượt là
A. F e 3 O 4 và 0,224.
B. F e 3 O 4 và 0,448.
C. FeO và 0,224.
D. F e 2 O 3 và 0,448.
Đặt X:
F e x O y T a c ó n O ( x ) = n C O 2 = n C O = 0 , 02 m o l → V = 0 , 02 . 22 , 4 = 0 , 448 l í t . x : y = n F e : n O ( X ) = 0 , 015 : 0 , 02 = 3 : 4 . V ậ y X l à F e 3 O 4 .
Chọn đáp án B.
Đúng 0
Bình luận (0)
khử hoàn toàn 16 gam oxit sắt (FexOy) bằng 7,392 lít H2 (đktc) ở nhiệt độ cao Xác định CTHH của oxit sắt, biết lượng H2 đã lấy dư 10% so với lượng cần thiết để phản ứng với oxit sắt
Xem chi tiết
Ta có: \(n_{H_2}=\dfrac{7,392}{22,4}=0,33\left(mol\right)\)
Gọi: nH2 (pư) = a (mol) ⇒ nH2 (dư) = 10%a (mol)
⇒ a + 10%a = 0,33
⇒ a = 0,3 (mol)
Có: \(H_2+O_{\left(trongoxit\right)}\rightarrow H_2O\)
⇒ nO (trong oxit) = 0,3 (mol)
\(\Rightarrow n_{Fe}=\dfrac{16-m_{O\left(trongoxit\right)}}{56}=0,2\left(mol\right)\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{0,2}{0,3}=\dfrac{2}{3}\)
Vậy: CTHH cần tìm là Fe2O3.
Đúng 1
Bình luận (0)
Hoàn tan hoàn toàn 12,8 gam hỗn hợp bột gồm sắt và oxit sắt bằng dd hcl dư thấy thoát ra 4,48 lít khí ở đktc mặt khác nếu khử hoàn toàn 6,4 gam hỗn hợp đí thù thu được 0,27 gam nước Tìm CTHH của oxit sắt
CTHH: FexOy
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,2<---------------------0,2
=> \(m_{Fe_xO_y}=12,8-0,2.56=1,6\left(g\right)\)
Trong 6,4g hỗn hợp rắn chứa 0,8g FexOy
\(n_{H_2O}=\dfrac{0,27}{18}=0,015\left(mol\right)\)
PTHH: FexOy + yH2 --to--> xFe + yH2O
\(\dfrac{0,015}{y}\)<---------------------0,015
=> \(M_{Fe_xO_y}=\dfrac{0,8}{\dfrac{0,015}{y}}=\dfrac{160}{3}y\)
=> \(56x+16y=\dfrac{160}{3}y\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\Rightarrow Fe_2O_3\)
Đúng 1
Bình luận (3)
Khử hoàn toàn một oxit sắt ở nhiệt độ cao cần vừa đủ V lít khí CO dư (đktc), sau phản ứng thu được 0,84 gam Fe và 0,02 mol khí CO2. Công thức của X và giá trị V lần lượt là A. Fe3O4 và 0,224 B. FeO và 0,224 C. Fe2O3 và 0,448 D. Fe3O4 và 0,448
Đọc tiếp
Khử hoàn toàn một oxit sắt ở nhiệt độ cao cần vừa đủ V lít khí CO dư (đktc), sau phản ứng thu được 0,84 gam Fe và 0,02 mol khí CO2. Công thức của X và giá trị V lần lượt là
A. Fe3O4 và 0,224
B. FeO và 0,224
C. Fe2O3 và 0,448
D. Fe3O4 và 0,448
Đáp án : D
FexOy + yCO -> xFe + yCO2
=> nFe : nCO2 = 0,015 : 0,02 = x : y
=> x : y = 3 : 4
Oxit sắt là : Fe3O4
nCO = nCO2 = 0,02 mol => V = 0,448 lit
Đúng 0
Bình luận (0)
BÀI 7/ Đun khử hoàn toàn 4 gam hỗn hợp CuO và oxit sắt FexOy bằng khí CO ở nhiệt độ cao , sau phản ứng thu được 2,88 gam chất rắn ,hòa tan chất rắn này vào dung dịch HCl
( vừa đủ) thì có 0,896 lit khí thoát ra (ở đktc). Xác định công thức của oxit sắt .
\(n_{H_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
PTHH: Fe + 2HCl ---> FeCl2 + H2
0,04 <----------------------- 0,04
\(\rightarrow m_{Cu}=2,88-0,04.56=0,64\left(g\right)\\\rightarrow n_{Cu}=\dfrac{0,64}{64}=0,01\left(mol\right)\)
\(m_{giảm}=m_{O\left(oxit\right)}=4-2,88=1,12\left(g\right)\\ \rightarrow n_O=\dfrac{1,12}{16}=0,07\left(mol\right)\)
\(\rightarrow n_{O\left(Fe_xO_y\right)}=0,07-0,01.1=0,06\left(mol\right)\)
CTHH FexOy
=> x : y = 0,04 : 0,06 = 2 : 3
CTHH Fe2O3
Đúng 4
Bình luận (3)
\(n_{CuO}=\dfrac{4}{80}=0,05mol\)
\(CuO+CO\underrightarrow{t^o}Cu+CO_2\)
\(Fe_xO_y+yCO\underrightarrow{t^o}xFe+yCO_2\)
Chất rắn sau phản ứng thu đc cho tác dụng với HCl chỉ có Fe tác dụng.
\(n_{H_2}=\dfrac{0,896}{22,4}=0,04mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,04 0,08 0,04 0,04
\(m_{Cu}=2,88-0,04\cdot56=0,64g\Rightarrow n_{CuO}=n_{Cu}=0,01mol\)
\(\Rightarrow m_{Fe_xO_y}=4-0,01\cdot80=3,2g\)
\(n_{Fe_xO_y}=\dfrac{1}{x}n_{Fe}=\dfrac{0,04}{x}\)
\(M=\dfrac{3,2}{\dfrac{0,04}{x}}=80x\)
Nhận thấy \(x=2\Rightarrow Fe_2O_3\)
Đúng 1
Bình luận (0)
Khử hoàn toàn 16 gam một oxit sắt (dạng bột) bằng khí CO ở nhiệt độ cao. Người ta nhận thấy lượng CO2 sinh ra vượt quá lượng CO cần dùng là 4,8 gam. Cho lượng chất rắn thu được sau phản ứng hòa tan trong dung dịch H2SO4 0,5M (vừa đủ), thu được V lít khí (đktc). Dẫn từ từ V lít khí đó đến khi hết qua 20 gam bột CuO nung nóng, thu được a gam chất rắn.a, Hãy xác định công thức oxit sắt.b, Tính V và thể tích dung dịch H2SO4 cần dùng.c, Tính a.
Đọc tiếp
Khử hoàn toàn 16 gam một oxit sắt (dạng bột) bằng khí CO ở nhiệt độ cao. Người ta nhận thấy lượng CO2 sinh ra vượt quá lượng CO cần dùng là 4,8 gam. Cho lượng chất rắn thu được sau phản ứng hòa tan trong dung dịch H2SO4 0,5M (vừa đủ), thu được V lít khí (đktc). Dẫn từ từ V lít khí đó đến khi hết qua 20 gam bột CuO nung nóng, thu được a gam chất rắn.
a, Hãy xác định công thức oxit sắt.
b, Tính V và thể tích dung dịch H2SO4 cần dùng.
c, Tính a.
a)
nCO2 = nCO = nO(bị khử)
Có \(m_{CO_2}-m_{CO}=4,8\)
=> \(44.n_{O\left(bị.khử\right)}-28.n_{O\left(bị.khử\right)}=4,8\)
=> nO(bị khử) = 0,3 (mol)
=> \(n_{Fe}=\dfrac{16-0,3.16}{56}=0,2\left(mol\right)\)
Xét nFe : nO = 0,2 : 0,3 = 2 : 3
=> CTHH: Fe2O3
b)
PTHH: Fe + H2SO4 --> FeSO4 + H2
0,2-->0,2--------------->0,2
=> V = 0,2.22,4 = 4,48 (l)
\(V_{dd.H_2SO_4}=\dfrac{0,2}{0,5}=0,4\left(l\right)\)
c) \(n_{CuO}=\dfrac{20}{80}=0,25\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
Xét tỉ lệ: \(\dfrac{0,25}{1}>\dfrac{0,2}{1}\) => H2 hết, CuO dư
PTHH: CuO + H2 --to--> Cu + H2O
0,2<--0,2-------->0,2
=> a = (0,25-0,2).80 + 0,2.64 = 16,8 (g)
Đúng 3
Bình luận (1)
Khử hoàn toàn 16 gam một oxit sắt (dạng bột) bằng khí CO ở nhiệt độ cao. Người ta nhận thấy lượng CO2 sinh ra vượt quá lượng CO cần dùng là 4,8 gam. Cho lượng chất rắn thu được sau phản ứng hòa tan trong dung dịch H2SO4 0,5M (vừa đủ), thu được V lít khí (đktc). Dẫn từ từ V lít khí đó đến khi hết qua 20 gam bột CuO nung nóng, thu được a gam chất rắn.a, Hãy xác định công thức oxit sắt.b, Tính V và thể tích dung dịch H2SO4 cần dùng.cần gấp ạ
Đọc tiếp
Khử hoàn toàn 16 gam một oxit sắt (dạng bột) bằng khí CO ở nhiệt độ cao. Người ta nhận thấy lượng CO2 sinh ra vượt quá lượng CO cần dùng là 4,8 gam. Cho lượng chất rắn thu được sau phản ứng hòa tan trong dung dịch H2SO4 0,5M (vừa đủ), thu được V lít khí (đktc). Dẫn từ từ V lít khí đó đến khi hết qua 20 gam bột CuO nung nóng, thu được a gam chất rắn.
a, Hãy xác định công thức oxit sắt.
b, Tính V và thể tích dung dịch H2SO4 cần dùng.
cần gấp ạ
\(m_{tăng}=m_O=4,8\left(g\right)\\ \rightarrow n_{O\left(trong\text{ oxit}\right)}=\dfrac{4,8}{16}=0,3\left(mol\right)\\ \rightarrow n_{Fe\left(\text{trong oxit}\right)}=\dfrac{16-4,8}{56}=0,2\left(mol\right)\)
CTHH của oxit sắt: FexOy
=> x : y = 0,2 : 0,3 = 2 : 3
=> CTHH là Fe2O3
\(PTHH:Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ Mol:0,2\rightarrow0,2\\ \rightarrow V_{ddH_2SO_4}=\dfrac{0,2}{0,5}=0,4\left(l\right)=400\left(ml\right)\)
Đúng 1
Bình luận (0)















