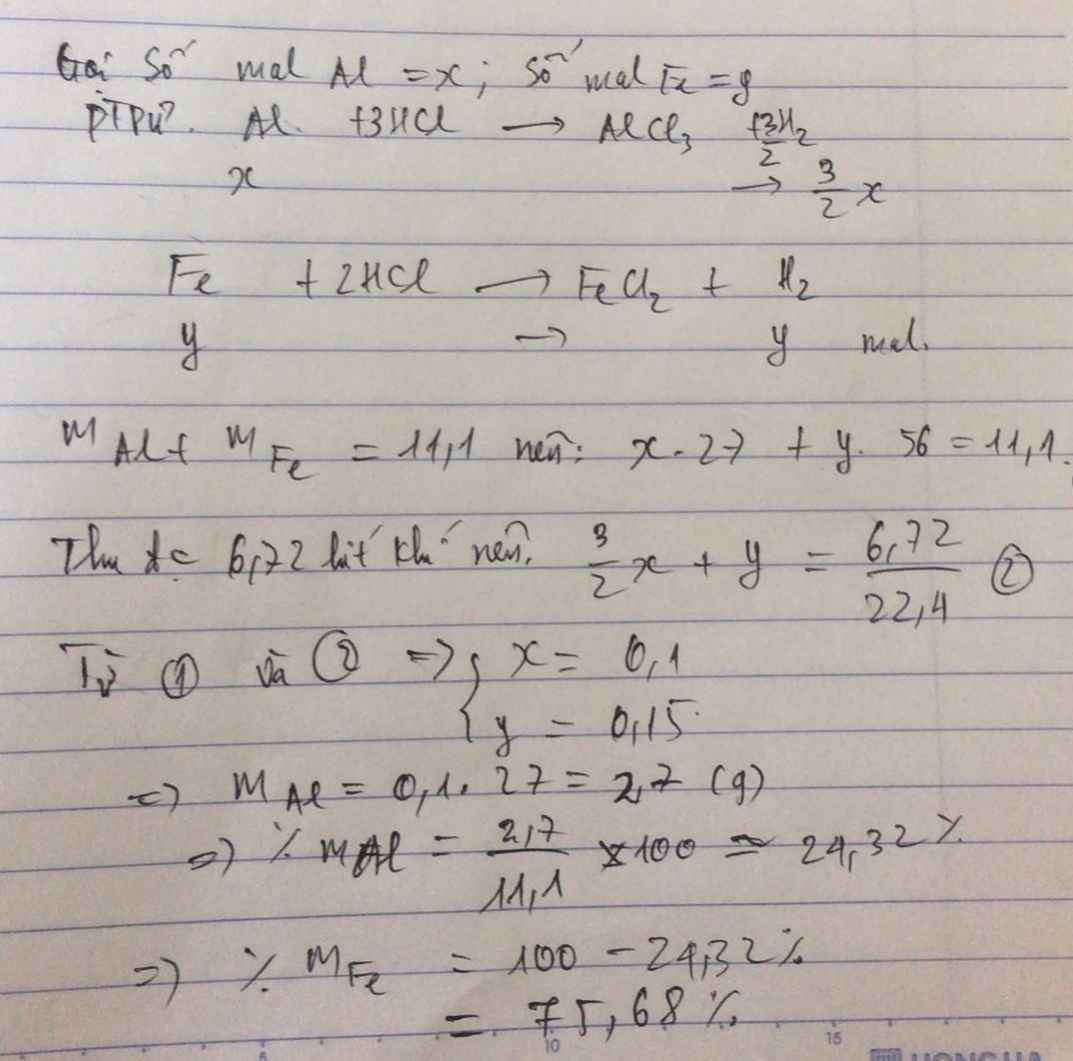Cho 7,2 gam một kim loại tác dụng vừa đủ với HCl cho 6,72 lít khí H2(đktc). Cho biết kim loại đó?

Những câu hỏi liên quan
Cho m gam Fe2O3 tác dụng vừa đủ với V lít khí H2(đktc). Toàn bộ lượng kim loại tạo thành tác dụng vừa đủ với dd HCl thu được V' lít khí H2(đktc). Tính tỉ lệ V/V'
$Fe_2O_3+3H_2\rightarrow 2Fe+3H_2O$
$Fe+2HCl\rightarrow FeCl_2+H_2$
Gọi số mol Fe2O3 là a
Ta có: $n_{H_2/(1)}=3a(mol);n_{H_2/(2)}=2a(mol)$
\(\Rightarrow\dfrac{V}{V'}=\dfrac{n_{H_2\left(1\right)}}{n_{H_2\left(2\right)}}=\dfrac{3}{2}\)
Đúng 2
Bình luận (0)
Cho 5,4 gam kim loại M(hóa trị III) tác dụng vừa hết với HCl thu được 6,72 khí H2(đktc). Xác định kim loại M
nH2 = 6.72/22.4 = 0.3 (mol)
2M + 6HCl => 2MCl3 + 3H2
0.2...................................0.3
MM = 5.4/0.2 = 27 (g/mol)
=> M là : Al
Đúng 1
Bình luận (0)
PTHH 2M + 6HCl ------>\(2MCl_3+3H_2\)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_M=\dfrac{0,3.2}{3}=0,2\left(mol\right)\)
\(=>M_M=\dfrac{5,4}{0,2}=27\left(\dfrac{g}{mol}\right)\)
Vậy M là Al
Chúc bạn học tốt
Đúng 1
Bình luận (0)
Cho 8,8 gam một hỗn hợp gồm hai kim loại kiềm thổ ở hai chu kì liên tiếp tác dụng với dung dịch HCl dư thu được 6,72 lít khí H2 (ở đktc). Hai kim loại đó là:
A. Ca và Sr.
B. Be và Mg
C. Mg và Ca
D. Sr và Ba
Chọn C
Các chất thỏa mãn : Al2O3 ; Zn(OH)2 ; NaHS ; (NH4)2CO3 ; Al
Đúng 0
Bình luận (0)
Cho 8,8 gam một hỗn hợp gồm hai kim loại kiềm thổ ở hai chu kì liên tiếp tác dụng với dung dịch HCl dư thu được 6,72 lít khí H2 (ở đktc). Hai kim loại đó là A. Ca và Sr. B. Be và Mg. C. Mg và Ca. D. Sr và Ba.
Đọc tiếp
Cho 8,8 gam một hỗn hợp gồm hai kim loại kiềm thổ ở hai chu kì liên tiếp tác dụng với dung dịch HCl dư thu được 6,72 lít khí H2 (ở đktc). Hai kim loại đó là
A. Ca và Sr.
B. Be và Mg.
C. Mg và Ca.
D. Sr và Ba.
Đáp án : C
Tổng quát : M + 2H2O -> M(OH)2 + H2
=> nM = nH2 = 0,3 mol => Mtb = 29,33g
=> Mg(24) và Ca(40)
Đúng 0
Bình luận (0)
cho 11,1 gam hỗn hợp gồm Al và Fe tác dụng vừa đủ với dung dịch V(ml) dung dịch HCl 1M thu được 6,72 lít khí H2 (đktc). phần trăm khối lượng mỗi kim loại tròn mỗi hỗn hợp trên
Gọi số mol Al, Fe là a, b (mol)
=> 27a + 56b = 11,1 (1)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
a----------------------->1,5a
Fe + 2HCl --> FeCl2 + H2
b------------------------>b
=> 1,5a + b = 0,3 (2)
(1)(2) => a = 0,1; b = 0,15
=> \(\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,1.27}{11,1}.100\%=24,32\%\\\%m_{Fe}=\dfrac{0,15.56}{11,1}.100\%=75,68\end{matrix}\right.\)
Đúng 4
Bình luận (0)
Cho 4,05 gam một kim loại chưa biết hóa trị tác dụng vừa đủ với 2,52 lít khí oxi (đktc). Tìm
kim loại đó.
Gọi kim loại cần tìm là R, hóa trị n
\(n_{O_2}=\dfrac{2,52}{22,4}=0,1125\left(mol\right)\)
PTHH: 4R + nO2 --to--> 2R2On
\(\dfrac{0,45}{n}\)<-0,1125
=> \(M_R=\dfrac{4,05}{\dfrac{0,45}{n}}=9n\left(g/mol\right)\)
- Nếu n = 1 => Loại
- Nếu n = 2 => Loại
- Nếu n = 3 => MR = 27 (g/mol)
=> R là Al
Đúng 5
Bình luận (0)
Ta đặt công thức là X , hóa trị 1
4X+O2-to>2X2O
0,45--0,1125 mol
n O2=\(\dfrac{2,52}{22,4}\)=0,1125 mol
=>MX=\(\dfrac{4,05}{0,45}\)=9 g\mol
Lập bảng :
n 1 2 3
M 9 18 27
=>n=3=>MX=27 (TM)
=>X là Nhôm (Al)
Đúng 5
Bình luận (0)
Cho 53,75 gam hỗn hợp X gồm kim loại Sn, Fe, Al tác dụng vừa đủ với 25,20 lít khí Cl2 (đktc). Mặt khác khi cho 0,40 mol hỗn hợp X tác dụng với dung dịch HCl nóng, dư thư được 9,92 lít khí H2 (đktc). Biết các phản ứng xảy ra hoàn toàn. Khối lượng của kim loại Al trong 0,40 mol hỗn hợp X có giá trị gần với A. 1,5 B. 4,0 C. 2,3 D. 3,1
Đọc tiếp
Cho 53,75 gam hỗn hợp X gồm kim loại Sn, Fe, Al tác dụng vừa đủ với 25,20 lít khí Cl2 (đktc). Mặt khác khi cho 0,40 mol hỗn hợp X tác dụng với dung dịch HCl nóng, dư thư được 9,92 lít khí H2 (đktc). Biết các phản ứng xảy ra hoàn toàn. Khối lượng của kim loại Al trong 0,40 mol hỗn hợp X có giá trị gần với
A. 1,5
B. 4,0
C. 2,3
D. 3,1
Đáp án : A
Trong 53,75g X có x mol Sn ; y mol Fe ; z mol Al
=> t(119x + 56y + 27z) = 53,75g
X + Cl2 -> SnCl4 ; FeCl3 ; AlCl3
⇒ t 4 x + 3 y + 3 z = 2 n C l 2 = 2 , 25 m o l
(Trong 0,4 mol lượng chất gấp t lần)
=> 9(119x + 56y + 27z) = 215(4x + 3y + 3z)
=> 211x – 141y – 402z = 0(1)
=> x + y + z = 0,4 mol(2)
n H 2 = x + y + 1,5z = 31/70 (mol) (3)
Từ (1,2,3) => z = 0,0857 mol
=> mAl = 2,314g
Đúng 0
Bình luận (0)
Một hỗn hợp gồm 3 kim loại: Na, Cu và Fe cho tác dụng với nước (dư) thì thu được dd A; hỗn hợp chất rắn B và 6,72 lít khí C (đktc). Cho B tác dụng vừa đủ với 0,2 mol HCl, sau phản ứng còn lại 10 gam chất rắn.a/ Xác định % khối lượng mỗi kim loại trong hỗn hợp ban đầu.b/ Khí C thu được tác dụng vừa đủ với 17,4 gam oxit sắt chưa rõ hoá trị ở to cao. Xác định CTHH của oxit sắt.
Đọc tiếp
Một hỗn hợp gồm 3 kim loại: Na, Cu và Fe cho tác dụng với nước (dư) thì thu được dd A; hỗn hợp chất rắn B và 6,72 lít khí C (đktc). Cho B tác dụng vừa đủ với 0,2 mol HCl, sau phản ứng còn lại 10 gam chất rắn.
a/ Xác định % khối lượng mỗi kim loại trong hỗn hợp ban đầu.
b/ Khí C thu được tác dụng vừa đủ với 17,4 gam oxit sắt chưa rõ hoá trị ở to cao. Xác định CTHH của oxit sắt.
a)
\(n_{H_2\left(1\right)}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Na + 2H2O --> 2NaOH + H2 (1)
0,6<----------------------0,3
=> mNa = 0,6.23 = 13,8 (g)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,1<-0,2
=> mFe = 0,1.56 = 5,6 (g)
mCu = 10 (g)
\(\left\{{}\begin{matrix}\%Na=\dfrac{13,8}{13,8+5,6+10}.100\%=46,94\%\\\%Fe=\dfrac{5,6}{13,8+5,6+10}.100\%=19,05\%\\\%Cu=\dfrac{10}{13,8+5,6+10}.100\%=34,01\%\end{matrix}\right.\)
b)
PTHH: FexOy + yH2 --to--> xFe + yH2O
\(\dfrac{0,3}{y}\)<--0,3
=> \(M_{Fe_xO_y}=\dfrac{17,4}{\dfrac{0,3}{y}}=58y\left(g/mol\right)\)
=> 56x = 42y
=> \(\dfrac{x}{y}=\dfrac{3}{4}\) => CTHH: Fe3O4
Đúng 4
Bình luận (0)
Một hỗn hợp gồm 3 kim loại: Na, Cu và Fe cho tác dụng với nước (dư) thì thu được dd A; hỗn hợp chất rắn B và 6,72 lít khí C (đktc). Cho B tác dụng vừa đủ với 0,2 mol HCl, sau phản ứng còn lại 10 gam chất rắn.a/ Xác định % khối lượng mỗi kim loại trong hỗn hợp ban đầu.b/ Khí C thu được tác dụng vừa đủ với 17,4 gam oxit sắt chưa rõ hoá trị ở to cao. Xác định CTHH của oxit sắt.
Đọc tiếp
Một hỗn hợp gồm 3 kim loại: Na, Cu và Fe cho tác dụng với nước (dư) thì thu được dd A; hỗn hợp chất rắn B và 6,72 lít khí C (đktc). Cho B tác dụng vừa đủ với 0,2 mol HCl, sau phản ứng còn lại 10 gam chất rắn.
a/ Xác định % khối lượng mỗi kim loại trong hỗn hợp ban đầu.
b/ Khí C thu được tác dụng vừa đủ với 17,4 gam oxit sắt chưa rõ hoá trị ở to cao. Xác định CTHH của oxit sắt.
a)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Na + 2H2O --> 2NaOH + H2
0,6<----------------------0,3
Fe + 2HCl --> FeCl2 + H2
0,1<--0,2
=> \(\left\{{}\begin{matrix}m_{Na}=0,6.23=13,8\left(g\right)\\m_{Fe}=0,1.56=5,6\left(g\right)\\m_{Cu}=10\left(g\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%m_{Na}=\dfrac{13,8}{13,8+5,6+10}.100\%=46,94\%\\\%m_{Fe}=\dfrac{5,6}{13,8+5,6+10}.100\%=19,05\%\\\%m_{Cu}=\dfrac{10}{13,8+5,6+10}.100\%=34,01\%\end{matrix}\right.\)
b)
PTHH: FexOy + yH2 --to--> xFe + yH2O
\(\dfrac{0,3}{y}\)<--0,3
=> \(M_{Fe_xO_y}=56x+16y=\dfrac{17,4}{\dfrac{0,3}{y}}\left(g/mol\right)\)
=> \(\dfrac{x}{y}=\dfrac{3}{4}\)
=> CTHH: Fe3O4
Đúng 1
Bình luận (0)