Khử hoàn toàn 32 gam hỗn hợp CuO; Fe2O3 bằng khí hidro ở nhiệt độ cao.
a. Viết PTHH xảy ra
b. Tính thể tích khí H2 cần để khử hỗn hợp (ở đktc), biết Fe2O3 chiểm 20% khối lượng hỗn hợp.
c.Tính khối lượng các kim loại tạo thành
Hòa tan hoàn toàn 11,9 gam hỗn hợp Al và Zn bằng dung dịch HCl thu được dung dịch X và một lượng H2 vừa đủ để khử 32 gam CuO. Tổng khối lượng muối trong X là
A. 12,7 gam
B. 40,3 gam
C. 43,9 gam
D. 28,4 gam
Hòa tan hoàn toàn 11,9 gam hỗn hợp Al và Zn bằng dung dịch HCl thu được dung dịch X và một lượng H2 vừa đủ để khử 32 gam CuO. Tổng khối lượng muối trong X là
A. 12,7 gam
B. 40,3 gam
C. 43,9 gam
D. 28,4 gam
Chọn đáp án B
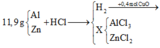
nH2 = nCuO = 0,4 (mol)
BTNT H: nHCl = 2nH2 = 0,8 (mol)
BTKL: mmuối = mAl+Zn + mCl- = 11,9 + 0,8.35,5 = 40,3 (g)
Hòa tan hoàn toàn 19,52 gam hỗn hợp CuO, FeO, Fe2O3 trong H2SO4 loãng dư thu được 45,12 gam hỗn hợp muối. Khử hoàn toàn hỗn hợp ban đầu bằng H2 dư thì khối lượng kim loại sinh ra là :
A. 13,2 gam
B. 14,4 gam
C. 16,8 gam
D. 15,1 gam
Hòa tan hoàn toàn 19,52 gam hỗn hợp CuO, FeO, Fe2O3 trong H2SO4 loãng dư thu được 45,12 gam hỗn hợp muối. Khử hoàn toàn hỗn hợp ban đầu bằng H2 dư thì khối lượng kim loại sinh ra là :
A. 13,2 gam
B 14,4 gam
C. 16,8 gam
D 15,1 gam
Hòa tan hoàn toàn 19,52 gam hỗn hợp CuO, FeO, Fe2O3 trong H2SO4 loãng dư thu được 45,12 gam hỗn hợp muối. Khử hoàn toàn hỗn hợp ban đầu bằng H2 dư thì khối lượng kim loại sinh ra là :
A. 13,2 gam
B 14,4 gam
C. 16,8 gam
D 15,1 gam
Để khử hoàn toàn m g hỗn hợp X gồm CuO, Fe2O3, Fe3O4 cần dùng vừa đủ 6,72 lít H2 (đktc). Nếu dùng nhôm làm chất khử thì khối lượng nhôm cần dùng để khử hoàn toàn m gam hỗn hợp X trên là
\(n_{H_2}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
\(H_2+O\rightarrow H_2O\)
\(0.3.....0.3\)
\(2Al+3O\rightarrow Al_2O_3\)
\(0.2......0.3\)
\(m_{Al}=0.2\cdot27=5.4\left(g\right)\)
dùng \(H_2\) khử hoàn toàn 31,2 gam hỗn hợp CuO và \(Fe_3O_4\) trong hỗn hợp khối lượng \(Fe_3O_4\) lớn hơn khối lượng CuO là 15,2 gam.tính khối lượng Cu và Fe tạo ra
\(m_{Fe_3O_4} = \dfrac{31,2 + 15,2}{2} = 23,2(gam) \Rightarrow n_{Fe_3O_4} = \dfrac{23,2}{232} = 0,1(mol)\\ Fe_3O_4 + 4H_2 \xrightarrow{t^o} 3Fe + 4H_2O\\ n_{Fe} = 3n_{Fe_3O_4} = 0,3(mol) \Rightarrow m_{Fe} = 0,3.56 = 16,8(gam)\\ CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ n_{Cu} = n_{CuO} = \dfrac{31,2-23,2}{80} = 0,1(mol) \Rightarrow m_{Cu} = 0,1.64 = 6,4(gam)\)
Ta có:\(\left\{{}\begin{matrix}m_{CuO}+m_{Fe_3O_4}=31,2\\m_{Fe_3O_{\text{4}}}-m_{CuO}=15,2\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}m_{Fe_3O_4}=23.2\\m_{CuO}=8\end{matrix}\right.\)
\(n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1\left(mol\right)\)
\(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
\(Fe_3O_4+4H_2\underrightarrow{t^o}3Fe+4H_2O\)
\(0,1\rightarrow\) 0.3
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
\(0,1\rightarrow\) 0,1
\(m_{Fe}=0,3.56=16,8\left(g\right)\)
\(m_{Cu}=0,1.64=6,4\left(g\right)\)
Khử hoàn toàn 32 g hỗn hợp CuO và Fe2O3 bằng khí H2 thấy tạo ra 9g H2O. Hỗn hợp kim loại thu được là?
Để khử hoá hoàn toàn 30 gam hỗn hợp rắn gồm CuO và F e 2 O 3 bằng khí H 2 , thu được m gam hỗn hợp kim loại và 4,5 gam H 2 O . Giá trị của m là
A. 22 gam.
B. 24 gam.
C. 26 gam.
D. 28 gam.