Nêu mục đích của những thí nghiệm sau:
1. Điều chế axetilen
2. Axetilen tác dụng với oxi
3. Axetilen tác dụng với dung dịch brom
Bài 24: Để điều chế khí axetilen, người ta cho 16g Canxi cacbua vào nước.
a) Tính thể tích khí axetilen thu được ở đktc?
b) Cho toàn bộ lượng khí axetilen sinh ra tác dụng hoàn toàn với dung dịch brom 25%. Tính khối lượng dung dịch brom cần dùng? Tính khối lượng sản phẩm thu được?
cho mk xin gấp đ/án vs ạkTT
giúp em với, mai thi rồi ạ
viết phương trinh phản ứng sau
a, buta 1,3-dien tác dụng với dung dịch Brom ở -80độC và 40độC
b. propin tác dụng với hidro xúc tác Pd/PbCO3
c. Phản ứng trime hóa của axetilen
d. axetilen tác dụng với hidroclorua có xúc tác HgCl2.
a, \(CH_2=CH-CH=CH_2+Br_2\xrightarrow[1:1]{-80^oC}CH_2Br-CHBr-CH=CH_2\)
\(CH_2=CH-CH=CH_2+Br_2\xrightarrow[1:1]{40^oC}CH_2Br-CH=CH-CH_2Br\)
b, \(CH\equiv C-CH_3+H_2\xrightarrow[Pd/PbCO_3]{t^o}CH_2=CH-CH_3\)
c, \(3C_2H_2\xrightarrow[xt]{t^o,p}C_6H_6\)
d, \(CH\equiv CH+HCl\underrightarrow{HgCl_2}CH_2=CHCl\)
Bạn tham khảo nhé!
Hình vẽ bên mô tả thí nghiệm điều chế và thử tính chất của khí axetilen. Hãy cho biết một cặp chất X, Y phù hợp với thí nghiệm. Nêu hiện tượng xảy ra trong ống nghiệm đựng dung dịch Br2 khi sục khí axetilen từ từ đến dư vào dung dịch Br2. Viết các phương trình hóa học và thử tính chất của axetilen trong thí nghiệm đó.
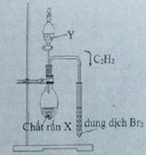
(X, Y) = (CaC2; H2O)
CH≡CH + Br2 → CH(Br2)–CH(Br2)
Dung dịch Br2 nâu đỏ dần nhạt màu rồi mất màu hoàn toàn
So sánh thể tích khí hiđro (cùng điều kiện t ° và p) thu được của từng cặp phản ứng trong những thí nghiệm sau :
Thí nghiệm 1:
0,1 mol Zn tác dụng với dung dịch HCl dư.
0,1 mol Zn tác dụng với dung dịch H 2 SO 4 dư.
Thí nghiệm 2 :
0,1 mol H 2 SO 4 tác dụng với Zn dư.
0,1 mol HCl tác dụng với Zn dư.
So sánh thể tích khí hiđro sinh ra
TN1 : Dùng dư axit để toàn lượng Zn tham gia phản ứng.
Theo (1) : 0,1 mol Zn điều chế được 0,1 mol H 2
Theo (2) : 0,1 mol Zn điều chế được 0,1 mol H 2
Kết luận : Những thể tích khí hiđro thu được trong thí nghiệm 1 là bằng nhau.
TN 2 - Dùng dư Zn để toàn lượng axit tham gia phản ứng.
Theo (1) : 0,1 mol HCl điều chế được 0,05 mol H 2
Theo (2) : 0,1 mol H 2 SO 4 điều chế được 0,1 mol H 2
Kết luận . Những thể tích khí hiđro thu được trong thí nghiệm 2 là không bằng nhau. Thể tích khí hiđro sinh ra ở (2) nhiều gấp 2 lần ở (1).
Cho các chất sau: axetilen, etilen, benzen, buta-1,3-đien, stiren, toluen, anlyl benzen, naphtalen. Số chất tác dụng được với dung dịch nước brom là
A. 6
B. 3
C. 5
D. 4
Chọn đáp án C
Các chất có thể tác dụng với nước brom có thể là : Chất có liên kết không bền ngoài nhóm chức, xicloankan với 3 cạnh, chất có chức nhóm – CHO, phenol, anilin.
Số chất tác dụng được với dung dịch nước brom là: axetilen, etilen, buta-1,3-đien, stiren, anlyl benzen.
Cho các chất sau: axetilen, etilen, benzen, buta-1,3-đien, stiren, toluen, anlyl benzen, naphtalen. Số chất tác dụng được với dung dịch nước brom là:
A. 6.
B. 3.
C. 5.
D. 4.
Chọn đáp án C
Các chất có thể tác dụng với nước brom có thể là: Chất có liên kết không bền ngoài nhóm chức, xicloankan với 3 cạnh, chất có chức nhóm – CHO, phenol, anilin.
Số chất tác dụng được với dung dịch nước brom là: axetilen, etilen, buta-1,3-đien, stiren, anlyl benzen
Cho các chất sau: axetilen, etilen, benzen, buta-1,3-đien, stiren, toluen, anlyl benzen, naphtalen. Số chất tác dụng được với dung dịch nước brom là:
A. 6.
B. 3.
C. 5.
D. 4.
Chọn đáp án C
Các chất có thể tác dụng với nước brom có thể là: Chất có liên kết không bền ngoài nhóm chức, xicloankan với 3 cạnh, chất có chức nhóm – CHO, phenol, anilin.
Số chất tác dụng được với dung dịch nước brom là: axetilen, etilen, buta-1,3-đien, stiren, anlyl benzen.
Cho các chất sau: etilen, vinylaxetilen, phenol, axit acrylic, glixerol, axetanđehit, axetilen, propan. Số chất tác dụng với brom (trong dung môi nước) ở điều kiện thường là:
A. 6
B. 7
C. 4
D. 5
cho 5,6 lít hỗn hợp khí ( đktc) gồm metan và axetilen tác dụng với 100ml dung dịch brom vừa đủ sau phản ứng thấy khối lượng dung dịch brom tăng 2,6gam
A) tính % thể tích mỗi khí trong hỗn hợp
B) tính nòng độ mol của dung dịch brom đã dùng
a.\(m_{dd.Br_2\left(tăng\right)}=m_{C_2H_2}=2,6g\)
\(n_{hh}=\dfrac{5,6}{22,4}=0,25mol\)
\(n_{C_2H_2}=\dfrac{2,6}{26}=0,1mol\)
\(\%V_{C_2H_2}=\dfrac{0,1}{0,25}.100=40\%\)
\(\%V_{CH_4}=100\%-40\%=60\%\)
b.\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
0,1 0,2 ( mol )
\(C_{M\left(dd.Br_2\right)}=\dfrac{0,2}{0,1}=2M\)