Viết phương trình hóa học biểu diễn sự cháy của sắt, phôtpho, lưu huỳnh, nhôm trong khí oxi

Những câu hỏi liên quan
Câu 9: (3,0 điểm)
a. Viết phương trình hóa học biểu diễn sự cháy của các chất sau trong khí oxi: đồng,
nhôm, lưu huỳnh, butan (C4H10)
b. Một oxit được tạo bởi 2 nguyên tố sắt và oxi trong đó tỉ lệ khối lượng giữa sắt và
oxi là 7:3. Tìm công thức phân tử của oxit đó.
a)\(2Cu+O_2\underrightarrow{t^o}2CuO\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(S+O_2\underrightarrow{t^o}SO_2\)
\(C_4H_{10}+\dfrac{13}{2}O_2\underrightarrow{t^o}4CO_2+5H_2O\)
b)Gọi CTHH là \(Fe_xO_y\)
\(x:y=\dfrac{m_{Fe}}{56}:\dfrac{m_O}{16}=\dfrac{7}{56}:\dfrac{3}{16}=0,125:0,1875=2:3\)
\(\Rightarrow\left\{{}\begin{matrix}x=2\\y=3\end{matrix}\right.\Rightarrow Fe_2O_3\)
Đúng 2
Bình luận (0)
Viết phản ứng hóa học biểu diễn sự cháy của oxi với lưu huỳnh và nhôm
\(S+O_2\rightarrow SO_2\)
\(4Al+3O_2\rightarrow2Al_2O_3\)
Đúng 0
Bình luận (1)
help me plss
Viết phương trình hóa học biểu diễn sự cháy trong oxi của các chất sau: a) Sắt, cacbon, magie, lưu huỳnh; b) Axetilen C2H2, hiđrosunfua H2S, sắt(II) sunfua FeS.
a)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
\(C+O_2\underrightarrow{t^o}CO_2\)
\(2Mg+O_2\underrightarrow{t^o}2MgO\)
\(S+O_2\underrightarrow{t^o}SO_2\)
b)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
\(H_2S+\dfrac{3}{2}O_2\underrightarrow{t^o}SO_2+H_2O\)
\(2FeS+\dfrac{7}{2}O_2\underrightarrow{t^o}Fe_2O_3+2SO_2\)
Đúng 6
Bình luận (0)
\(a,3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\\ C+O_2\rightarrow\left(t^o\right)CO_2\\ 2Mg+O_2\rightarrow\left(t^o\right)2MgO\\ S+O_2\rightarrow\left(t^o\right)SO_2\\ b,2C_2H_2+5O_2\rightarrow\left(t^o\right)4CO_2+2H_2O\\ 2H_2S+3O_2\rightarrow\left(t^o\right)2SO_2+2H_2O\\ 4FeS+7O_2\rightarrow\left(t^o\right)2Fe_2O_3+4SO_2\)
Đúng 5
Bình luận (0)
a.
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
\(C+O_2\rightarrow\left(t^o\right)CO_2\)
\(Mg+\dfrac{1}{2}O_2\rightarrow\left(t^o\right)MgO\)
\(S+O_2\rightarrow\left(t^o\right)SO_2\)
b.
\(C_2H_2+\dfrac{5}{2}O_2\rightarrow\left(t^o\right)2CO_2+H_2O\)
\(2H_2S+3O_2\rightarrow\left(t^o\right)2SO_2+2H_2O\)
\(4FeS+7O_2\rightarrow\left(t^o\right)2Fe_2O_3+4SO_2\)
Đúng 1
Bình luận (0)
Viết pthh biểu diễn sự cháy của sắt, phôt pho lưu huỳnh, metan(CH4)trong khí oxi
3Fe + 2O2 -to-> Fe3O4
S + O2 -to-> SO2
CH4 + 2O2 -to-> CO2 + 2H2O
Đúng 1
Bình luận (1)
3Fe + 2O2 -> Fe3O4
4P + 5O2 -> 2P2O5
S + O2 -> SO2
CH4 + 2O2 -> CO2 + 2H2O
P/s: Có kèm nhiệt độ nha bạn! Mình dùng đt ko viết đc
Đúng 0
Bình luận (0)
Viết phương trình hóa học biểu diễn sự cháy của oxi với các đơn chất : Lưu huỳnh S, nhôm AL ,magie Mg .Biết rằng sản phẩm là những hợp chất lần lượt là : SO2, AL2O3 ,MgO . Gọi tên các sản phẩm .
GIÚP MÌNH GẤP MỌI NGƯỜI ƠI !
HELP ME
S.O.S
\(S+O_2\rightarrow\left(t^o\right)SO_2\\ 4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\\ 2Mg+O_2\rightarrow\left(t^o\right)2MgO\)
Đọc tên sản phẩm:
SO2 : Lưu huỳnh dioxit
Al2O3: Nhôm oxit
MgO: Magie oxit
Đúng 5
Bình luận (0)
C1 viết phương trình hóa học biểu diễn sự chảy của sắt,photpho,lưu hình ,nhôm trong khí oxi
C2 dẫn 2,24 lít khí hidro(đktc) vào một ống chứa 12g CuO đã nung nóng đến một nhiệt độ thích hợp.Khối lượng nước tạo thành là:
C3 Cho chất Fe2O3
a) hợp chất Fe2O3 gồm mấy nguyên tố ? đó là nguyên tố nào?
b) Tính phần trăm về khối lượng của oxi
C1:
3Fe + 2O2 -> (t°) Fe3O4
4P + 5O2 -> (t°) 2P2O5
S + O2 -> (t°) SO2
C2:
nH2 = 2,24/22,4 = 0,1 (mol)
nCuO = 12/80 = = 0,15 (mol)
PTHH: CuO + H2 -> (t°) Cu + H2O
LTL 0,15 > 0,1 => CuO dư
nH2O = 0,1 (mol)
mH2O = 0,1 . 18 = 1,8 (g)
C3:
Fe2O3 gồm 2 nguyên tố: Fe và O
%Fe = 112/160 = 70%
%O = 100% - 70% = 30%
Đúng 3
Bình luận (2)
Câu 1: Photpho: 4P + 5O2 (to)-> 2P2O5
Lưu huỳnh: S + O2 (to)-> SO2
Nhôm: 4Al + 3O2 (to)-> Al2O3
Câu 2:
PTHH: \(CuO+H_2=>Cu+H_2O\)
\(nH_2=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(nCuO=\dfrac{12}{80}=0,15\left(mol\right)\)
\(=>CuOdư\)
\(nH_2O=nH_2=0,1\left(mol\right)\)
\(mH_2=0,1\text{×}18=1,8\left(gam\right)\)
Đúng 3
Bình luận (0)
Viết phương trình hóa học biểu diễn sự oxi hóa cho các chất sau:Kali,Cacbon,Nhôm, Sắt đồng, Kẽm>C3H8>C5H10>C2H5OH
Xem chi tiết
\(4K+O_2\underrightarrow{t^0}2K_2O\)
\(C+O_2\underrightarrow{t^0}CO_2\)
\(4Al+3O_2\underrightarrow{t^0}2Al_2O_3\)
\(3Fe+2O_2\underrightarrow{t^0}Fe_3O_4\)
\(2Cu+O_2\underrightarrow{t^0}2CuO\)
\(2Zn+O_2\underrightarrow{t^0}2ZnO\)
\(C_3H_8+5O_2\underrightarrow{t^0}3CO_2+4H_2O\)
\(C_5H_{10}+\dfrac{15}{2}O_2\underrightarrow{t^0}5CO_2+5H_2O\)
\(C_2H_5OH+3O_2\underrightarrow{t^0}2CO_2+3H_2O\)
Đúng 1
Bình luận (0)
Lưu huỳnh (S) cháy trong không khí sinh ra chất khí mùi hắc, gây ho đó là lưu huỳnh đioxit (khí sunfurơ) có công thức hóa học là SO2. a) Viết phương trình hóa học của lưu huỳnh cháy trong không khí. b) Biết khối lượng lưu huỳnh tham gia phản ứng là 1,6g. Hãy tìm. -Thể tích khí sunfurơ sinh ra ở đktc. -Thể tích không khí cần dùng ở đktc. Biết oxi chiếm 1/5 thể tích không khí.
Đọc tiếp
Lưu huỳnh (S) cháy trong không khí sinh ra chất khí mùi hắc, gây ho đó là lưu huỳnh đioxit (khí sunfurơ) có công thức hóa học là SO2.
a) Viết phương trình hóa học của lưu huỳnh cháy trong không khí.
b) Biết khối lượng lưu huỳnh tham gia phản ứng là 1,6g. Hãy tìm.
-Thể tích khí sunfurơ sinh ra ở đktc.
-Thể tích không khí cần dùng ở đktc. Biết oxi chiếm 1/5 thể tích không khí.
a) Phương trình hóa học S + O2 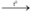 SO2
SO2
b) nS = 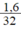 = 0,05 mol.
= 0,05 mol.
Theo phương trình trên, ta có:
nSO2 = nS = nO2 = 0,05 mol.
⇒ VSO2 = 0,05 .22,4 = 1,12 l.
⇒ VO2 = 22,4.0,05 = 1,12 l
Vì khí oxi chiếm 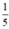 thể tích của không khí nên thể tích không khí cần là
thể tích của không khí nên thể tích không khí cần là
⇒ Vkk = 5VO2 = 5.1,12 = 5,6 l
Đúng 1
Bình luận (0)
Lưu huỳnh cháy trong oxi hoặc trong không khí sinh ra lưu huỳnh đioxit SO2. Hãy tính thể tích (đktc) sinh ra, nếu có 4 gam khí O2
tham gia phản ứng
Bước 1: Viết phương trình hóa học
Bước 2: Tìm số mol khí
Bước 3: thông qua phương trình hóa học, tìm số mol chất cần tính
Bước 4: Tìm thể tích khí
b1:
PTHH: \(S+O_2\Rightarrow SO_2\)
b2:
nSO2=\(\dfrac{m}{M}=\dfrac{4}{64}=0,0625mol\)
b4:
VSO2=22,4.n=22,4.0,0625=1,4 (lít)
Đúng 1
Bình luận (0)





























