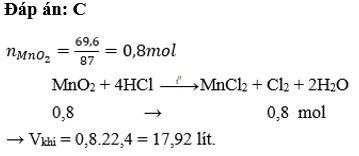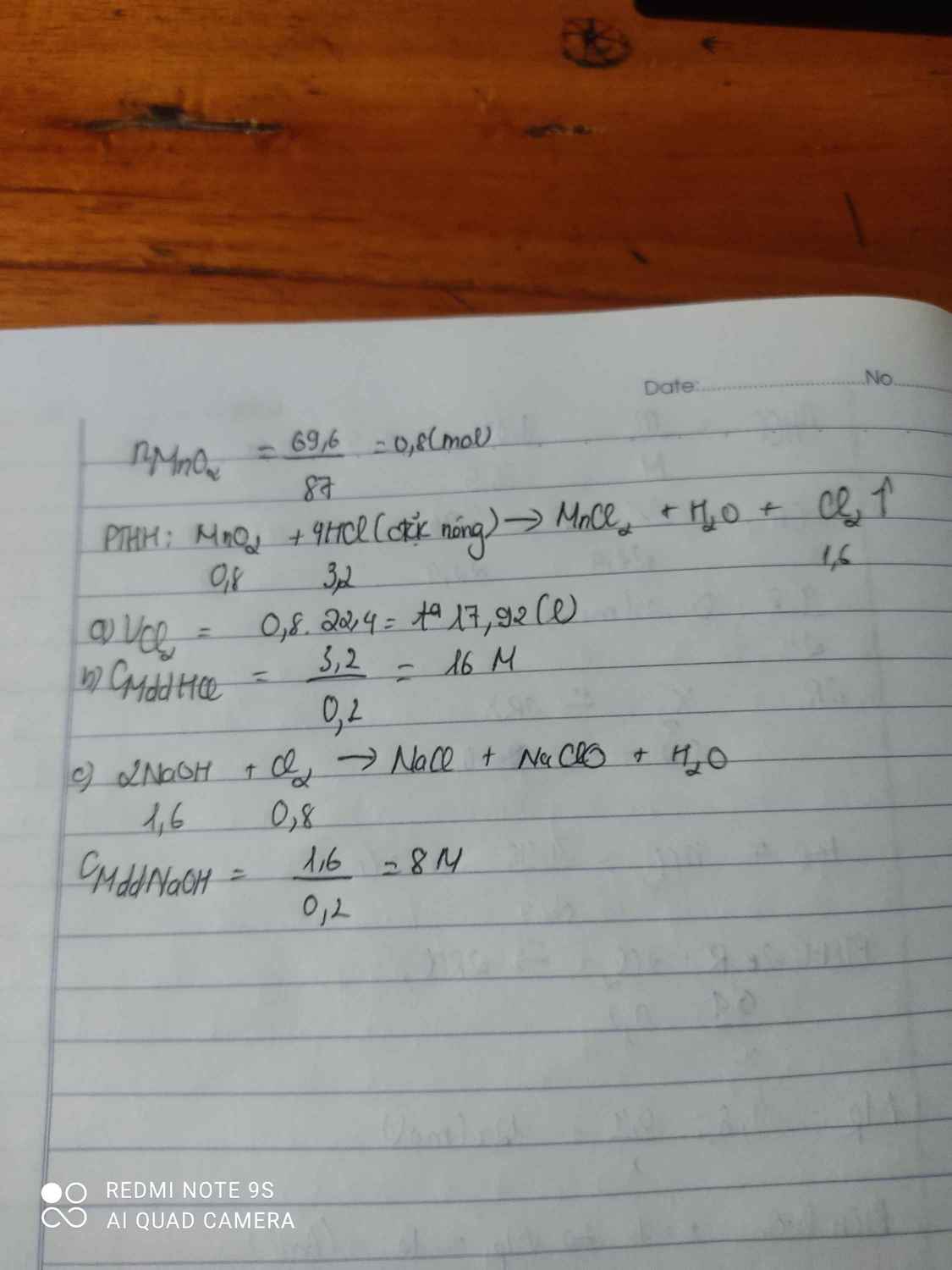Tính thể tích khí Cl2 thu được ở điều kiện tiêu chuẩn khi cho 18,25g HCl tác dụng với MnO2 [cứu em vớiiiiiii]

Những câu hỏi liên quan
Cho 13,05 gam MnO2 tác dụng hết với dung dịch HCl đăc, dư, đun nóng. Thể tích khí Cl2 thu được ở điều kiện tiêu chuẩn là V lít. Giá trị của V là A. 3,36 B. 2,24 C. 4,48 D. 5,6.
Đọc tiếp
Cho 13,05 gam MnO2 tác dụng hết với dung dịch HCl đăc, dư, đun nóng. Thể tích khí Cl2 thu được ở điều kiện tiêu chuẩn là V lít. Giá trị của V là
A. 3,36
B. 2,24
C. 4,48
D. 5,6.
Đáp án : A
MnO2 + 4HCl -> MnCl2 + Cl2 + 2H2O
=> nCl2 = nMnO2 = 0,15 mol
=> VCl2 = 3,36 lit
Đúng 0
Bình luận (0)
Cho 69,6 gam M n O 2 tác dụng với dung dịch HCl đặc, nóng, dư. Thể tích khí ở điều kiện tiêu chuẩn thu được là
A. 4,48 lít
B. 6,72 lít
C. 17,92 lít
D. 13,44 lít
Tính số gam HCl thu được khi cho 6,72 lít khí hirdo tác dụng với 1,12 lít khí clo ( Các thể tích khí ở Điều Kiện Tiêu Chuẩn )
\(n_{H_2}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
\(n_{Cl_2}=\dfrac{1.12}{22.4}=0.05\left(mol\right)\)
\(H_2+Cl_2\underrightarrow{^{^{as}}}2HCl\)
\(n_{H_2}>n_{Cl_2}\Rightarrow H_2dư\)
\(m_{HCl}=0.05\cdot2\cdot36.5=3.65\left(g\right)\)
Đúng 3
Bình luận (0)
$n_{H_2} = 0,3(mol) ; n_{Cl_2} = 0,05(mol)$
$H_2 + Cl_2 \xrightarrow{ánh\ sáng} 2HCl$
Ta thấy : $n_{H_2} > n_{Cl_2}$ nên Hidro dư
$n_{HCl} = 2n_{Cl_2} = 0,1(mol)$
$m_{HCl} = 0,1.36,5 = 3,65(gam)$
Đúng 3
Bình luận (0)
nCl2=1.1222.4=0.05(mol)nCl2=1.1222.4=0.05(mol)
H2+Cl2as→2HClH2+Cl2as→2HCl
nH2>nCl2⇒H2dưnH2>nCl2⇒H2dư
mHCl=0.05⋅2⋅36.5=3.65(g)
#HT#
Đúng 1
Bình luận (0)
Cho 32,5g kẽm tác dụng hoàn toàn với dd HCl thu được muối kẽm clorua và khí hidro. Tính thể tích khí hidro thu được ở điều kiện tiêu chuẩn Giúp em với ạ🥺
\(n_{Zn}=\dfrac{m}{M}=\dfrac{32,5}{65}=0,5\left(mol\right)\\ PTHH:Zn+2HCl->ZnCl_2+H_2\)
tỉ lệ 1 : 2 : 1 : 1
n(mol) 0,5------------------------------->0,5
\(V_{H_2\left(dktc\right)}=n\cdot22,4=0,5\cdot22,4=11,2\left(l\right)\)
Đúng 1
Bình luận (0)
Cho 69,6 gam MnO2 tác dụng với dung dịch HCl đặc dư. Biết phản ứng xảy ra hoàn toàna. Tính thể tích khí H2 thu được ở điều kiện tiêu chuẩn?b. Tính nồng độ mol dung dịch axit cần dùng cho phản ứng. Biết thể tích dung dịch axit ban đầu là 200ml.c. Dẫn toàn bộ lượng khí clo thu được ở trên cho tác dụng hết với 200ml dung dịch NaOH để điều chế nước Javen. Viết PTHH và tính nồng độ mol của dung dịch NaOH cần dùng.
Đọc tiếp
Cho 69,6 gam MnO2 tác dụng với dung dịch HCl đặc dư. Biết phản ứng xảy ra hoàn toàn
a. Tính thể tích khí H2 thu được ở điều kiện tiêu chuẩn?
b. Tính nồng độ mol dung dịch axit cần dùng cho phản ứng. Biết thể tích dung dịch axit ban đầu là 200ml.
c. Dẫn toàn bộ lượng khí clo thu được ở trên cho tác dụng hết với 200ml dung dịch NaOH để điều chế nước Javen. Viết PTHH và tính nồng độ mol của dung dịch NaOH cần dùng.
Cho 13g Zn tác dụng với 18,25g HCl a.Viết phương trình hoá học của phản ứng b.Tính khối lượng chất dư c.Tính khối lượng muối thu được và thể tích H2 thu được ( điều kiện tiêu chuẩn)
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\\ n_{HCl}=\dfrac{18,25}{35}=0,5\left(mol\right)\\ a.Zn+2HCl\rightarrow ZnCl_2+H_2\\ Vì:\dfrac{0,5}{2}>\dfrac{0,2}{1}\Rightarrow HCldư\\ n_{HCl\left(dư\right)}=0,5-0,2.2=0,1\left(mol\right)\\ m_{HCl}=0,1.36,5=3,65\left(g\right)\\ c.n_{ZnCl_2}=n_{Zn}=n_{H_2}=0,2\left(mol\right)\\ m_{ZnCl_2}=0,2.136=27,2\left(g\right)\\ V_{H_2\left(đktc\right)}=0,2.22,4=4,48\left(l\right)\)
Đúng 1
Bình luận (0)
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
\(n_{HCl}=\dfrac{18,25}{36,5}=0,5\left(mol\right)\)
a) Pt : \(Zn+2HCl\rightarrow ZnCl_2+H_2|\)
1 2 1 1
0,2 0,5 0,2 0,2
b) Lập tỉ số so sánh : \(\dfrac{0,2}{1}< \dfrac{0,5}{2}\)
⇒ Zn phản ứng hết , HCl dư
⇒ Tính toán dựa vào số mol của Zn
\(n_{HCl\left(dư\right)}=0,5-\left(0,2.2\right)=0,1\left(mol\right)\)
⇒ \(m_{HCl\left(dư\right)}=0,1.36,5=3,65\left(g\right)\)
c) \(n_{ZnCl2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{ZnCl2}=0,2.136=27,2\left(g\right)\)
\(n_{H2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,2.22,4=4,48\left(l\right)\)
Chúc bạn học tốt
Đúng 0
Bình luận (0)
Cho 5,6g sắt tác dụng với 100ml dung dịch axit clohidric HCl thu được sắt 2 và khí hidro thoát ra ở điều kiện tiêu chuẩn a,tính thể tích khí hidro thoát ra ở điều kiện tiêu chuẩn b,tính nồng độ mol của dung dịch axit clohidric đã dùng Giúp với ạ sắp thi r
`Fe + 2HCl -> FeCl_2 + H_2 \uparrow`
`0,1` `0,2` `0,1` `0,1` `(mol)`
`n_[Fe]=[5,6]/56=0,1(mol)`
`a)V_[H_2]=0,1.22,4=2,24(l)`
`b)C_[M_[HCl]]=[0,2]/[0,1]=2(M)`
Đúng 3
Bình luận (2)
Cho 2,7g Al tác dụng với axít clohidirc dư (HCL), thu được AlCl3 và khí H2 a/ viết pthh b/ tính khối lượng HCL cần dùng c/ tính khối lượng ALCL3 thu được d/ tính thể tích khí H2 thu được ở điều kiện tiêu chuẩn
Xem chi tiết
a) nAl=2,7/27=0,1(mol)
PTHH: 2Al + 6 HCl -> 2 AlCl3 + 3H2
0,1_________0,3___0,1_____0,15(mol)
b) mHCl=0,3.36,5=10,95(g)
c) mAlCl3=0,1.133,5=13,35(g)
d) V(H2,đktc)=0,15.22,4=3,36(l)
Đúng 2
Bình luận (0)
a. PTHH: 2Al + 6HCl \(\rightarrow\) 2AlCl\(_3\) + 3H\(_2\)
b. \(n_{Al}=\dfrac{m_{Al}}{M_{Al}}=\dfrac{2,7}{27}=0,1\) (mol)
\(n_{HCl}=\dfrac{0,1.6}{2}=0,3\) (mol)
\(m_{HCl}=n_{HCl}.M_{HCl}=0,3.36,5=10,95\) (g)
c. \(n_{AlCl_3}=\dfrac{0,1.2}{2}=0,1\) (mol)
\(m_{AlCl_3}=n_{AlCl_3}.M_{AlCl_3}=0,1.133,5=13,35\) (g)
d. \(n_{H_2}=\dfrac{0,1.2}{3}=0,15\) (mol)
\(V_{H_2}=n_{H_2}.22,4=0,15.22,4=3,36\) (l)
Đúng 1
Bình luận (0)
Tính thể tích khí H2 ở điều kiện tiêu chuẩn khi cho 4,8 gam Mg tác dụng với 500ml dung dịch HCl 1M
$n_{Mg} = \dfrac{4,8}{24} = 0,2(mol) ; n_{HCl} = 0,5(mol)$
$Mg + 2HCl \to MgCl_2 + H_2$
Ta thấy :
$n_{Mg} : 1 < n_{HCl} : 2$ nên HCl dư
$n_{H_2} = n_{Mg} = 0,2(mol) \Rightarrow V_{H_2} = 0,2.22,4 = 4,48(lít)$
Đúng 2
Bình luận (0)