Đốt 28 g bột sắt ngoài không khí thu m gam hôn hợp X. Cho X và dd HNO3 thu được dd A và 2.24 l khí NO. Số mol HNO3 đã phản ứng

Những câu hỏi liên quan
Cho 8,16 gam hh X gồm (Fe, FeO, Fe2O3 và Fe3O4 phản ứng với dd HNO3 (dd Y) thu được 1,344 lít khí NO (đktc) và dd Z. Dung dịch Z hòa tan tối đa 5,04 gam Fe, tạo ra khí NO. Tính số mol của HNO3 trong Y.
Số mol HNO3 có trong Y là
A. 0,54 mol. B. 0,78 mol. C. 0,50 mol. D. 0,44 mol.
Đây là câu khá kinh điển, nhưng năm nào luyện các bạn cũng sẽ thấy trong các đề thi thử. Các bạn phải giải chi tiết thì mới nhớ lâu.
Đầu tiên bàn về cách làm, vì hỗn hợp sắt và oxit qúa nhiều nên viết pt là không khả thi. Cách làm của mình là giả sử nó là hỗn hợp Fe và O.
Ta có 56x + 16y = 8.16g = phương trình khối lượng
Vì Y dư HNO3 nên mới tạo ra NO khi tiếp tục phản ứng với Fe nữa nên chắc chắn Fe lên +3 tất, O xuống -2, N từ +5 xuống +2 trong NO.
Vậy 3x = 2y + 1.344 * 3/22.4
Tại sao mình không tính luôn 1.344/22.4 vì máy tính sẽ tính cho bạn, bạn lập hệ là máy tính tự tính kết qủa. x = 0.12, y = 0.09, số mol NO = 0.06
Bây giờ các bạn chú ý đề bài lừa nè. Đây là TỐI ĐA Fe có thể tác dụng được, nên nó sẽ tác dụng với cả HNO3 cho lên +3 nhưng sau đó Fe lại tác dụng để xuống +2.
Vậy cuối cùng là Fe ở mức Fe2+.
0.12 Fe3+ tác dụng được với 0.06Fe để tạo ra Fe2+
5.04 = 0.09 mol Fe nên sẽ còn 0.03 mol tác dụng với HNO3.
0.03mol Fe cho 0.06 mol e để lên +2, nên số mol NO sẽ là 0.02.
Từ đó: NO = 0.06 + 0.02 = 0.08
Fe2+ = 0.09 + 0.12 = 0.21
HNO3 = NO3- + NO = 0.21*2 + 0.08 = 0.5
Vậy C
Đúng 0
Bình luận (2)
Cho m gam hôn hợp sắt trong không khí khoảng 1 thời gian sau thu được 7,2 gam hỗn hợp X gồm các oxit của sắt và sắt , sau đó cho hỗn hợp X vào dd H2So4 đ thu được V So2 (đktc) có số mol phản ứng của H2So4 là 0,2 mol tìm m và V. Giải giúp em với ạ :(((
Coi X gồm Fe(x mol) và O(y mol)
=> 56x + 16y = 7,2(1)
Bảo toàn electron :
3n Fe = 2n O + 2n SO2
=> n SO2 = (3x -2y)/2 = 1,5x - y(mol)
Bảo toàn nguyên tố với Fe :
n Fe2(SO4)3 = 1/2 n Fe = 0,5x(mol)
Bảo toàn nguyên tố với S :
n H2SO4 = n SO2 + 3n Fe2(SO4)3 = 1,5x - y + 0,5x.3 = 3x - y = 0,2(2)
Từ (1)(2) suy ra x = 0,1 ; y = 0,1
Vậy :
m = 0,1.56 = 5,6(gam)
n SO2 = 1,5x - y = 0,05 mol => V SO2 = 0,05.22,4 = 1,12(lít)
Đúng 1
Bình luận (0)
Coi X gồm Fe(x mol) và O(y mol)
=> 56x + 16y = 7,2(1)
Bảo toàn electron :
3n Fe = 2n O + 2n SO2
=> n SO2 = (3x -2y)/2 = 1,5x - y(mol)
Bảo toàn nguyên tố với Fe :
n Fe2(SO4)3 = 1/2 n Fe = 0,5x(mol)
Bảo toàn nguyên tố với S :
n H2SO4 = n SO2 + 3n Fe2(SO4)3 = 1,5x - y + 0,5x.3 = 3x - y = 0,2(2)
Từ (1)(2) suy ra x = 0,1 ; y = 0,1
Vậy :
m = 0,1.56 = 5,6(gam)
n SO2 = 1,5x - y = 0,05 mol => V SO2 = 0,05.22,4 = 1,12(lít)
Đúng 0
Bình luận (0)
Nung nóng m gam hỗn hợp X gồm bột Al và FexOy trong điều kiện không có không khí đến phản ứng hoàn toàn thu được hỗn hợp Y. Nghiền nhỏ, trộn đều hỗn hợp Y rồi chia thành 2 phần: - Phần 1: có khối lượng 6,025 gam được hòa tan hết trong dung dịch HNO3 loãng dư, đun nóng thu được dd Z và 0,075 mol NO (sản phẩm khử duy nhất) - Phần 2 đem tác dụng với dd NaOH dư, đun nóng thu được 0,1125 mol H2 và còn lại 8,4 gam chất rắn. Công thức của oxit sắt và giá trị của m lần lượt là: A. Fe3O4 và 13,92 B. Fe2...
Đọc tiếp
Nung nóng m gam hỗn hợp X gồm bột Al và FexOy trong điều kiện không có không khí đến phản ứng hoàn toàn thu được hỗn hợp Y. Nghiền nhỏ, trộn đều hỗn hợp Y rồi chia thành 2 phần:
- Phần 1: có khối lượng 6,025 gam được hòa tan hết trong dung dịch HNO3 loãng dư, đun nóng thu được dd Z và 0,075 mol NO (sản phẩm khử duy nhất)
- Phần 2 đem tác dụng với dd NaOH dư, đun nóng thu được 0,1125 mol H2 và còn lại 8,4 gam chất rắn. Công thức của oxit sắt và giá trị của m lần lượt là:
A. Fe3O4 và 13,92
B. Fe2O3 và 24,1
C. Fe3O4 và 19,32
D. Fe2O3 và 28,98
Đáp án B
Do P2 tác dụng với NaOH sinh ra H2 => Al dư sau phản ứng nhiệt nhôm => Y gồm Al dư, Fe, Al2O3
+P2: nAl dư=nH2/1,5=0,075 mol;
Chất rắn là Fe: nFe=8,4/56=0,15 mol
=>nAl/nFe=1/2
+ P1: Giả sử số mol
Al dư: x
Fe: 2x
BT e: 3nAl+3nFe=3nNO=>3x+3.2x=3.0,075=>x=0,025 mol
=>mAl2O3=6,025-0,025.27-0,05.56=2,55 g=>nAl2O3=0,025 mol
=>nO=3nAl2O3=0,075 mol
=>nFe/nO=0,05/0,075=2/3 (Fe2O3)
m=4mP1=6,025.4=24,1 gam
Đúng 0
Bình luận (0)
Đốt 4,2 gam sắt trong không khí thu được 5,32 gam hỗn hợp X gồm sắt và các oxit sắt. Hòa tan toàn bộ X bằng 200 ml dung dịch HNO3 a mol/l, thu được 0,448 lít khí NO (ở đktc, sản phẩm khử duy nhất của HNO3). Giá trị của a là A. 1,3 B. 1,2 C. 1,1 D. 1,5
Đọc tiếp
Đốt 4,2 gam sắt trong không khí thu được 5,32 gam hỗn hợp X gồm sắt và các oxit sắt. Hòa tan toàn bộ X bằng 200 ml dung dịch HNO3 a mol/l, thu được 0,448 lít khí NO (ở đktc, sản phẩm khử duy nhất của HNO3). Giá trị của a là
A. 1,3
B. 1,2
C. 1,1
D. 1,5
Đáp án C
Quy đổi hỗn hợp X thành Fe (0,075 mol) và O (0,07 mol)
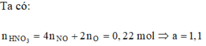
Đúng 0
Bình luận (0)
Đốt 4,2 gam sắt trong không khí thu được 5,32 gam hỗn hợp X gồm sắt và các oxit sắt. Hòa tan toàn bộ X bằng 200 ml dung dịch HNO3 a mol/l, thu được 0,448 lít khí NO (ở đktc, sản phẩm khử duy nhất của HNO3). Giá trị của a là A. 1,3. B. 1,2. C. 1,1. D. 1,5.
Đọc tiếp
Đốt 4,2 gam sắt trong không khí thu được 5,32 gam hỗn hợp X gồm sắt và các oxit sắt. Hòa tan toàn bộ X bằng 200 ml dung dịch HNO3 a mol/l, thu được 0,448 lít khí NO (ở đktc, sản phẩm khử duy nhất của HNO3). Giá trị của a là
A. 1,3.
B. 1,2.
C. 1,1.
D. 1,5.
Chọn C.
Quy đổi hỗn hợp X thành Fe (0,075 mol) và O (0,07 mol) Ta có:
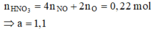
Đúng 0
Bình luận (0)
Hòa tan hết 44,0 gam hỗn hợp gồm Mg, Fe và Cu trong dung dịch HNO3 loãng dư thu được dung dịch X chứa 205,0 gam muối và hỗn hợp khí Y gồm 0,1 mol khí Z và 0,2 mol khí T. Cho dung dịch NaOH dư vào dung dịch X, lọc kết tủa nung ngoài không khí đến khối lượng không đổi thu được 64,0 gam rắn khan. Số mol HNO3 đã phản ứng là A. 3,15. B. 3,04 C. 2,85 D. 2,15
Đọc tiếp
Hòa tan hết 44,0 gam hỗn hợp gồm Mg, Fe và Cu trong dung dịch HNO3 loãng dư thu được dung dịch X chứa 205,0 gam muối và hỗn hợp khí Y gồm 0,1 mol khí Z và 0,2 mol khí T. Cho dung dịch NaOH dư vào dung dịch X, lọc kết tủa nung ngoài không khí đến khối lượng không đổi thu được 64,0 gam rắn khan. Số mol HNO3 đã phản ứng là
A. 3,15.
B. 3,04
C. 2,85
D. 2,15
hòa tan hỗn hợp A gồm 32,4 g Al và 22,4 gam Cu vào dung dịch HNO3 dư phản sau phản ứng thu được 22,4 lít hỗn hợp khí X gồm NO,NO2,N2 có khối lượng là 35,8g.tính mol của NO,số mol của HNO3 đã phản ứng
Ta có: \(n_{NO}+n_{NO_2}+n_{N_2}=\dfrac{22,4}{22,4}=1\left(mol\right)\left(1\right)\)
Mà: mX = 35,8 (g)
\(\Rightarrow30n_{NO}+46n_{NO_2}+28n_{N_2}=35,8\left(2\right)\)
Có: \(n_{Al}=\dfrac{32,4}{27}=1,2\left(mol\right)\)
\(n_{Cu}=\dfrac{22,4}{64}=0,35\left(mol\right)\)
BT e, có: 3nNO + nNO2 + 10nN2 = 3nAl + 2nCu = 4,3 (3)
Từ (1), (2) và (3) \(\Rightarrow\left\{{}\begin{matrix}n_{NO}=0,3\left(mol\right)\\n_{NO_2}=0,4\left(mol\right)\\n_{N_2}=0,3\left(mol\right)\end{matrix}\right.\)
⇒ nHNO3 = 4nNO + 2nNO2 + 12nN2 = 5,6 (mol)
Đúng 1
Bình luận (0)
cho 19,6 gam fe vào dd hno3,sau khi sắt tan hết thu được dd X và 6,72l khí no và dd X chứa a gam muối .tính a
BTNT Fe: nFe(NO3)2 + nFe(NO3)3 = nFe = 0,35 (mol) (1)
BT e, có: 2nFe(NO3)2 + 3nFe(NO3)3 = 3nNO = 0,9 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Fe\left(NO_3\right)_2}=0,15\left(mol\right)\\n_{Fe\left(NO_3\right)_3}=0,2\left(mol\right)\end{matrix}\right.\)
⇒ a = 0,15.180 + 0,2.242 = 75,4 (g)
Đúng 1
Bình luận (0)
cho m gam fe tan hết với dd hno3 thu được 6.72l no(đktc, sản phẩm khử duy nhất)và dung dịch X .số mol fe phản ứng bằng 32.5% số mol hno3 phản ứng . tính m và khối lượng fe(no3)3 trong dd X
\(n_{NO} =\dfrac{6,72}{22,4} = 0,3(mol)\\ 4H^+ +NO_3^- \to NO + 2H_2O\\ n_{HNO_3\ pư} = 4n_{NO} = 0,3.4 = 1,2(mol)\\ \Rightarrow n_{Fe\ pư} = 1,2.32,5\% = 0,39(mol)\\ \Rightarrow m = 0,39.56 = 21,84\ gam\\ n_{Fe(NO_3)_2} = a\ mol\ ;\ n_{Fe(NO_3)_3} = b\ mol\\ \Rightarrow a + b = 0,39(1)\\ BT\ e\ :2a + 3b = 0,3.3(2)\\ (1)(2) \Rightarrow a = 0,27 ; b = 0,12\\ \Rightarrow m_{Fe(NO_3)_3} = 0,12.242 = 29,04\ gam\)
Đúng 2
Bình luận (0)
cho 8.96 g fe tan hết trong dd hno2 loãng thu được dd X chứa 34.38 g chất tan. tính kl fe(no3)3 trong đd X
Đúng 0
Bình luận (0)