cho 3,36 lít oxi (đktc) phản ứng hoàn toàn với kim loại có hóa trị III thu được 10,2 gam oxit xác định tên kim loại đó
. Oxi hóa hoàn toàn một kim loại R ( chưa biết hóa trị) bảng 3,36 lít khí Oxi ở đktc, sau phản ứng thu được 10,2 gam oxit. Xác định kim loại R
giải nhanh giúp mik
Cho 3,36 lit khí oxi (ở đktc) phản ứng hoàn toàn với 1 kim loại hóa trị III thu được 10,2g oxit. Xác định tên kim loại.
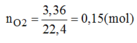
Gọi A là kí hiệu của kim loại có hóa trị III, M A là nguyên tử khối của A.
Ta có PTHH:

Theo PTHH trên ta có:
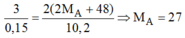
Vậy A là nhôm.
đốt cháy 1 kim loại X có hoá trị III tỏng 3,36 lít khí oxi (đktc)thu được 10,2 gam oxit .Tìm tên kim loại X
nO2 = 3,36 : 22,4 = 0,15 (mol)
pthh : 4X + 3O2 -t-> 2X2O3
0,15 0,1
=> MX2O3 = 10,2 : 0,1 = 102 (G/MOL)
=> MX = (102 - 48):2 = 27 (g/mol)
=> X là Al
Hoàn tan 10,8 gam kim loại M (hóa trị III) vào dung dịch HNO3 vừa đủ. Sau phản ứng thu được muối nitrat của kim loại và 3,36 lít khí N2O (đktc). Xác định tên kim loại M. Giúp em câu này với ạ
\(\text{Ta có }n_M=\dfrac{10,8}{M_M}\left(mol\right);n_{N_2O}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ PTHH:8M+30HNO_3\rightarrow8M\left(NO_3\right)_3+3N_2O+15H_2O\\ \Rightarrow n_M=\dfrac{8}{3}n_{N_2O}=0,4\left(mol\right)\\ \Rightarrow\dfrac{10,8}{M_M}=0,4\\ \Rightarrow M_M=27\)
Vậy M là nhôm (Al)
Clus. Cho 13,5 gam kim loại M hóa trị x tác dụng 6,72 lít O_{2} ở đktc phản ứng hoàn toàn thu được m gam chất rắn A A tác dụng với dd HCl dư thu được 3,36 lít H_{2} ở dktc . Xác định m và tên kim loại
Ta có: \(n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
BT e, có: x.nM = 4nO2 + 2nH2
\(\Rightarrow n_M=\dfrac{1,5}{x}\left(mol\right)\)
\(\Rightarrow M_M=\dfrac{13,5}{\dfrac{1,5}{x}}=9x\left(g/mol\right)\)
Với x = 3 thì MM = 27 (g/mol)
→ M là nhôm (Al)
m = mKL + mO2 = 13,5 + 0,3.32 = 23,1 (g)
`n_(O_2)=0,3(mol)`
`n_(H_2)=0,15(mol)`
`4M+xO_2 \rightarrow M_2O_x` (Đk: nhiệt độ)(1)
Từ (1) có `n_M=\frac{1,2}{x} (mol) (I)`
`\Rightarrow n_(M_(dư))=\frac{13,5}{M}-\frac{1,2}{x} (mol)`
PTHH:
`2M+2xHCl\rightarrow 2MCl_x+xH_2` (2)
Từ (2) có: `n_M=\frac{0,3}{x} (mol)(II)`
Từ (I), (II) có:
`\frac{13,5}{M}-\frac{1,2}{x}=\frac{0,3}{x}`
Với `x=3` `\Rightarrow M=27`
M là Al.
`m=102.0,1+0,1.27=12,9(g)`
đốt cháy hoàn toàn một kim loại A có hóa trị II cần vừa đủ 2.24 lít khí oxi ở đktc. Sau phản ứng thu được 6.72g Oxit. xác định kim loại A
\(n_{O_2} = \dfrac{2,24}{22,4} = 0,1(mol)\\ 2A + O_2 \xrightarrow{t^o} 2AO\\ n_{Oxit} = 2n_{O_2} = 0,2(mol)\\ \Rightarrow M_{Oxit}= A + 16 = \dfrac{6,72}{0,2}=\dfrac{168}{5}\\ \Rightarrow A = 17,6\)
(Sai đề)
Bài 1: Cho 16 gam kim loại M hóa trị II tác dụng hết với Oxi, sau phản ứng thu được 20 gam oxit. Xác định kim loại M đem phản ứng.
Bài 2: Cho 16,2 gam kim loại R hóa trị III tác dụng với clo có dư thu được 80,1 gam muối. Xác định kim loại đem phản ứng.
Bài 1:
\(n_M=\dfrac{16}{M_M}\left(mol\right)\)
PTHH: 2M + O2 --to--> 2MO
\(\dfrac{16}{M_M}\)---------->\(\dfrac{16}{M_M}\)
=> \(\dfrac{16}{M_M}\left(M_M+16\right)=20\)
=> MM = 64 (g/mol)
=> M là Cu
Bài 2:
\(n_R=\dfrac{16,2}{M_R}\left(mol\right)\)
PTHH: 2R + 3Cl2 --to--> 2RCl3
\(\dfrac{16,2}{M_R}\)------------>\(\dfrac{16,2}{M_R}\)
=> \(\dfrac{16,2}{M_R}\left(M_R+106,5\right)=80,1\)
=> MR = 27 (g/mol)
=> R là Al
1
ADDDLBTKL ta có
\(m_{O_2}=m_{MO}-m_M\\
m_{O_2}=20-16=4g\\
n_{O_2}=\dfrac{4}{32}=0,125\left(mol\right)\\
pthh:2M+O_2\underrightarrow{t^o}2MO\)
0,25 0,125
\(M_M=\dfrac{16}{0,25}=64\left(\dfrac{g}{mol}\right)\)
=> M là Cu
2
ADĐLBTKL ta có
\(m_{Cl_2}=m_{RCl_3}-m_R\\
m_{Cl_2}=80,1-16,2=63,9g\\
n_{Cl_2}=\dfrac{63,9}{71}=0,9\left(mol\right)\\
pthh:2R+3Cl_2\underrightarrow{t^o}2RCl_3\)
0,6 0,9
\(M_R=\dfrac{16,2}{0,6}=27\left(\dfrac{g}{mol}\right)\)
=> R là Al
\(1 ) 2M+O_2\rightarrow 2MO n_M=n_{MO}\Leftrightarrow \dfrac{16}{M_M}=\dfrac{20}{m_M+16} \Rightarrow m_m = 64(g/mol) \rightarrow M : Cu \)
\(2) 2R+3Cl_2\rightarrow 2RCl_3 n_R=nn_{RCl_3}\Leftrightarrow \dfrac{16,2}{M_R}=\dfrac{80,1}{M_R+35,5.3}\Rightarrow M_R = 27(g/mol)\rightarrow R:Al \)
Bài 24. Hòa tan 3,6g một kim loại A hóa trị II bằng một lượng dư axit HCl thu được 3,36 lít khí H2 (đktc). Xác định tên kim loại A
Bài 25. Hòa tan hoàn toàn 8,1g kim loại A hóa trị III trong dd HCl dư thu đucợ 10,08 lít khí H2 (đktc). Xác định tên A và m HCl đã dùng
Bài 24:
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ PTHH:A+2HCl\rightarrow ACl_2+H_2\uparrow\)
Theo pthh: nA = nH2 = 0,15 (mol)
=> MA = \(\dfrac{3,6}{0,15}=24\left(\dfrac{g}{mol}\right)\)
=> A là Mg
Bài 25:
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\\ PTHH:2A+6HCl\rightarrow2ACl_3+3H_2\uparrow\\ Mol:0,3\leftarrow0,9\leftarrow0,3\leftarrow0,45\\ \rightarrow\left\{{}\begin{matrix}M_A=\dfrac{8,1}{0,3}=27\left(\dfrac{g}{mol}\right)\Rightarrow A:Al\\m_{HCl}=0,9.36,5=32,85\left(g\right)\end{matrix}\right.\)
Bài 24.
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15mol\)
\(n_A=\dfrac{3,6}{M_A}\) mol
\(A+2HCl\rightarrow ACl_2+H_2\)
0,15 0,15 ( mol )
\(\Rightarrow\dfrac{3,6}{M_A}=0,15mol\)
\(\Leftrightarrow M_A=24\) ( g/mol )
=> A là Magie ( Mg )
Bài 25.
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45mol\)
\(n_A=\dfrac{8,1}{M_A}\) mol
\(2A+6HCl\rightarrow2ACl_3+3H_2\)
0,3 0,45 ( mol )
\(\Rightarrow\dfrac{8,1}{M_A}=0,3\)
\(\Leftrightarrow M_A=27\) g/mol
=> A là nhôm ( Al )
bài 1:cho 7,2g kim loại hóa trị II phản ứng hoàn toàn 100ml dung dịch HCL 6M. Xác định tên kim loại đã dùng
baì 2: hòa tan hoàn toàn 7,56g kim loại R có hóa trị III vào dung dịch axit HCL thu được 9,408 lít H2 (đktc). Tìm kim loại R
Giúp mik vs ạ ! Cảm ơn
Bài 1:
Gọi KL cần tìm là A.
PT: \(A+2HCl\rightarrow ACl_2+H_2\)
Ta có: \(n_{HCl}=0,1.6=0,6\left(mol\right)\)
Theo PT: \(n_A=\dfrac{1}{2}n_{HCl}=0,3\left(mol\right)\)
\(\Rightarrow M_A=\dfrac{7,2}{0,3}=24\left(g/mol\right)\)
Vậy: KL cần tìm là Mg.
Bài 2:
PT: \(2R+6HCl\rightarrow2RCl_3+3H_2\)
Ta có: \(n_{H_2}=\dfrac{9,408}{22,4}=0,42\left(mol\right)\)
Theo PT: \(n_R=\dfrac{2}{3}n_{H_2}=0,28\left(mol\right)\)
\(\Rightarrow M_R=\dfrac{7,56}{0,28}=27\left(g/mol\right)\)
Vậy: R là Al.