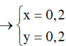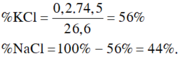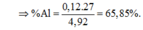Cho 0,325 hỗn hợp gồm NaCl và KCl được hòa tan vào nước. Sau đó tác dụng với dung dịch AgNO3, ta được 1 kết tủa, sấy khô đến khối lượng không đổi cân nặng 0,717 g. Thành phần phần trăm về khối lượng các chất trong hỗn hợp

Những câu hỏi liên quan
Cho 0,3 25 gam hỗn hợp NaCl và kcl được hòa tan vào HCl sau đó Cho dung dịch AgNO3 vào dung dịch trên ta được một kết tủa sấy kết tủa đến khối lượng không đổi thấy cân nặng 0,7 17 gam Tính thành phần phần trăm về khối lượng các chất trong hỗn hợp ban đầu
Gọi a ,b là số mol của NaCl và KCl.(Khi vào nước tạo dd thì số mol chấ tan không đổi )
NaCl + AgNO3 ----. AgCl + NaNO3 (1)
a mol ------------> a mol
KCl + AgNO3 -----> AgCl + KNO3 (2)
b mol ------------> b mol
ta có :
mNaCl + m KCl = 0,325
<=> 58,5 a + 74,5 b = 0,325 (*)
m AgCl PƯ1 + m AgCl PƯ2 = 0,717
<=> 143,5a + 143,5b = 0,717 (**)
ừ (*) và (**) được hệ phương rình. Giải ra được a = 0,003 => m NaCl = 0,1755 --> 54,2 %
b = 0,002 => m KCl = 0,149 --> 45,8%
Đúng 1
Bình luận (0)
Gọi a ,b là số mol của NaCl và KCl.(Khi vào nước tạo dd thì số mol chấ tan không đổi )
NaCl + AgNO3 ----. AgCl + NaNO3 (1)
a mol ------------> a mol
KCl + AgNO3 -----> AgCl + KNO3 (2)
b mol ------------> b mol
ta có :
mNaCl + m KCl = 0,325
<=> 58,5 a + 74,5 b = 0,325 (*)
m AgCl PƯ1 + m AgCl PƯ2 = 0,717
<=> 143,5a + 143,5b = 0,717 (**)
ừ (*) và (**) được hệ phương rình. Giải ra được a = 0,003 => m NaCl = 0,1755 --> 54,2 %
b = 0,002 => m KCl = 0,149 --> 45,8%
Đúng 0
Bình luận (0)
Võ Đông Anh TuấnLê Nguyên Hạo
cop bài cùng chỗ
=))
Đúng 0
Bình luận (0)
Cho 26,6 gam hỗn hợp KCl và NaCl hòa tan vào nước để được 500 gam dung dịch. Cho dung dịch trên tác dụng vừa đủ với AgNO3 thì thu được 57,4 gam kết tủa. Thành phần phần trăm theo khối lượng của KCl và NaCl trong hỗn hợp đầu là A. 34% và 66% B. 56% và 44% C. 60% và 40% D. 70% và 30%
Đọc tiếp
Cho 26,6 gam hỗn hợp KCl và NaCl hòa tan vào nước để được 500 gam dung dịch. Cho dung dịch trên tác dụng vừa đủ với AgNO3 thì thu được 57,4 gam kết tủa. Thành phần phần trăm theo khối lượng của KCl và NaCl trong hỗn hợp đầu là
A. 34% và 66%
B. 56% và 44%
C. 60% và 40%
D. 70% và 30%
Đáp án B
Đặt số mol các chất là KCl: a mol ; NaCl: b mol.

Đúng 1
Bình luận (0)
Cho 26,6 gam hỗn hợp KCl và NaCl hòa tan vào nước để được 500 gam dung dịch. Cho dung dịch trên tác dụng vừa đủ với AgNO3 thì thu được 57,4 gam kết tủa. Thành phần phần trăm theo khối lượng của KCl và NaCl trong hỗn hợp đầu là:
A. 56% và 44%.
B. 60% và 40%
C. 70% và 30%
D. 65% và 35%
Hoà tan 0,887 g hỗn hợp NaCl và KCl trong nước. Xử lí dung dịch thu được bằng một lượng dư dung dịch A g N O 3 . Kết tủa khô thu được có khối lượng 1,913 g. Tính thành phần phần trăm của từng chất trong hỗn hợp.
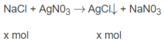
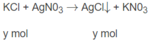
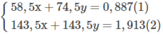
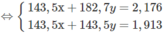
⇒ y = 6,71. 10 - 3 mol
Khối lượng KCl là : 74,5. 6,71. 10 - 3 = 0,5(g) KCl
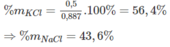
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn hỗn hợp gồm 0,2mol Fe và 0,1mol Fe2O3 vào dung dịch HCl dư thu được dung dịch A. Cho dung dịch A tác dụng với NaOH dư thu được kết tủa, rửa sạch, sấy khô và nung trong không khí đến khối lượng không đổi được m(g) chất rắn. m có giá trị là: A. 32g B. 42g C. 23g D. 24g
Đọc tiếp
Hòa tan hoàn toàn hỗn hợp gồm 0,2mol Fe và 0,1mol Fe2O3 vào dung dịch HCl dư thu được dung dịch A. Cho dung dịch A tác dụng với NaOH dư thu được kết tủa, rửa sạch, sấy khô và nung trong không khí đến khối lượng không đổi được m(g) chất rắn. m có giá trị là:
A. 32g
B. 42g
C. 23g
D. 24g
Đáp án : A
Fe;Fe2O3 -> FeCl2;FeCl3 -> Fe(OH)2;Fe(OH)3 -> Fe2O3
Bảo toàn Fe : 2nFe2O3 sau = nFe + 2nFe2O3 ban đầu
=> nFe2O3 sau = 0,2 mol
=> m = 32g
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 4,92 gam hỗn hợp A gồm (Al, Fe) trong 390 ml dung dịch HCl 2M thu được dung dịch B. Thêm 800 ml dung dịch NaOH 1M vào dung dịch B thu được kết tủa C, lọc kết tủa C, rửa sạch sấy khô nung trong không khí đến khối lượng không đổi, thu được 7,5 gam chất rắn. Phần trăm khối lượng của Al trong hỗn hợp A có giá trị gần nhất với giá trị nào sau đây? A. 85,6%. B. 65,8%. C. 20,8%. D. 16,5%
Đọc tiếp
Hòa tan hoàn toàn 4,92 gam hỗn hợp A gồm (Al, Fe) trong 390 ml dung dịch HCl 2M thu được dung dịch B. Thêm 800 ml dung dịch NaOH 1M vào dung dịch B thu được kết tủa C, lọc kết tủa C, rửa sạch sấy khô nung trong không khí đến khối lượng không đổi, thu được 7,5 gam chất rắn. Phần trăm khối lượng của Al trong hỗn hợp A có giá trị gần nhất với giá trị nào sau đây?
A. 85,6%.
B. 65,8%.
C. 20,8%.
D. 16,5%
Hòa tan hoàn toàn 4,92 gam hỗn hợp A gồm (Al, Fe) trong 390 ml dung dịch HCl 2M thu được dung dịch B. Thêm 800 ml dung dịch NaOH 1M vào dung dịch B thu được kết tủa C, lọc kết tủa C, rửa sạch sấy khô nung trong không khí đến khối lượng không đổi, thu được 7,5 gam chất rắn. Phần trăm khối lượng của Al trong hỗn hợp A có giá trị gần nhất với giá trị nào sau đây ? A. 65,8%. B. 85,6%. C. 16,5%. D. 20,8%.
Đọc tiếp
Hòa tan hoàn toàn 4,92 gam hỗn hợp A gồm (Al, Fe) trong 390 ml dung dịch HCl 2M thu được dung dịch B. Thêm 800 ml dung dịch NaOH 1M vào dung dịch B thu được kết tủa C, lọc kết tủa C, rửa sạch sấy khô nung trong không khí đến khối lượng không đổi, thu được 7,5 gam chất rắn. Phần trăm khối lượng của Al trong hỗn hợp A có giá trị gần nhất với giá trị nào sau đây ?
A. 65,8%.
B. 85,6%.
C. 16,5%.
D. 20,8%.
Câu 1: Cho 6,81 gam hỗn hợp rắn gồm NaCl và KCl hòa tan hoàn toàn vào nước được dung dịch X. Cho dung dịch X tác dụng vừa đủ với dung dịch AgNO3 thu được 14,35 gam kết tủa. Tính khối lượng mỗi muối có trong hỗn hợp rắn ban đầuCâu 2: Hòa tan 3,93 gam hỗn hợp MgCl2, KCl thành 500ml dung dịch A. Để kết tủa hết ion Cl- trong 25ml dung dịch A cần dùng 60ml dung dịch AgNO3 0,05M. Tính % khối lượng mỗi muối
Đọc tiếp
Câu 1: Cho 6,81 gam hỗn hợp rắn gồm NaCl và KCl hòa tan hoàn toàn vào nước được dung dịch X. Cho dung dịch X tác dụng vừa đủ với dung dịch AgNO3 thu được 14,35 gam kết tủa. Tính khối lượng mỗi muối có trong hỗn hợp rắn ban đầu
Câu 2: Hòa tan 3,93 gam hỗn hợp MgCl2, KCl thành 500ml dung dịch A. Để kết tủa hết ion Cl- trong 25ml dung dịch A cần dùng 60ml dung dịch AgNO3 0,05M. Tính % khối lượng mỗi muối
Câu 1:
Gọi số mol NaCl, KCl là a, b (mol)
=> 58,5a + 74,5b = 6,81 (1)
\(n_{AgCl}=\dfrac{14,35}{143,5}=0,1\left(mol\right)\)
Bảo toàn Cl: a + b = 0,1 (2)
(1)(2) => a = 0,04 (mol); b = 0,06 (mol)
\(\left\{{}\begin{matrix}m_{NaCl}=0,04.58,5=2,34\left(g\right)\\m_{KCl}=0,06.74,5=4,47\left(g\right)\end{matrix}\right.\)
Câu 2:
Gọi số mol MgCl2, KCl là a, b (mol)
=> 95a + 74,5b = 3,93 (1)
25ml dd A chứa \(\left\{{}\begin{matrix}MgCl_2:0,05a\left(mol\right)\\KCl:0,05b\left(mol\right)\end{matrix}\right.\)
nAgNO3 = 0,05.0,06 = 0,003 (mol)
=> nAgCl = 0,003 (mol)
Bảo toàn Cl: 0,1a + 0,05b = 0,003 (2)
(1)(2) => a = 0,01 (mol); b = 0,04 (mol)
\(\left\{{}\begin{matrix}\%m_{MgCl_2}=\dfrac{0,01.95}{3,93}.100\%=24,173\%\\\%m_{KCl}=\dfrac{0,04.74,5}{3,93}.100\%=75,827\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Có 26,6 g hỗn hợp gồm kcl và NaCl hòa tan hỗn hợp vào nước thành 500 gam dung dịch X Cho dung dịch X tác dụng với AgNO3 dư thì tạo thành 57,4 gam kết tủa nồng độ phần trăm mỗi muối trong dung dịch X là
Xem chi tiết
Chúc bạn học tốt !!!
\(m_{hh}=74.5a+58.5b=26.6\left(g\right)\left(1\right)\)
\(n_{AgCl}=\dfrac{57.4}{143.5}=0.4\left(mol\right)\)
\(KCl+AgNO_3\rightarrow KNO_3+AgCl\)
\(NaCl+AgNO_3\rightarrow NaNO_3+AgCl\)
\(n_{AgCl}=a+b=0.4\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):\)
\(a=b=0.2\)
\(m_{dd\left(saupư\right)}=26.6+500-57.4=469.2\left(g\right)\)
\(C\%_{KNO_3}=\dfrac{0.2\cdot101}{469.2}\cdot100\%=4.31\%\)
\(C\%_{NaNO_3}=\dfrac{0.2\cdot85}{469.2}\cdot100\%=3.62\%\)
Đúng 2
Bình luận (1)