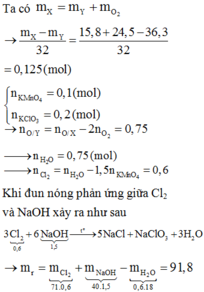Nhiệt phân 24,5 gam KClO3, khí sinh ra cho tác dụng với 32 gam Cu đun nóng . Tính khối lượng CuO tạo thành.

Những câu hỏi liên quan
Nhiệt phân hoàn toàn 24,5 gam KClO3 thu được KCl và khí O2.
a) Tính thể tích khí O2 thu được (đkc).
b) Cho toàn bộ khí O2 trên tác dụng với 32 gam Cu.
- Sau phản ứng, chất nào còn dư? Dư bao nhiêu gam?
- Tính khối lượng CuO thu được. Cho NTK: K=39, O=16; Cu = 64, Cl = 35,5.
a, PT: \(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
Ta có: \(n_{KClO_3}=\dfrac{24,5}{122,5}=0,2\left(mol\right)\)
Theo PT: \(n_{O_2}=\dfrac{3}{2}n_{KClO_3}=0,3\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,3.24,79=7,437\left(g\right)\)
b, PT: \(2Cu+O_2\underrightarrow{t^o}2CuO\)
Ta có: \(n_{Cu}=\dfrac{32}{64}=0,5\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,5}{2}< \dfrac{0,3}{1}\), ta được O2 dư.
Theo PT: \(\left\{{}\begin{matrix}n_{O_2\left(pư\right)}=\dfrac{1}{2}n_{Cu}=0,25\left(mol\right)\\n_{CuO}=n_{Cu}=0,5\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{O_2\left(dư\right)}=0,3-0,25=0,05\left(mol\right)\)
\(\Rightarrow m_{O_2\left(dư\right)}=0,05.32=1,6\left(g\right)\)
\(m_{CuO}=0,5.80=40\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 3,25 gam Zn tác dụng với dung dịch HCL dư a) Tính thể tích khí (ở đkc) thu được sau phản ứng và khối lượng muối tạo thành b) Cho lượng H2 thu được ở trên đi qua 8,0 gam bột CuO nung nóng. Tính khối lượng Cu sinh ra
\(n_{Zn}=\dfrac{m}{M}=\dfrac{3,25}{65}=0,05\left(mol\right)\)
\(PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\)
1 2 1 1
0,05 0,1 0,05 0,05
a) \(V_{H_2}=n.24,79=0,05.24,79=1,2395\left(l\right)\)
\(m_{ZnCl_2}=n.M=0,05.\left(65+35,5.2\right)=6,8\left(g\right)\)
b) \(PTHH:CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Ta cos tỉ lệ: \(\dfrac{0,1}{1}>\dfrac{0,05}{1}\Rightarrow\) CuO dư.
Theo ptr, ta có: \(n_{Cu}=n_{H_2}=0,05mol\\ \Rightarrow m_{Cu}=n.M=0,05.64=3,2\left(g\right).\)
Đúng 1
Bình luận (0)
a, PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Ta có: \(n_{Zn}=\dfrac{3,25}{65}=0,05\left(mol\right)\)
THeo PT: \(n_{ZnCl_2}=n_{H_2}=n_{Zn}=0,05\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,05.24,79=1,2395\left(l\right)\)
\(m_{ZnCl_2}=0,05.136=6,8\left(g\right)\)
b, Ta có: \(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,1}{1}>\dfrac{0,05}{1}\), ta được CuO dư.
Theo PT: \(n_{Cu}=n_{H_2}=0,05\left(mol\right)\Rightarrow m_{Cu}=0,05.64=3,2\left(g\right)\)
Đúng 1
Bình luận (0)
cho 11 gam hỗn hợp gồm al và fe tác dụng vừa đủ với đ hcl tạo 8,96 lít khí h2 thoát thành ra ở đktc. Viết pthh và tính:
a)tính % về khối lượng các chất ban đầu
b)dẫn toàn bộ khí trên qua 16 gam bột cuo đun nóng đến phản ứng kết thúc. tính cu thu được
a) PTHH: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
a_____________________\(\dfrac{3}{2}\)a (mol)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
b____________________b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}27a+56b=11\\\dfrac{3}{2}a+b=\dfrac{8,96}{22,4}=0,4\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2\cdot27}{11}\cdot100\%\approx49,09\%\\\%m_{Fe}=50,91\%\end{matrix}\right.\)
b) PTHH: \(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\\n_{H_2}=\dfrac{3}{2}a+b=0,4\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) H2 còn dư, tính theo CuO
\(\Rightarrow n_{Cu}=0,2\left(mol\right)\) \(\Rightarrow m_{Cu}=0,2\cdot64=12,8\left(g\right)\)
Đúng 3
Bình luận (1)
Gọi n Al = a ( mol ) , n Fe = b ( mol )
Có: n H2 = 0,4 ( mol )
PTHH
2AL + 6HCL ===> 2ALCL3 + 3H2
a--------------------------------------a
Fe + 2HCl ====> FeCL2 + H2
b------------------------------------b
Ta có hpt:
\(\left\{{}\begin{matrix}27a+56b=11\\1,5a+b=0,4\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
=> m AL = 5,4 ( g ) ; m Fe = 5,6 ( g )
b) Có : n CuO = 0,2 ( mol )
PTHH:
CuO + H2 ====> Cu +H2O
0,2----0,2-----------0,2
theo pthh: n Cu = 0,2 ( mol ) => m Cu = 12,8 ( g )
Đúng 1
Bình luận (1)
\(n_{H2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Pt : \(2Al+6HCl\rightarrow2AlCl_3+3H_2|\)
2 6 2 3
a 1,5a
\(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
b 1b
a) Gọi a là số mol của Al
b là số mol của Fe
\(m_{Al}+m_{Fe}=11\left(g\right)\)
⇒ \(n_{Al}.M_{Al}+n_{Fe}.M_{Fe}=11g\)
⇒ 27a + 56b = 11g (1)
Theo phương trình : 1,5a +1b = 0,4(2)
Từ (1),(2), ta có hệ phương trình :
27a + 56b = 11
1,5a + 1b = 0,4
⇒ \(\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
\(m_{Al}=0,2.27=5,4\left(g\right)\)
\(m_{Fe}=0,1.56=5,6\left(g\right)\)
0/0Al = \(\dfrac{5,4.100}{11}=49,09\)0/0
0/0Fe = \(\dfrac{5,6.100}{11}=50,91\)0/0
b) Pt : \(H_2+CuO\rightarrow\left(t_o\right)Cu+H_2O|\)
1 1 1 1
0,4 0,4
\(n_{Cu}=\dfrac{0,4.1}{1}=0,4\left(mol\right)\)
⇒ \(m_{Cu}=0,4.64=25,6\left(g\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (2)
Nung nóng hỗn hợp X gồm 15,8 gam KMnO4 và 24,5 gam KClO3 một thời gian thu được 36,3 gam hỗn hợp Y gồm 6 chất. Cho Y tác dụng với dung dịch HCl đặc dư đun nóng lượng khí clo sinh ra cho hấp thụ vào 300 ml dung dịch NaOH 5M đun nóng thu được dung dịch Z. Cô cạn Z được chất rắn khan các phản ứng xảy ra hoàn toàn. Khối lượng chất rắn khan (gam) thu được là A. 111 B. 12 C. 79,8 D. 91,8
Đọc tiếp
Nung nóng hỗn hợp X gồm 15,8 gam KMnO4 và 24,5 gam KClO3 một thời gian thu được 36,3 gam hỗn hợp Y gồm 6 chất. Cho Y tác dụng với dung dịch HCl đặc dư đun nóng lượng khí clo sinh ra cho hấp thụ vào 300 ml dung dịch NaOH 5M đun nóng thu được dung dịch Z. Cô cạn Z được chất rắn khan các phản ứng xảy ra hoàn toàn. Khối lượng chất rắn khan (gam) thu được là
A. 111
B. 12
C. 79,8
D. 91,8
Nung nóng hỗn hợp gồm 15,8 gam KMnO4 và 24,5 gam KClO3 một thời gian thu được 36,3 gamhỗn hợp Y gồm 6 chất. Cho Y tác dụng với dung dịch HCl đặc dư đun nóng lượng khí clo sinh ra cho hấpthụ vào 300 ml dung dịch NaOH 5M đun nóng thu được dung dịch Z. Cô cạn Z được chất rắn khan cácphản ứng xảy ra hoàn toàn. Khối lượng chất rắn khan thu được là?
Em có thể tham khảo cách giải sau:
Ta có: mO2 = (15,8 + 24,5)-36,3 = 4 gam. => nO2 = 0,125 mol.
nKMnO4 = 0,1 mol, nKClO3 = 0,2 mol.
Mn7+ + 5e -> Mn2+
Cl5+ + 6e -> Cl-1
2O2- -> O2 + 4e
2Cl-1 -> Cl2 + 2e
Bảo toàn electron, ta có: 0,1*5 + 0,2*6 = 0,125*4 + 2*nCl2
=> nCl2 =0,6 mol.
3Cl2 + 6NaOH -> 5NaCl + NaClO3 + 3H2O (vì đun nóng).
Bđ 0,6 1,5
P/ư 0,6 1,2 1,0 0,2
Sau p/ư 0 0,3 1,0 0,2.
=> m Rắn =0,3*40 + 1,0*58,5 + 0,2*106,5 = 91,8 gam.
Đúng 0
Bình luận (0)
Bài 6 PT nhiệt phân theo sơ đồ sau: Sample picture a) Tính thể tích khí oxi (đktc) thu được khi nhiệt phân 31,6 g KmnO4. b) Tính khối lượng CuO được tạo thành khi cho lượng khí oxi sinh ra ở trên tác dụng hết với Cu.
Nung nóng hỗn hợp gồm 15,8 gam KMnO4 và 24,5 gam KClO3 một thời gian thu được 36,3 gam hỗn hợp Y gồm 6 chất. Cho Y tác dụng với dung dịch HCl đặc dư, đun nóng, lượng khí clo sinh ra cho thụ vào 300ml dung dịch NaOH 5M đun nóng thu được dung dịch Z. Cô cạn Z thu được m gam chất rắn khan. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là: A. 12 gam B. 91,8 gam C. 111 gam D. 79,8 gam
Đọc tiếp
Nung nóng hỗn hợp gồm 15,8 gam KMnO4 và 24,5 gam KClO3 một thời gian thu được 36,3 gam hỗn hợp Y gồm 6 chất. Cho Y tác dụng với dung dịch HCl đặc dư, đun nóng, lượng khí clo sinh ra cho thụ vào 300ml dung dịch NaOH 5M đun nóng thu được dung dịch Z. Cô cạn Z thu được m gam chất rắn khan. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là:
A. 12 gam
B. 91,8 gam
C. 111 gam
D. 79,8 gam
Đáp án B
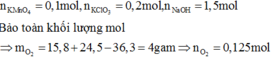
Khi cho hỗn hợp Y phản ứng với HCl đặc sẽ xảy ra phản ứng oxi hóa – khử tạo ra Cl2
![]()

Đúng 0
Bình luận (0)
Cho 12,8 gam Cu tác dụng với dung dịch H2SO4 đặc nóng dư, khí sinh ra hấp thụ vào 200 ml dung dịch NaOH 2M. Hỏi muối nào được tạo thành và khối lượng là bao nhiêu gam? A. Na2SO3 và23,2 gam. B. Na2SO3 và 24,2 gam. C. Na2SO3 và 25,2 gam. D. NaHSO3 15 gam và Na2SO3 26,2 gam.
Đọc tiếp
Cho 12,8 gam Cu tác dụng với dung dịch H2SO4 đặc nóng dư, khí sinh ra hấp thụ vào 200 ml dung dịch NaOH 2M. Hỏi muối nào được tạo thành và khối lượng là bao nhiêu gam?
A. Na2SO3 và23,2 gam.
B. Na2SO3 và 24,2 gam.
C. Na2SO3 và 25,2 gam.
D. NaHSO3 15 gam và Na2SO3 26,2 gam.
Đáp án C
Bảo toàn e : 2nCu = 2nSO2 => nSO2 = 0,2 mol
nNaOH = 0,4 mol = 2nSO2
=> Chỉ có phản ứng : 2NaOH + SO2 -> Na2SO3 + H2O
=> mNa2SO3 = 25,2g
Đúng 0
Bình luận (0)
Cho 6,5 g kim loại kẽm phản ứng hết với dung dịch axit clohiđric a viết phương trình hóa học xảy ra b tính thể tích khí H2 dkt C sinh ra C lượng khí H2 sinh ra từ phản ứng trên cho tác dụng với 12 gam CuO nung nóng tính khối lượng Cu thu được
a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Zn}=0,1\left(mol\right)\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
c, \(n_{CuO}=\dfrac{12}{80}=0,15\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,15}{1}>\dfrac{0,1}{1}\), ta được CuO dư.
Theo PT: \(n_{Cu}=n_{H_2}=0,1\left(mol\right)\Rightarrow m_{Cu}=0,1.64=6,4\left(g\right)\)
Đúng 2
Bình luận (0)