
Những câu hỏi liên quan
Đốt cháy hỗn hợp gồm 1,68g Mg và 2,16g Al với khí X gồm O2 và Cl2, sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua. Hòa tan Y bằng một lượng vừa đủ 120 ml dung dịch HCl 2M, thu được dung dịch Z. Tính % thể tích khí Cl2 trong hỗn hợp X
\(n_{Mg}=0,07mol;n_{Al}=0,08mol\\ n_{Cl_2}=a;n_{O_2}=b\\ 2H^++O^{2-}->H_2O\\ n_{H^+}=0,12\cdot\dfrac{2}{2}=2b\\ b=0,06mol\\ BTDT:0,07\cdot2+0,08\cdot3=2a+4b\\ a=0,07\\ \%V_{Cl_2}=\dfrac{a}{a+b}=53,85\%\)
Đúng 1
Bình luận (0)
Đốt cháy hỗn hợp gồm 1,68 gam Mg và 2,16 gam Al với khí X gồm O2 và Cl2 sauphản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua. Hòa tan Y bằng một lượng vừa đủ 120 mldung dịch HCl 2M, thu được dung dịch Z. Tính % thể tích khí Cl2 trong hỗn hợp X
Đốt cháy hỗn hợp gồm 1,68 gam Mg và 2,16 gam Al với khí X gồm O2 và Cl2 sauphản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua. Hòa tan Y bằng một lượng vừa đủ 120 mldung dịch HCl 2M, thu được dung dịch Z. Tính % thể tích khí Cl2 trong hỗn hợp X?
\(n_{HCl}=0,12.2=0,24\left(mol\right)\)
=> \(n_{H_2O}=0,12\left(mol\right)\)
=> \(n_{O\left(oxit\right)}=0,12\left(mol\right)\)
=> \(n_{O_2}=0,06\left(mol\right)\)
\(n_{Mg}=\dfrac{1,68}{24}=0,07\left(mol\right)\); \(n_{Al}=\dfrac{2,16}{27}=0,08\left(mol\right)\)
Gọi số mol Cl2 là x (mol)
Mg0 - 2e --> Mg+2
0,07->0,14
Al0 - 3e --> Al+3
0,08->0,24
O20 + 4e --> 2O-2
0,06->0,24
Cl20 + 2e --> 2Cl-
x--->2x
Bảo toàn e: 2x + 0,24 = 0,24 + 0,14
=> x = 0,07 (mol)
=> \(\%V_{Cl_2}=\dfrac{0,07}{0,06+0,07}.100\%=53,846\%\)
Đúng 4
Bình luận (0)
Đốt cháy hỗn hợp gồm 1,92 gam Mg và 4,48 gam Fe với hỗn hợp khí X gồm clo và oxi, sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua (không còn khí dư). Hòa tan Y bằng một lượng vừa đủ 120 ml dung dịch HCl 2M, thu được dung dịch Z. Cho AgNO3 dư vào dung dịch Z, thu được 56,69 gam kết tủa. Phần trăm thể tích của clo trong hỗn hợp X là: A. 51,72% B. 76,70% C. 53,85% D. 56,36%
Đọc tiếp
Đốt cháy hỗn hợp gồm 1,92 gam Mg và 4,48 gam Fe với hỗn hợp khí X gồm clo và oxi, sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua (không còn khí dư). Hòa tan Y bằng một lượng vừa đủ 120 ml dung dịch HCl 2M, thu được dung dịch Z. Cho AgNO3 dư vào dung dịch Z, thu được 56,69 gam kết tủa. Phần trăm thể tích của clo trong hỗn hợp X là:
A. 51,72%
B. 76,70%
C. 53,85%
D. 56,36%
Chọn C
nMg = 0,08 mol ; nFe = 0,08 mol
Khi phản ứng với X thì có x mol Cl2 và y mol O2 phản ứng
Giả sử tạo a mol Fe2+ và (0,08 – a) mol Fe3+
Bảo toàn điện tích : 2.0,08 + 2a + 3(0,08 – a) = 2x + 4y
Hòa tan Y bằng HCl : 2Cl thay thế 1 O => nO = ½ nHCl = 0,12 mol = 2y
=> 0,4 – a = 2x + 4.0,06 (1)
,Sau đó : phản ứng với AgNO3 tạo : (2x + 0,24) mol AgCl và a mol Ag
=> 56,69 = 143,5(2x + 0,24) + 108a (2)
Từ (1),(2) => x = 0,07 ; a = 0,02 mol
=> %VCl2(X) = 53,85%
Đúng 0
Bình luận (0)
Đốt cháy hỗn hợp gồm 1,92 gam Mg và 4,48 gam Fe với hỗn hợp khí X gồm clo và oxi, sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua (không còn khí dư). Hòa tan Y bằng một lượng vừa đủ 120 ml dung dịch HCl 2M, thu được dung dịch Z. Cho dung dịch Z tác dụng hoàn toàn với lượng dư AgNO3, thu được 56,69gam kết tủa. Phần trăm thể tích của clo trong hỗn hợp X gần với giá trị nào nhất sau đây? A. 56%. B. 54%. C. 52%. D. 76%.
Đọc tiếp
Đốt cháy hỗn hợp gồm 1,92 gam Mg và 4,48 gam Fe với hỗn hợp khí X gồm clo và oxi, sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua (không còn khí dư). Hòa tan Y bằng một lượng vừa đủ 120 ml dung dịch HCl 2M, thu được dung dịch Z. Cho dung dịch Z tác dụng hoàn toàn với lượng dư AgNO3, thu được 56,69gam kết tủa. Phần trăm thể tích của clo trong hỗn hợp X gần với giá trị nào nhất sau đây?
A. 56%.
B. 54%.
C. 52%.
D. 76%.
Đốt cháy hỗn hợp gồm 0,08 mol Mg và 0,08 mol Fe trong hỗn hợp khí X gồm Cl2 và O2, sau khi kết thúc phản ứng thu được hỗn hợp Y gồm các oxit và muối clorua (không còn khí dư). Hòa tan toàn bộ Y cần vừa đủ 120 ml dung dịch HCl 2M, thu được dung dịch Z. Cho dung dịch AgNO3 dư vào Z, thu được 56,69 gam kết tủa. Phần trăm thể tích của O2 trong X có giá trị gần nhất với giá trị nào sau đây? A. 46 B.76. C.53. D.56.
Đọc tiếp
Đốt cháy hỗn hợp gồm 0,08 mol Mg và 0,08 mol Fe trong hỗn hợp khí X gồm Cl2 và O2, sau khi kết thúc phản ứng thu được hỗn hợp Y gồm các oxit và muối clorua (không còn khí dư). Hòa tan toàn bộ Y cần vừa đủ 120 ml dung dịch HCl 2M, thu được dung dịch Z. Cho dung dịch AgNO3 dư vào Z, thu được 56,69 gam kết tủa. Phần trăm thể tích của O2 trong X có giá trị gần nhất với giá trị nào sau đây?
A. 46
B.76.
C.53.
D.56.
Đáp án A
Mol Mg = mol Fe = 0,08 và mol HCl = 0,24
Mg - 2e ---> Mg2+
0,08--0,16
Fe - 3e ---> Fe3+
0,08--0,24
Cl2 + 2e ---> 2 Cl-
a-----2a---------2a
O2 + 4e ---> 2 O2-
b-------4b--------2b
Ag+ + e ---> Ag
x--------x---------x
2 H+ + O2- --> H2O
0,24----0,12
mol O = 2b = 0,12 ==>> b = 0,06
Bảo toàn mol e : 2a + 4b + x = 0,16 + 0,24 = 0,40 ==> 2a + x = 0,16
Kết tủa gồm : AgCl (2a + 0,24) mol và Ag x mol
==> 143,5(2a+0,24) + 108x = 56,69 ==> 287a + 108x = 22,25
===> a = 0,07 và x = 0,02
==> X gồm 0,07 mol Cl2 và 0,06 mol O2 ===> %mol O2 = 46,15
Đúng 0
Bình luận (0)
Đốt cháy hỗn hợp gồm 0,08 mol Mg và 0,08 mol Fe trong hỗn hợp khí X gồm Cl2 và O2, sau khi kết thúc phản ứng thu được hỗn hợp Y gồm các oxit và muối clorua (không còn khí dư). Hòa tan toàn bộ Y cần vừa đủ 120 ml dung dịch HCl 2M, thu được dung dịch Z. Cho dung dịch AgNO3 dư vào Z, thu được 56,69 gam kết tủa. Phần trăm thể tích của O2 trong X có giá trị gần nhất với giá trị nào sau đây? A. 46. B.76. C.53. D.56.
Đọc tiếp
Đốt cháy hỗn hợp gồm 0,08 mol Mg và 0,08 mol Fe trong hỗn hợp khí X gồm Cl2 và O2, sau khi kết thúc phản ứng thu được hỗn hợp Y gồm các oxit và muối clorua (không còn khí dư). Hòa tan toàn bộ Y cần vừa đủ 120 ml dung dịch HCl 2M, thu được dung dịch Z. Cho dung dịch AgNO3 dư vào Z, thu được 56,69 gam kết tủa. Phần trăm thể tích của O2 trong X có giá trị gần nhất với giá trị nào sau đây?
A. 46.
B.76.
C.53.
D.56.
Đáp án A
Mol Mg = mol Fe = 0,08 và mol HCl = 0,24
Mg - 2e ---> Mg2+
0,08--0,16
Fe - 3e ---> Fe3+
0,08--0,24
Cl2 + 2e ---> 2 Cl-
a-----2a---------2a
O2 + 4e ---> 2 O2-
b-------4b--------2b
Ag+ + e ---> Ag
x--------x---------x
2 H+ + O2- --> H2O
0,24----0,12
mol O = 2b = 0,12 ==>> b = 0,06
Bảo toàn mol e : 2a + 4b + x = 0,16 + 0,24 = 0,40 ==> 2a + x = 0,16
Kết tủa gồm : AgCl (2a + 0,24) mol và Ag x mol
==> 143,5(2a+0,24) + 108x = 56,69 ==> 287a + 108x = 22,25
===> a = 0,07 và x = 0,02
==> X gồm 0,07 mol Cl2 và 0,06 mol O2 ===> %mol O2 = 46,15
Đúng 0
Bình luận (0)
Đốt cháy hỗn hợp gồm l,92g Mg và 4,48g Fe với hỗn hợp khí X gồm O2và Cl2. Sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua ( không còn khí dư). Hòa tan Y bằng 120ml dung dịch HCl 2M (vừa đủ) thu được dung dịch Z.. Cho AgNO3 (dư) vào Zthu được 56,69g kết tủa. Phần trăm thể tích khí Cl2 trong hỗn hợp X là. A.51,72% B.76,70% C.53,85% D.56,36%
Đọc tiếp
Đốt cháy hỗn hợp gồm l,92g Mg và 4,48g Fe với hỗn hợp khí X gồm O2và Cl2. Sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua ( không còn khí dư). Hòa tan Y bằng 120ml dung dịch HCl 2M (vừa đủ) thu được dung dịch Z.. Cho AgNO3 (dư) vào Zthu được 56,69g kết tủa. Phần trăm thể tích khí Cl2 trong hỗn hợp X là.
A.51,72%
B.76,70%
C.53,85%
D.56,36%
Đáp án C:
![]()
![]()
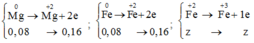
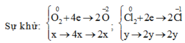
Bảo toàn electron ta có: ne cho= nenhận
![]()
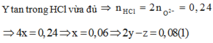
Y tác dụng với AgNO3.
Quá trình trao đổi electron:
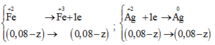
Tạo kết tủa AgCl và Ag => m kết tủa = mAgCl + mAg
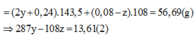
(1) và(2)=>y = 0,07; z = 0,06
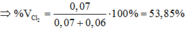
Đúng 0
Bình luận (0)
Đốt cháy hỗn hợp gồm 1,92 gam Mg và 4,48 gam Fe với khí X gồm O2 và Cl2 sau pư chỉ thu được hh Y gồm các oxit và muối clorua ( không còn khí dư). Hòa tan Y bằng một lượng vừa đủ 120 ml dd HCl 2M, thu được dd Z. Cho AgNO3 dư vào dd Z thu được 56,69 gam kết tủa. Tính % thể tích clo trong hỗn hợp X A. 76,7% B. 56,36% C. 51,72% D. 53,85%
Đọc tiếp
Đốt cháy hỗn hợp gồm 1,92 gam Mg và 4,48 gam Fe với khí X gồm O2 và Cl2 sau pư chỉ thu được hh Y gồm các oxit và muối clorua ( không còn khí dư). Hòa tan Y bằng một lượng vừa đủ 120 ml dd HCl 2M, thu được dd Z. Cho AgNO3 dư vào dd Z thu được 56,69 gam kết tủa. Tính % thể tích clo trong hỗn hợp X
A. 76,7%
B. 56,36%
C. 51,72%
D. 53,85%
Đáp án : D
nMg = 0,08 mol ; nFe = 0,08 mol
Khi phản ứng với X thì có x mol Cl2 và y mol O2 phản ứng
Giả sử tạo a mol Fe2+ và (0,08 – a) mol Fe3+
Bảo toàn điện tích : 2.0,08 + 2a + 3(0,08 – a) = 2x + 4y
Hòa tan Y bằng HCl : 2Cl thay thế 1 O => nO = ½ nHCl = 0,12 mol = 2y
=> 0,4 – a = 2x + 4.0,06 (1)
,Sau đó : phản ứng với AgNO3 tạo : (2x + 0,24) mol AgCl và a mol Ag
=> 56,69 = 143,5(2x + 0,24) + 108a (2)
Từ (1),(2) => x = 0,07 ; a = 0,02 mol
=> %VCl2(X) = 53,85%
Đúng 0
Bình luận (0)












