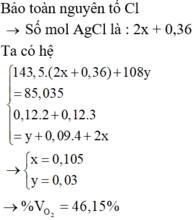đốt 6.45 gam hỗn hợp x gồm mg và al trong bình chứa 3.36 lít hôn hợp O2 và Cl2 thu được chất rắn Y. Để hòa tan hoàn toàn Y người ta cần vừa đủ 450 ml HCl 1M sau phản ứng thu được 2.8l H2 và dung dịch Z. Tính khối lượng Mg trong hỗn hợp ban đầu

Những câu hỏi liên quan
Tiến hành phản ứng nhiệt nhôm hỗn hợp X gồm Al và Cr2O3, sau một thời gian thu được 15,4 gam chất rắn Y. Để hòa tan hoàn toàn Y cần vừa đủ 450 ml dung dịch HCl 2M, thu được dung dịch Z và 1,344 lít khí H2 (đktc). Dung dịch Z phản ứng tối đa với dung dịch chứa m gam NaOH. Các phản ứng thực hiện trong khí trơ. Giá trị của m là A. 37,6. B. 36,0. C. 34,8. D. 40,8.
Đọc tiếp
Tiến hành phản ứng nhiệt nhôm hỗn hợp X gồm Al và Cr2O3, sau một thời gian thu được 15,4 gam chất rắn Y. Để hòa tan hoàn toàn Y cần vừa đủ 450 ml dung dịch HCl 2M, thu được dung dịch Z và 1,344 lít khí H2 (đktc). Dung dịch Z phản ứng tối đa với dung dịch chứa m gam NaOH. Các phản ứng thực hiện trong khí trơ. Giá trị của m là
A. 37,6.
B. 36,0.
C. 34,8.
D. 40,8.
Đáp án : D
Sau phản ứng nhiệt nhôm thu được : x mol Al ; y mol Cr2O3 ; z mol Cr và t mol Al2O3
Do phản ứng hoàn toàn nên Y không có Al hoặc không có Cr2O3
=> Bảo toàn khối lượng : mX = mY = 27.(x+2t) + 152.(y+0,5z) = 15,4g (1)
nHCl = 3nAl + 6nAl2O3 + 6nCr2O3 + 2nCr = 3x + 6t + 6y + 2z = 0,9 mol (2)
,nH2 = 1,5nAl + nCr => 3x + 2z = 0,06.2 = 0,12 mol (3)
Từ (2),(3) => y + t = 0,13 mol
=> nNaOH = 4nAlCl3 + 4nCrCl3 + 2nCrCl2 = 4(x+2t) + 4.2y + 2z = 8y + 8t + 4x + 2z
+) TH1 : Không có Al => x = 0 => z = 0,06 mol
=> 54t + 152y = 10,84g và t + y = 0,13
=> t = 0,09 và y = 0,04 => nNaOH pứ = 1,02 mol => m =40,8g
+)TH2 : Không có Cr2O3 => y = 0 => t = 0,13 mol
=> 27x + 76z = 8,38g và 3x + 2z = 0,06
=> x = - 0,07 mol (L)
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Al và
Fe
2
O
3
.Nếu cho m gam hỗn hợp X tác dụng với dung dịch HCl dư thu được 2,688 lít khí
H
2
(đktc).Nếu nung nóng m gam hỗn hợp X để thực hiện phản ứng nhiệt nhôm hoàn toàn, thu được chất rắn Y. Hòa tan hết chất rắn Y với dung dịch NaOH dư thu được 0,336 lít
H
2
(đktc).Để hòa tan hết m gam hỗn hợp X cần bao nhiêu...
Đọc tiếp
Hỗn hợp X gồm Al và Fe 2 O 3 .
Nếu cho m gam hỗn hợp X tác dụng với dung dịch HCl dư thu được 2,688 lít khí H 2 (đktc).
Nếu nung nóng m gam hỗn hợp X để thực hiện phản ứng nhiệt nhôm hoàn toàn, thu được chất rắn Y. Hòa tan hết chất rắn Y với dung dịch NaOH dư thu được 0,336 lít H 2 (đktc).
Để hòa tan hết m gam hỗn hợp X cần bao nhiêu ml dung dịch A chứa HCl 1M và H 2 SO 4 0,5M ?
A. 300 ml
B. 225 ml
C. 360 ml
D. 450 ml
Hỗn hợp X gồm Al và
Fe
2
O
3
.Nếu cho m gam hỗn hợp X tác dụng với dung dịch HCl dư thu được 13,44 lít khí
H
2
(đktc).Nếu nung nóng m gam hỗn hợp X để thực hiện phản ứng nhiệt nhôm hoàn toàn, thu được chất rắn Y. Hòa tan hết chất rắn Y với dung dịch NaOH dư thu được 3,36 lít
H
2
(đktc).Để hòa tan hết m gam hỗn hợp X cần bao nhiêu...
Đọc tiếp
Hỗn hợp X gồm Al và Fe 2 O 3 .
Nếu cho m gam hỗn hợp X tác dụng với dung dịch HCl dư thu được 13,44 lít khí H 2 (đktc).
Nếu nung nóng m gam hỗn hợp X để thực hiện phản ứng nhiệt nhôm hoàn toàn, thu được chất rắn Y. Hòa tan hết chất rắn Y với dung dịch NaOH dư thu được 3,36 lít H 2 (đktc).
Để hòa tan hết m gam hỗn hợp X cần bao nhiêu ml dung dịch A chứa HCl 2M và H 2 SO 4 1M ?
A. 500 ml
B. 525 ml
C. 360 ml
D. 450 ml
Cho 9,6 gam hỗn hợp gồm Mg và Fe có tỉ lệ mol 1:1 phản ứng với hỗn hợp khí X gồm Cl2 và O2, sau phản ứng chỉ thu được hỗn hợp rắn gồm các oxit và muối clorua, không còn khí dư. Hòa tan hoàn toàn hỗn hợp sản phẩm bằng một lượng vừa đủ 360 ml dung dịch HCl 1M, thu được dung dịch Y. Cho AgNO3 dư vào dung dịch Y, thu được 85,035 gam kết tủa. Phần trăm thể tích của O2 trong hỗn hợp X là A. 48,28%. B. 23,3%. C. 46,15%. D. 43,64%.
Đọc tiếp
Cho 9,6 gam hỗn hợp gồm Mg và Fe có tỉ lệ mol 1:1 phản ứng với hỗn hợp khí X gồm Cl2 và O2, sau phản ứng chỉ thu được hỗn hợp rắn gồm các oxit và muối clorua, không còn khí dư. Hòa tan hoàn toàn hỗn hợp sản phẩm bằng một lượng vừa đủ 360 ml dung dịch HCl 1M, thu được dung dịch Y. Cho AgNO3 dư vào dung dịch Y, thu được 85,035 gam kết tủa. Phần trăm thể tích của O2 trong hỗn hợp X là
A. 48,28%.
B. 23,3%.
C. 46,15%.
D. 43,64%.
Hỗn hợp bột X gồm Al và
Fe
2
O
3
- Nếu cho m gam hỗn hợp X tác dụng hết với dung dịch HCl thu được 5,376 lít
H
2
(đktc). - Nếu nung nóng m gam hỗn hợp X để thực hiện hoàn toàn phản ứng nhiệt nhôm, thu được chất rắn Y. Hòa tan hết Y trong NaOH dư thu được 0,672 lít
H
2
(đktc). - Để hòa tan hết m gam X cần V ml dung dịch hỗn hợp HCl...
Đọc tiếp
Hỗn hợp bột X gồm Al và Fe 2 O 3
- Nếu cho m gam hỗn hợp X tác dụng hết với dung dịch HCl thu được 5,376 lít H 2 (đktc).
- Nếu nung nóng m gam hỗn hợp X để thực hiện hoàn toàn phản ứng nhiệt nhôm, thu được chất rắn Y. Hòa tan hết Y trong NaOH dư thu được 0,672 lít H 2 (đktc).
- Để hòa tan hết m gam X cần V ml dung dịch hỗn hợp HCl 1M và H 2 SO 4 0,5M. Giá trị của V là
A, 300 ml
B. 450 ml
C. 360 ml
D. 600 ml
Cho 9,6 gam hỗn hợp gồm Mg và Fe có tỉ lệ mol 1:1 phản ứng với hỗn hợp khí X gồm Cl2 và O2, sau phản ứng chỉ thu được hỗn hợp rắn gồm các oxit và muối clorua, không còn khí dư. Hòa tan hoàn toàn hỗn hợp sản phẩm bằng một lượng vừa đủ 360ml dung dịch HCl 1M, thu được dung dịch Y. Cho AgNO3 dư vào dung dịch Y, thu được 85,035 gam kết tủa. Phần trăm thể tích của O2 trong hỗn hợp X là: A. 48,18% B. 23,3% C. 46,15% D. 43,64%
Đọc tiếp
Cho 9,6 gam hỗn hợp gồm Mg và Fe có tỉ lệ mol 1:1 phản ứng với hỗn hợp khí X gồm Cl2 và O2, sau phản ứng chỉ thu được hỗn hợp rắn gồm các oxit và muối clorua, không còn khí dư. Hòa tan hoàn toàn hỗn hợp sản phẩm bằng một lượng vừa đủ 360ml dung dịch HCl 1M, thu được dung dịch Y. Cho AgNO3 dư vào dung dịch Y, thu được 85,035 gam kết tủa. Phần trăm thể tích của O2 trong hỗn hợp X là:
A. 48,18%
B. 23,3%
C. 46,15%
D. 43,64%
Đáp án C
nMg=nFe=9,6/(24+56)=0,12 mol
nO=nH+/2=0,36/2=0,18 mol => nO2=0,09 mol
nCl2=z
Giả sử trong Y:
Fe2+: x
Fe3+: y
Cl-: 2z+0,36 (BTNT Cl)
Fe2+ + Ag+ → Fe3+ + Ag
x x
Ag+ + Cl- → AgCl
2z+0,36 2z+0,36
BTNT Fe: x+y=0,12 (1)
BT e: 0,12.2+2x+3y=2z+0,18.2 (2)
m kết tủa = 108x+143,5(2z+0,36) = 85,035 (3)
Giải hệ pt ta được: x=0,03; y=0,09; z=0,105
%VO2=0,09/(0,09+0,105)=46,15%
Đúng 0
Bình luận (0)
Đốt cháy hỗn hợp gồm 1,68g Mg và 2,16g Al với khí X gồm O2 và Cl2, sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua. Hòa tan Y bằng một lượng vừa đủ 120 ml dung dịch HCl 2M, thu được dung dịch Z. Tính % thể tích khí Cl2 trong hỗn hợp X...
Xem chi tiết
\(n_{H^+} = n_{HCl} = 0,12.2 = 0,24(mol)\\ 2H^+ + O^{2-} \to H_2O\\ n_{O(oxit)} = \dfrac{1}{2}n_{H^+} = 0,12(mol)\\ \Rightarrow n_{O_2} = \dfrac{n_{O(oxit)}}{2} = 0,06(mol)\\ n_{Mg} = \dfrac{1,68}{24} = 0,07(mol) ; n_{Al} = \dfrac{2,16}{27} = 0,08(mol)\)
Bảo toàn electron :
\(2n_{Mg} + 3n_{Al} = 4n_{O_2} + 2n_{Cl_2}\\ \Rightarrow n_{Cl_2} = \dfrac{0,07.2 + 0,08.3-0,06.4}{2} = 0,07(mol)\\ \Rightarrow \%V_{Cl_2} = \dfrac{0,07}{0,07+0,06}.100\% = 53,85\%\)
Đúng 3
Bình luận (2)
Đốt cháy hỗn hợp gồm 1,68g Mg và 2,16g Al với khí X gồm O2 và Cl2, sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua. Hòa tan Y bằng một lượng vừa đủ 120 ml dung dịch HCl 2M, thu được dung dịch Z. Tính % thể tích khí Cl2 trong hỗn hợp X
\(n_{Mg}=0,07mol;n_{Al}=0,08mol\\ n_{Cl_2}=a;n_{O_2}=b\\ 2H^++O^{2-}->H_2O\\ n_{H^+}=0,12\cdot\dfrac{2}{2}=2b\\ b=0,06mol\\ BTDT:0,07\cdot2+0,08\cdot3=2a+4b\\ a=0,07\\ \%V_{Cl_2}=\dfrac{a}{a+b}=53,85\%\)
Đúng 1
Bình luận (0)
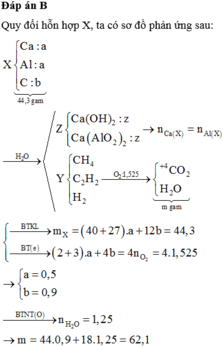
Hòa tan 44,3 gam hỗn hợp X gồm Ca, CaC2, Al và Al4C3 vào nước (dư), sau phản ứng, thu được hỗn hợp khí Y và dung dịch Z trong suốt, chỉ chứa 2 chất tan có cùng nồng độ mol. Đốt cháy hoàn toàn Y cần vừa đủ 34,16 lít O2 (đktc), thu được m gam hỗn hợp CO2 và H2O. Giá trị của m là A. 66,5. B. 62,1. C. 57,6. D. 61,2.
Đọc tiếp
Hòa tan 44,3 gam hỗn hợp X gồm Ca, CaC2, Al và Al4C3 vào nước (dư), sau phản ứng, thu được hỗn hợp khí Y và dung dịch Z trong suốt, chỉ chứa 2 chất tan có cùng nồng độ mol. Đốt cháy hoàn toàn Y cần vừa đủ 34,16 lít O2 (đktc), thu được m gam hỗn hợp CO2 và H2O. Giá trị của m là
A. 66,5.
B. 62,1.
C. 57,6.
D. 61,2.