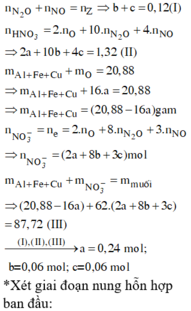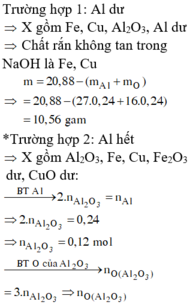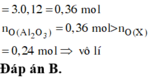Cho hỗn hợp A gồm 16g \(Fe_2O_3\) và 6,4g CuO vào 160ml dung dịch \(H_2SO_4\) 2M Sau phản ứng thấy còn m gam rắn không tan a) tính m b) tính thể tích dung dịch hỗn hợp gồm axit HCl 1M và axit\(H_2SO_4\) 0.5M cần dùng để phản ứng hết hỗn hợp A
a) \(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right);n_{CuO}=\dfrac{6,4}{80}=0,08\left(mol\right)\)
\(n_{H_2SO_4}=0,16.2=0,32\left(mol\right)\)
TH1 Fe2O3 phản ứng trước CuO dư
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
0,1------------->0,3
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
0,02<-------0,32-0,3=0,02
=> \(m_{cr}=\left(0,08-0,02\right).80=4,8\left(g\right)\)
TH2: CuO phản ứng trước Fe2O3 dư
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)0,08------->0,08
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
0,08<----------0,32-0,08=0,24
=> \(m_{cr}=\left(0,1-0,08\right).160=3,2\left(g\right)\)
Đúng 2
Bình luận (0)
b) Gọi V là thể tích cần tìm của hỗn hợp
=> \(n_{H^+}=V.1+V.2.0,5=2V\) (1)
\(Fe_2O_3+3H^+\rightarrow Fe^{3+}+3H_2O\)
\(CuO+2H^+\rightarrow Cu^{2+}+H_2O\)
Theo PT => \(n_{H^+}=3n_{Fe_2O_3}+2n_{CuO}=0,46\left(mol\right)\) (2)
Từ (1),(2) => V=0,23(l)
Đúng 1
Bình luận (1)
Hòa tan hỗn hợp bột kim loại gồm 8,4 gam Fe và 6,4 gam Cu vào 350 ml dung dịch AgNO3 2M. Sau khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Giá trị của m là:
A. 70,2 gam B. 54 gam C. 75,6 gam D. 64,8 gam
nFe = 0,15 mol ; nCu = 0,1 ; nAg+ = 0,7 mol
Fe + 2Ag+ → Fe2+ + 2Ag (1)
0,15→ 0,3 0,15 0,3
Cu + 2Ag+ → Cu2+ + 2Ag
0,1 → 0,2 0,2
Fe2+ + Ag+ → Fe3+ + Ag (3)
0,15 → 0,15 0,15
Từ (1) ; (2) → m = (0,3 + 0,2 + 0,15).108 = 70,2 gam → Đáp án A
Đúng 0
Bình luận (2)
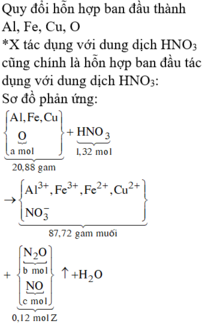
Nung nóng 20,88 gam hỗn hợp gồm Al, Fe2O3 và CuO trong khí trơ đến khi phản ứng xảy ra hoàn toàn thu được chất rắn X. Cho X vào dung dịch NaOH dư, thấy lượng NaOH phản ứng là 9,6 gam, thu được m gam chất rắn không tan. Nếu hòa tan hoàn toàn X trong dung dịch chứa 1,32 mol HNO3 thu được dung dịch Y chỉ chứa các muối nitrat của kim loiaj và 0,12 mol hỗn hợp khí Z gồm N2O và NO. Cô cạn dung dịch Y thu được 87,72 gam muối khan. Giá trị của m là: A.10,80. B.10,56. C.8,64. D.14,40.
Đọc tiếp
Nung nóng 20,88 gam hỗn hợp gồm Al, Fe2O3 và CuO trong khí trơ đến khi phản ứng xảy ra hoàn toàn thu được chất rắn X. Cho X vào dung dịch NaOH dư, thấy lượng NaOH phản ứng là 9,6 gam, thu được m gam chất rắn không tan. Nếu hòa tan hoàn toàn X trong dung dịch chứa 1,32 mol HNO3 thu được dung dịch Y chỉ chứa các muối nitrat của kim loiaj và 0,12 mol hỗn hợp khí Z gồm N2O và NO. Cô cạn dung dịch Y thu được 87,72 gam muối khan. Giá trị của m là:
A.10,80.
B.10,56.
C.8,64.
D.14,40.
Hòa tan 6 gam hỗn hợp A gồm Fe và Cu trong dung dịch H2SO4 loãng dư, sau khi phản ứng xảy ra hoàn toàn thu được 1,12 lit khí H2 (đktc) và còn lại m gam chất rắn không tan. Giá trị của m là
Biết Fe =56; Cu==1; S=32; O=16
A.3,2
B.4,8
C.2,8
D.1,6
\(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
_____0,05<--------------------0,05
=> mFe = 0,05.56 = 2,8 (g)
=> mCu = 6-2,8 = 3,2 (g)
=> A
Đúng 2
Bình luận (0)
Hòa tan hỗn hợp bột kim loại gồm 8,4 gam Fe vào 100 ml dung dịch Cu(NO3)2 2M. Sau khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Giá trị của m là:
Đọc tiếp
Hòa tan hỗn hợp bột kim loại gồm 8,4 gam Fe vào 100 ml dung dịch Cu(NO3)2 2M. Sau khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Giá trị của m là:
đây ạ
nFe = 8.4/56=0.15 mol
nCu = 6.4/64=0.1 mol
nAgNO3 = 0.35*2=0.7 mol
Fe + 2AgNO3 --> Fe(NO3)2 + 2Ag
0.15___0.3________0.15_____0.3
Cu + 2AgNO3 --> Cu(NO3)2 + 2Ag
0.1____0.2________0.1_______0.2
nAgNO3( còn lại ) = 0.7 - 0.3 - 0.2 = 0.2 mol
Vì : AgNO3 còn dư nên tiếp tục phản ứng với Fe(NO3)2
Fe(NO3)2 + AgNO3 --> Fe(NO3)3 + Ag
Bđ: 0.15________0.2
Pư: 0.15________0.15_______________0.15
Kt: 0___________0.05_______________0.15
Chất rắn : 0.65 (mol) Ag
mAg = 0.65*108 = 70.2g
Đúng 1
Bình luận (0)
em là hs lớp 6 ạ mong senpai tick giúp em
Đúng 2
Bình luận (0)
Hòa tan m gam hỗn hợp bột X gồm Al và K vào nước dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y; 6,72 lít H2 (đktc) và còn lại 0,12m gam chất rắn không tan. Giá trị của m là: A. 22,50. B. 17,42. C. 11,25. D. 8,71.
Đọc tiếp
Hòa tan m gam hỗn hợp bột X gồm Al và K vào nước dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y; 6,72 lít H2 (đktc) và còn lại 0,12m gam chất rắn không tan. Giá trị của m là:
A. 22,50.
B. 17,42.
C. 11,25.
D. 8,71.
Hòa tan 6 gam hỗn hợp A gồm Fe và Cu trong dung dịch H2SO4 loãng dư, sau khi phản ứng xảy ra hoàn toàn thu được 1,12 lít khí H2 (đktc) và còn lại m gam chất rắn không tan. Giá trị của m là
A. 1,6
B. 2,8
D. 4,8
D. 3,2
\(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
____0,05<------------------------0,05
=> mFe = 0,05.56 = 2,8 (g)
=> mCu = 6 - 2,8 = 3,2 (g)
=> D
Đúng 0
Bình luận (0)
Hoà tan hoàn toàn 20 gam hỗn hợp A gồm MgO, CuO và Fe2O3 cần vừa đủ 350ml dung dịch HCl 2M. Mặt khác nếu lấy 0,4 mol hỗn hợp A đốt nóng trong ống sứ không có không khí rồi cho luồng H2 dư đi qua tới phản ứng hoàn toàn thu được 7,2 gam H2O và m gam chất rắn. Giá trị của m là A. 25,2 gam B. 25,3 gam C. 25,6 gam D. 25,8 gam
Đọc tiếp
Hoà tan hoàn toàn 20 gam hỗn hợp A gồm MgO, CuO và Fe2O3 cần vừa đủ 350ml dung dịch HCl 2M. Mặt khác nếu lấy 0,4 mol hỗn hợp A đốt nóng trong ống sứ không có không khí rồi cho luồng H2 dư đi qua tới phản ứng hoàn toàn thu được 7,2 gam H2O và m gam chất rắn. Giá trị của m là
A. 25,2 gam
B. 25,3 gam
C. 25,6 gam
D. 25,8 gam
Trong 20 gam hỗn hợp A, gọi nMgO = a; nCuO = b; n F e 2 O 3 = c
Các phản ứng hòa tan A vào dung dịch HCl:
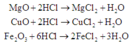
(Đơn giản có thể coi: 2H+ + O2- → H2O để nhẩm nhanh nHCl theo số mol các oxit)
Do đó 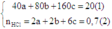
Khi cho H2 đi qua hỗn hợp A gồm MgO, CuO và Fe2O3 thì chỉ có CuO và Fe2O3 bị khử (Mg đứng trước Al trong dãy hoạt động hóa học nên MgO không bị khử). Vì H2 dư nên các oxit này bị khử hoàn toàn về kim loại tương ứng:
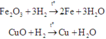
Khi đó H2 dư khử (a + b + c) mol hỗn hợp A, sau phản ứng thu được (b + 3c) mol H2O. Mà theo giả thiết, lấy 0,4 mol hỗn hợp A đốt nóng trong ống sứ không có không khí rồi cho luồng H2 dư đi qua tới phản ứng hoàn toàn thu được 7,2 gam H2O (0,4 mol H2O) nên ta lập tỉ lệ để tìm mối quan hệ:
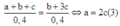
Từ (1), (2), (3) có 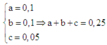
Do đó, 0,4 mol hỗn hợp A có khối lượng là: 0 , 4 0 , 25 . 20 = 32(gam)
![]()
Đáp án C.
Đúng 0
Bình luận (0)
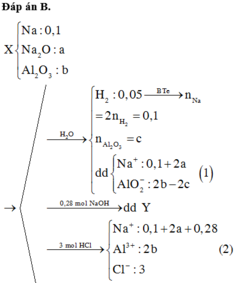
Hòa tan m gam hỗn hợp X gồm Na, Na2O và Al2O3 vào nước (dư), sau phản ứng, thu được 1,12 lít khí H2 (đktc) và còn lại 0,2334m gam rắn không tan. Mặt khác, hòa tan hoàn toàn m gam X vào 140 ml dung dịch NaOH 2M, thu được dung dịch Y. Cho Y phản ứng với dung dịch HCl thì lượng HCl phản ứng tối đa là 3 mol. Giá trị của m gần nhất với giá trị nào sau đây? A. 52,0. B. 52,5. C. 53,0. D. 53,5.
Đọc tiếp
Hòa tan m gam hỗn hợp X gồm Na, Na2O và Al2O3 vào nước (dư), sau phản ứng, thu được 1,12 lít khí H2 (đktc) và còn lại 0,2334m gam rắn không tan. Mặt khác, hòa tan hoàn toàn m gam X vào 140 ml dung dịch NaOH 2M, thu được dung dịch Y. Cho Y phản ứng với dung dịch HCl thì lượng HCl phản ứng tối đa là 3 mol. Giá trị của m gần nhất với giá trị nào sau đây?
A. 52,0.
B. 52,5.
C. 53,0.
D. 53,5.
Hòa tan m gam hỗn hợp bột X gồm Al và K vào nước dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y; 6,72l khí H2 (đktc) và còn lại 0,12g chất rắn không tan .Giá trị của m là: A. 22,50 B. 17,42 C. 11,25 D. 8,71
Đọc tiếp
Hòa tan m gam hỗn hợp bột X gồm Al và K vào nước dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y; 6,72l khí H2 (đktc) và còn lại 0,12g chất rắn không tan .Giá trị của m là:
A. 22,50
B. 17,42
C. 11,25
D. 8,71
Đáp án : C
K + H2O -> KOH + ½ H2
KOH + Al + H2O -> KAlO2 + 3/2 H2
=> chất rắn không tan là Al
=> nK = nAl pứ = ½ nH2 = 0,15 mol
=> m – 0,12m = mKl pứ = 0,15.39 + 0,15.27
=> m = 11,25g
Đúng 0
Bình luận (0)