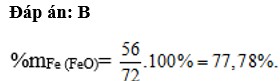Trong các hợp chất sau, hợp chất nào có hàm lượng Fe cao nhất: \(FeO;Fe_2O_3;Fe_3O_4;Fe\left(OH\right)_3;FeCl_2;FeSO_4.5H_2O\) (Chú ý: Hợp chất cuối cùng có dấu nhân ở giữa nha; không phải dấu phẩy đâu các bn!)
cho các chất sau : \(Fe;Fe_2O_3;Fe_2\left(SO_4\right)_3;Fe\left(OH\right)_3;Fe\left(NO_3\right)_3\) . Hãy sắp xếp các chất trên thành 3 dãy chuyển đổi háo học , và viết pt
Fe →(1) Fe2(SO4)3 →(2) Fe(OH)3 →(3) Fe2O3 →(4) Fe(NO3)3
(1) 2Fe + 3H2SO4 → Fe2(SO4)3 + 3H2
(2) Fe2(SO4)3 + 6NaOH -> 3Na2SO4 + 2Fe(OH)3
(3) 2Fe(OH)3 →t○ Fe2O3 + 3H2O
(4) Fe2O3 + 6HNO3 -> 2Fe(NO3)3 + 3H2O
Đúng 0
Bình luận (0)
Bài 1: Tính thành phần phần trăm của:Fe trong: FeO;Fe_2O_3;Fe_3O_4;Feleft(OHright)_2;Feleft(OHright)_3;Fe_2left(SO_4right)_3;FeSO_4;7H_2O.C trong: CO;CO_2;H_2CO_3;Na_2CO_3;CaCO_3;Mgleft(HCO_3right)_2.Bài 2 : Xác định Công Thức Hóa Học của những hợp chất có thành phần gồm 70%Fe và 30%O, biết khối lượng mol hợp chất là 160g.33,33%Na , 20,29%N , 46,37%O và Mh/c 69g.giúp mink với đag cần gấp!
Đọc tiếp
Bài 1: Tính thành phần phần trăm của:
Fe trong: FeO;\(Fe_2O_3\);\(Fe_3O_4\);\(Fe\left(OH\right)_2\);\(Fe\left(OH\right)_3\);\(Fe_2\left(SO_4\right)_3\);\(FeSO_4\);\(7H_2O\).
C trong: CO;\(CO_2\);\(H_2CO_3\);\(Na_2CO_3\);\(CaCO_3\);\(Mg\left(HCO_3\right)_2\).
Bài 2 : Xác định Công Thức Hóa Học của những hợp chất có thành phần gồm
70%Fe và 30%O, biết khối lượng mol hợp chất là 160g.
33,33%Na , 20,29%N , 46,37%O và Mh/c = 69g.
giúp mink với đag cần gấp!
Phân loại và gọi tên các hợp chất sau Mg\(\left(HCO_3\right)_2\) , \(Fe_2O_3,Ca\left(OH\right)_2,Fe_2\left(SO_4\right)_3\)
| Chất | Phân loại | Tên |
| Mg(HCO3)2 | Muối axit | Magie hiđrocacbonat |
| Fe2O3 | Oxit bazơ | Sắt (III) oxit |
| Ca(OH)2 | Bazơ | Canxi hiđroxit |
| Fe2(SO4)3 | Muối trung hòa | Sắt (III) sunfat |
Đúng 0
Bình luận (0)
M : Mg(HCO3)2 : magiê hidrocabonat
Fe2(SO4)3: sắt III sunfat
OB: Fe2O3 : sắt III oxit
BZ: Ca(OH)2: canxi hidroxit
Đúng 0
Bình luận (0)
Cân bằng các phương trình hóa học sau:
\(Fe_2O_3+CO->Fe+CO_2\)
\(Fe_2O_3+HCl->FeCl_3+H_2O\)
\(Fe_3O_4+H_2SO_4->FeSO_4+Fe_2\left(SO_4\right)_3+H_2O\)
Fe2O3+3CO---(to)--->2Fe+3CO2
Fe2O3+6HCl−>2FeCl3+3H2O
Fe3O4+4H2SO4−>FeSO4+Fe2(SO4)3+4H2O
Đúng 0
Bình luận (0)
Fe2O3 + 3CO → 2Fe + 3CO2
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Cân bằng các phương trình sau theo phương pháp thăng bằng electron:
\(1.FeS_2+O_2\rightarrow Fe_2O_3+SO_2\\ 2.FeS+HNO_3\rightarrow Fe\left(NO_3\right)_3+NO+H_2O+H_2SO_4\\ 3.Fe\left(CrO_2\right)_2+Na_2CO_3\rightarrow Na_2CrO_4+Fe_2O_3+CO_2\\ 4.AsS_3+KClO_3\rightarrow H_3AsO_4+H_2SO_4+KCl\\ 5.CrI_3+KOH+Cl_2\rightarrow K_2CrO_4+KIO_4+KCl+H_2O\\ 6.FeI_2+H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+SO_2+I_2+H_2O\)
1) \(\overset{+2}{Fe}\overset{-1}{S_2}+\overset{0}{O_2}\rightarrow\overset{+3}{Fe_2}\overset{-2}{O_3}+\overset{+4}{S}\overset{-2}{O_2}\)
quá trình OXH :\(\overset{+2}{Fe}\overset{-1}{S_2}\rightarrow\overset{+3}{Fe}+\overset{+4}{2S}+11e|\times4\)
quá trình khử : \(\overset{0}{2O}+2.2e\rightarrow\overset{-2}{2O}|\times11\)
\(\Rightarrow4FeS_2+11O_2\rightarrow2Fe_2O_3+8SO_2\)2) \(\overset{+2}{Fe}\overset{-2}{S}+H\overset{+5}{N}O_3\rightarrow\overset{+3}{Fe}\left(\overset{+5}{N}O_3\right)_3+\overset{+2}{N}\overset{-2}{O}+H_2O+H_2\overset{+6}{S}O_4\)
quá trình OXH : \(\overset{+2}{Fe}\overset{-2}{S}\rightarrow\overset{+3}{Fe}+\overset{+6}{S}+9e|\times1\)
quá trình khử : \(\overset{+5}{N}+3e\rightarrow\overset{+2}{N}|\times3\)
\(\Rightarrow FeS+6HNO_3\rightarrow Fe\left(NO_3\right)_3+3NO+2H_2O+H_2SO_4\)
CÒN ĐỂ CHIỀU MK LM CHO NHA
Đúng 0
Bình luận (0)
cho 13,8 g Na vào 240ml dung dịch có khối lượng riêng la 1,25g/ml chứa \(Fe_2\left(SO_4\right)_3\) 0,125M và \(Al_2\left(SO_4\right)_3\) 0,25M. sau phản ứng hoàn toàn thu được dung dịch A và kết tủa B. . Đem nung B đến khối lượng không đổi thu được m(g) chất rắn C
a, tính m
b. tính C% của các muối trong A
Trong các chất sau đây chất nào chứa hàm lượng sắt nhiều nhất
A. F e S 2
B. F e O
C. F e 2 O 3
D. F e 3 O 4
% m F e ( F e O ) = 56 72 .100 % = 77,78 % .
Đáp án B
Đúng 0
Bình luận (0)
Trong các chất sau đây chất nào chứa hàm lượng sắt nhiều nhất?
A. F e S 2
B. F e O
C. F e 2 O 3
D. F e 3 O 4
Viết PTHH hoàn thành chuỗi chuyển hóa sau:
\(Fe\underrightarrow{\left(1\right)}FeCl_3\underrightarrow{\left(2\right)}Fe\left(OH\right)_3\underrightarrow{\left(3\right)}Fe_2O_3\underrightarrow{\left(4\right)}Fe_2\left(SO_4\right)_3\underrightarrow{\left(5\right)}FeCl_3\)
(1) 2Fe + 3Cl2 -t0-> 2FeCl3
(2) FeCl3 + 3NaOH - > Fe(OH)3 + 3NaCl
(3) 2Fe(OH)3 -t0-> Fe2O3 + 3H2O
(4) Fe2O3 + 3H2SO4(l) - > Fe2(SO4)3 + 3H2O
(5) Fe2(SO4)3 + 3BaCl2 - > 2FeCl3 + 3BaSO4
Đúng 0
Bình luận (0)
1. 2Fe + 3Cl2 \(\rightarrow\)2 FeCl3
2. FeCl3 + 3NaOH \(\rightarrow\) Fe(OH)3 + 3NaCl
3. 2Fe(OH)3 \(\rightarrow\) Fe2O3 + 3H2O
4. Fe2O3 + 3H2SO4 \(\rightarrow\) Fe2(SO4)3 + 3H2O
5. Fe2(SO4)3 + 3BaCl2 \(\rightarrow\) 2FeCl3 + 3BaSO4
Đúng 0
Bình luận (0)