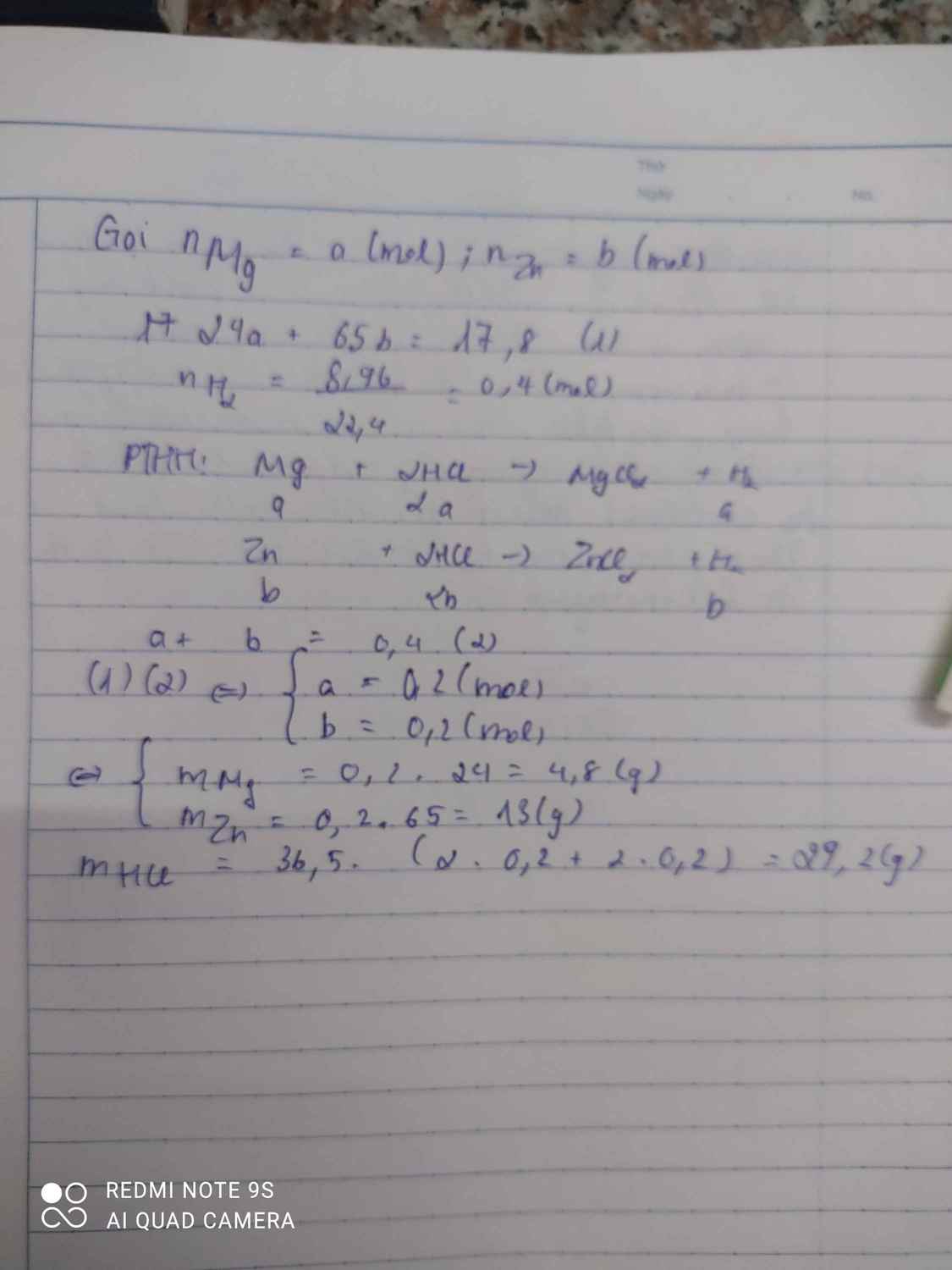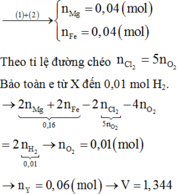cho 5g hỗn hợp fe và mg tác dụng vói hcl dư thì thu được 2,224 lít khí h2 a, viết phản ưng xảy ra b, tính khối lượng muỗi kim loại

Những câu hỏi liên quan
Cho 13,2g hh Mg và Fe tác dụng với lượng dư dd HCl,sau phản ứng thu được dd X và 7,84 lít khí H2( đktc)
a) Viết phương trình phản ứng xảy ra và tính phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu
b) Cô cạn dung dịch X thu được m gam muối khan.Tính m
mn giúp em với
Xem chi tiết
nH2= 0,35(mol)
a) PTHH: Mg + 2 HCl -> MgCl2 + H2
x_________2x_______x______x(mol)
PTHH: Fe + 2 HCl -> FeCl2 + H2
y________2y________y_____y(mol)
Ta có hpt: \(\left\{{}\begin{matrix}24x+56y=13,2\\x+y=0,35\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,15\end{matrix}\right.\)
b) m=m(muối khan)= mMgCl2 + mFeCl2= 95.x+127y=95.0,2+127.0,15= 38,05(g)
Đúng 1
Bình luận (0)
a)
Gọi
\(n_{Fe} = a(mol) ; n_{Mg} = b(mol)\\ \Rightarrow 56a + 24b = 13,2(1)\)
\(Mg + 2HCl \to MgCl_2 + H_2\\ Fe + 2HCl \to FeCl_2 + H_2\)
Theo PTHH : \(n_{H_2} = a + b = 0,35(mol)\)(2)
Từ (1)(2) suy ra a = 0,15 ;b = 0,2
Vậy :
\(\%m_{Fe} = \dfrac{0,15.56}{13,2}.100\% = 63,64\%\\ \Rightarrow m_{Mg} = 100\% - 63,64\% = 36,36\%\)
b)
Ta có :\(n_{HCl} = 2n_{H_2} = 0,7(mol)\)
Bảo toàn khối lượng :
\(m_{muối} = m_{kim\ loại} + m_{HCl} - m_{H_2} = 13,2 + 0,7.36,5 - 0,35.2=38,05(gam)\)
Đúng 1
Bình luận (0)
Cho 13,2g hh Mg và Fe tác dụng với lượng dư dd HCl,sau phản ứng thu được dd X và 8,6765
lít khí H2( đktc) a) Viết phương trình phản ứng xảy ra và tính phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu b) Cô cạn dung dịch X thu được m gam muối khan.Tính mSửa đề: đktc → đkc
a, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Ta có: 24nMg + 56nFe = 13,2 (1)
\(n_{H_2}=\dfrac{8,6765}{24,79}=0,35\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Mg}+n_{Fe}=0,35\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Mg}=0,2\left(mol\right)\\n_{Fe}=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,2.24}{13,2}.100\%\approx36,36\%\\\%m_{Fe}\approx63,64\%\end{matrix}\right.\)
b, Theo PT: \(\left\{{}\begin{matrix}n_{MgCl_2}=n_{Mg}=0,2\left(mol\right)\\n_{FeCl_2}=n_{Fe}=0,15\left(mol\right)\end{matrix}\right.\)
⇒ m muối khan = 0,2.95 + 0,15.127 = 38,05 (g)
Đúng 2
Bình luận (0)
Cho 5g hỗn hợp X gồm Mg và Cu tác dụng với dung dịch HCl 14,6% (phản ứng vừa đủ), thu được dung dịch Y và 3,36 lít khí H2 (ở đktc)
a) Viết PTHH của phản ứng xảy ra
b) Tính % theo khối lượng của mỗi kim loại trong hhX?
c) Tính Khối lượng dung dịch HCl đã dùng
d) Tính nồng độ % của dung dịch Y
a. PTHH : Mg + 2HCl ➝ MgCl2 + H2 (1)
b. theo bài : nH2 = 3,36 : 22,4 = 0,15 (mol)
theo (1) nMg = nH2 = 0,15 (mol)
➞ mMg = 0,15 ✖ 24 = 3,6 (g)
➞ %mMg = (3,6 : 5)✖100 = 72%
➞ %mCu = 100% - 72% = 28%
c. theo (1) nHCl = 2nH2 = 2✖0,15 = 0,3 (mol)
mHCl = 0,3✖36,5 = 10,95(g)
➜mddHCl = (10,95✖100):14,6 = 75(g)
d. dung dịch Y : MgCl2
mdd(spư)= 3,6+75-0,3 = 78,3(g)
theo (1) nMgCl2 = nH2 = 0,15(mol)
mMgCl2 = 0,15✖95 = 14,25(g)
C%MgCl2 = (14,25 : 78,3)✖100 = 18,199%
Đúng 0
Bình luận (0)
Cho 8,25 gam hỗn hợp kim loại Mg và Fe tác dụng hết với dung dịch HCL,thấy thoát ra 5,6 lít khí H2 (đktc)
a) Viết PTHH của phản ứng hoá học xảy ra
b) Tính khối lượng và thành phần phần trăm về khối lượng của mỗi kim loại trong hỗn hợp ban đầu
a. PTHH:
Fe + 2HCl ---> FeCl2 + H2 (1)
Mg + 2HCl ---> MgCl2 + H2 (2)
b. Gọi x, y lần lượt là số mol của Fe và Mg
Ta có: \(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Theo PT(1): \(n_{H_2}=n_{Fe}=x\left(mol\right)\)
Theo PT(2): \(n_{H_2}=n_{Mg}=y\left(mol\right)\)
\(\Rightarrow x+y=0,25\) (*)
Theo đề, ta lại có: 56x + 24y = 8,25 (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}x+y=0,25\\56x+24y=8,25\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x\approx0,07\\y\approx0,18\end{matrix}\right.\)
=> \(m_{Fe}=0,07.56=3,92\left(g\right)\)
=> \(\%_{m_{Fe}}=\dfrac{3,92}{8,25}.100\%=47,52\%\)
\(\%_{m_{Mg}}=100\%-47,52\%=52,48\%\)
Đúng 2
Bình luận (0)
BT4.cho hỗn hợp A gồm 17,8 gam Mg và Zn tác dụng vs dung dịch HCl dư . sau phản ứng thu đc 8,96 lít H2 (đktc)
a) viết PTHH của phản ứng xảy ra .
b) tính khối lượng mỗi kim loại trong hỗn hợp A.
c)tính khối lượng HCl tối thiểu cần dùng .
lm giúp mik vsssssssss
Mg+2HCl->MgCl2+H2
x------------------------x
Zn+2HCl->ZnCl2+H2
y-------------------------y
Ta có :
\(\left\{{}\begin{matrix}24x+65y=17,8\\x+y=\dfrac{8,96}{22,4}\end{matrix}\right.\)
=>x=0,2 mol, y=0,2 mol
=>mMg=0,2.24=4,8g
=>m Zn=0,2.65=13g
=>m HCl=0,8.36,5=29,2g
Đúng 4
Bình luận (0)
Cho 14,8 gam hỗn hợp X gồm 2 kim loại Fe và Cu vào dung dịch HCl dư, thu được 3,36 lít khí H2(đktc). Mặc khác cho 29,6 gam hỗn hợp X tác dụng với H2SO4 đặc nguội thì thu được V lít khí ở đktc
1. Viết PTHH xảy ra
2. Tính thành phần % khối lượng mỗi kim loại có trong hỗn hợp X
3. Tính V
1)
Fe + 2HCl --> FeCl2 + H2
Cu + 2H2SO4 --> CuSO4 + SO2 + 2H2O
2)
- Xét TN1:
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,15<------------------0,15
=> mFe = 0,15.56 = 8,4 (g)
\(\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{8,4}{14,8}.100\%=56,757\%\\\%m_{Cu}=100\%-56,757\%=43,243\%\end{matrix}\right.\)
3)
- Xét TN2:
\(n_{Cu}=\dfrac{29,6.43,243\%}{64}=0,2\left(mol\right)\)
PTHH: Cu + 2H2SO4 --> CuSO4 + SO2 + 2H2O
0,2-------------------------->0,2
=> V = 0,2.22,4 = 4,48 (l)
Đúng 2
Bình luận (0)
Cho 4,32 gam hỗn hợp X gồm Mg và Fe tác dụng vói V lít (đktc) hỗn hợp Y gồm Cl2 và O2 (có tỉ khối hơi với H2 bằng 32,25), thu được hỗn hợp rắn Z. Cho Z vào đung dịch HCl, thu được 1,12 gam một kim loại không tan, dung dịch T và 0,224 lít khí H2 (đktc). Cho T vào dung dịch AgNO3 dư, thu đuợc 27,28 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của V là A A. 1,536 B. 1,680 C. 1,344 D. 2,016
Đọc tiếp
Cho 4,32 gam hỗn hợp X gồm Mg và Fe tác dụng vói V lít (đktc) hỗn hợp Y gồm Cl2 và O2 (có tỉ khối hơi với H2 bằng 32,25), thu được hỗn hợp rắn Z. Cho Z vào đung dịch HCl, thu được 1,12 gam một kim loại không tan, dung dịch T và 0,224 lít khí H2 (đktc). Cho T vào dung dịch AgNO3 dư, thu đuợc 27,28 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của V là A
A. 1,536
B. 1,680
C. 1,344
D. 2,016
Cho 20,8 gam hỗn hợp kim loại Fe và Mg tác dụng với dung dịch HCl dư
thì thu được 13,44 lít khí H2 (đktc). Tính khối lượng muối thu được sau phản ứng?
(Cho khối lượng nguyên tử: Fe = 56; Mg = 24; H = 1; Cl = 35,5)
\(n_{Cl}=n_{HCl}=2n_{H_2}=2\cdot\dfrac{13.44}{22.4}=1.2\left(mol\right)\)
\(m_{muối}=m_{kl}+m_{Cl}=20.8+1.2\cdot35.5=63.4\left(g\right)\)
Đúng 0
Bình luận (0)
Cho 23,2 gam hỗn hợp Mg và Fe tác dụng với dd HCl dư thu được 11,2 lít H2 (đktc)
a) Viết PTPƯ
b) Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu
a/ PTHH: Mg + 2HCl ==> MgCl2 + H2
Fe + 2HCl ===> FeCl2 + H2
b/ nH2 = 11,2 / 22,4 = 0,5 mol
Đặt số mol của Mg, Fe lần lượt là x, y
Theo đề ra, ta có hệ phương trình sau:
\(\begin{cases}24x+56y=23,2\\x+y=0,5\end{cases}\)=> \(\begin{cases}x=0,15\\y=0,35\end{cases}\)
=> mMg = 0,15 x 24 = 3,6 gam
mFe = 0,35 x 56 = 19,6 gam
Đúng 1
Bình luận (0)
Mg + 2 HCl => MgCl2 + H2
y y
Fe + 2HCl => FeCl2 + H2
x x
ta có mol H2 =\(\frac{11,2}{22,4}\) = 0,5 mol
ta có mFe + mMg = 23,2 <=> 56x + 24y = 23,2 (1)
x + y = 0,5 (2)
Từ (1) và (2) => x=0,35 , y = 0,15
=> mFe = 0,35 x 56 = 19,6 g , mMg = 23,2 -19,6 = 3,6 g
Đúng 1
Bình luận (0)