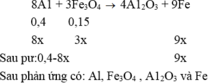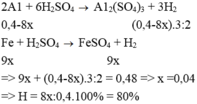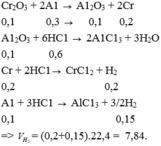dùng v (ml) khí h2 để pư vs 2,16g bột feo ở nhiệt độ thích hợp, sau pư thu đc 1,84g chất rắn. tính v và hiệu suất pư trên

Những câu hỏi liên quan
Trộn 10,8g bột Al với 34,8g bột Fe3O4 rồi tiến hành pư nhiệt nhôm trong điều kiện không có không khí. Hòa tan hoàn toàn hh rắn sau pư bằng dd H2SO4 loãng (dư), thu được 10,752 lít khí H2 (đktc). Hiệu suất của pư nhiệt nhôm 1à A. 80% B. 90% C. 70% D. 60%
Đọc tiếp
Trộn 10,8g bột Al với 34,8g bột Fe3O4 rồi tiến hành pư nhiệt nhôm trong điều kiện không có không khí. Hòa tan hoàn toàn hh rắn sau pư bằng dd H2SO4 loãng (dư), thu được 10,752 lít khí H2 (đktc). Hiệu suất của pư nhiệt nhôm 1à
A. 80%
B. 90%
C. 70%
D. 60%
Cho V lít khí CO phản ứng vs fe2o3 ở nhiệt độ cao tạo thành phe và co2. Nếu cho lượng fe sau phản ứng tan hết trong h2so4 loãng đc 20,16 lít khí hidro đktc.a) tính V CO đã pư đkt.b) nếu hòa tan hết c rắn sau pư khử bđ phải dùng hết 94,9 g HCl thì khối lượng fe2o3 đã dùng nđ là bn?c) nếu sau pư bđ vs cùg kl fe2o3 ns trên toàn bộ khí sau pư khử td vừa đủ vs 3,36 l oxi đktc thì V CO đã dùng nđ ở đkt bn lít?
Đọc tiếp
Cho V lít khí CO phản ứng vs fe2o3 ở nhiệt độ cao tạo thành phe và co2. Nếu cho lượng fe sau phản ứng tan hết trong h2so4 loãng đc 20,16 lít khí hidro đktc.
a) tính V CO đã pư đkt.
b) nếu hòa tan hết c rắn sau pư khử bđ phải dùng hết 94,9 g HCl thì khối lượng fe2o3 đã dùng nđ là bn?
c) nếu sau pư bđ vs cùg kl fe2o3 ns trên toàn bộ khí sau pư khử td vừa đủ vs 3,36 l oxi đktc thì V CO đã dùng nđ ở đkt bn lít?
Nung hh bột gồm 15,2 gam Cr2O3 và m gam Al ở nhiệt độ cao. Sau khi pư hoàn toàn, thu được 23,3 gam hh rắn X. Cho toàn bộ hh X pư với axit HCl(dư) thoát ra V 1ít khí H2 (ở đktc). Giá trị của V 1à A. 7,84 B. 4,48 C. 3,36 D. 10,08
Đọc tiếp
Nung hh bột gồm 15,2 gam Cr2O3 và m gam Al ở nhiệt độ cao. Sau khi pư hoàn toàn, thu được 23,3 gam hh rắn X. Cho toàn bộ hh X pư với axit HCl(dư) thoát ra V 1ít khí H2 (ở đktc). Giá trị của V 1à
A. 7,84
B. 4,48
C. 3,36
D. 10,08
1. nhiệt phân 10,1g KNO3 thu đc 2,688 lit khí O2(dktc)
a. tính hiệu suất
tính %m các chất trong chất rắn sau pư
b. cho hỗn hợp gồm 0,1mol Ag, 0,2mol Al pư hoàn toàn vs lượng O2 thu đc ở trên.
Tính m chất rắn sau pư
2. đốt cháy 36g FeS2 trong 11,2lit khí O2(dktc) thu đc 16g Fe2O3 và X lit khí SO2(đktc).Tính:
a.hiệu suất
b.X?
c. %m các chất trong chất rắn sau pư
HELP ME
Đọc tiếp
1. nhiệt phân 10,1g KNO3 thu đc 2,688 lit khí O2(dktc)
a. tính hiệu suất
tính %m các chất trong chất rắn sau pư
b. cho hỗn hợp gồm 0,1mol Ag, 0,2mol Al pư hoàn toàn vs lượng O2 thu đc ở trên.
Tính m chất rắn sau pư
2. đốt cháy 36g FeS2 trong 11,2lit khí O2(dktc) thu đc 16g Fe2O3 và X lit khí SO2(đktc).Tính:
a.hiệu suất
b.X=?
c. %m các chất trong chất rắn sau pư
HELP ME
Bài 1:
a) nKNO3= 1(mol); nO2 = 0,12(mol)
2KNO3 ---> 2KNO2 + O2
0,24 0,24 0,12
=> H pứ= \(\dfrac{0,24}{1}\). 100%= 24%
Sau pứ có KNO2 và KNO3 dư
mKNO2= 20,4(g); m KNO3 = 24,24(g)
b) Ag ko pứ với O2
4Al + 3O2---> 2Al2O3
0,2 0,1
m chất sau pứ= 21(g)
2. nFeS2= 0,3; nO2= 0,5; nFe2O3= 0,1
4FeS2 + 11O2 --> 2Fe2O3 + 8SO2
0,2 0,1 0.4
a) H pứ = 66,67%
b) X= 8,96 (l)
c) m chất rắn sau phản ứng= 40 (g)
%m Fe2O3= 40%
%m FeS2 = 60%
Đúng 0
Bình luận (0)
Hà Yến NhiTrần Hữu TuyểnVũ Phương LyNguyễn Phương TrâmMystOtaku Nobierious Person
Nhiên An TrầnThien NguyenAyanokouji Yikotaka Đậu Thị Khánh HuyềnPhùng Hà ChâuTô Ngọc HàThảo Phương Nguyễn An
muốn đặt tên nhưng chưa nghĩ ra bạn nào tốt nghĩ giùm m giúp vs ạ
Đúng 0
Bình luận (2)
1. nhiệt phân 101g KNO3 thu đc 2,688 lit khí O2(dktc)
mình sửa chỗ in đậm nhé
Đúng 0
Bình luận (2)
Đốt cháy hoàn toàn 13g hh A gồm C và S trong khí O2 vừa đủ, sau pư thu đc hh khí B gồm CO2 và SO2 có tỉ khối đối vs H2 là 29
a, Tính thành phần % theo khối lượng mỗi chất trong A
b,Tính thể tích khí O2 đã pư đktc
c,Tính khối lượng KMnO4 cần dùng để khi phân hủy thu đc lượng khí O2 ở trên? Biết hiệu suất pứ phân hủy KMnO4 là 80%
a,PTHH: C + O2 -> CO2 (*)
x x x (mol)
S + O2 -> SO2 (**)
y y y (mol)
Ta có dB/H2=9 => MB = 29.2=58 (g)=m hh khí B / n hh Khí B
<=>58= \(\frac{44x+64y}{x+y}\)
=>44x+64y=58x+58y
<=>7x=3y
<=> 7x-3y=0 (1)
Mà hh A =12x+32y=13 (2)
b,Từ (1),(2) ta có hệ pt
\(\hept{\begin{cases}7x-3y=0\\12x+3y=13\end{cases}}\Leftrightarrow\hept{\begin{cases}x=0,15\\y=0,35\end{cases}}\)
=>%C = (12.0,15)/13 .100%=13,84%
%S= 100%-13,84%= 86,16%
Từ pt (*),(**) ta có VO2(đktc)=(x+y).22,4=11,2(l)
Đúng 0
Bình luận (0)
dẫn luồng khí H2 đi qua ống đựng 24g CuO nung nóng , sau một thời gian pư thu được 21,6 g chất rắn a, tính hiệu suất pư b, tính thể tích H2 đã tham gia pư (đktc)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\\ Đặt:n_{CuO\left(p.ứ\right)}=a\left(mol\right)\\ \Rightarrow n_{Cu}=a\left(mol\right);m_{CuO\left(dư\right)}=24-80a\left(g\right)\\ \Rightarrow m_{rắn}=m_{CuO\left(dư\right)}+m_{Cu}=\left(24-80a\right)+64a=21,6\\ \Leftrightarrow-16a=-2,4\\ \Leftrightarrow a=0,15\\ Vậy:H=\dfrac{0,15.80}{24}.100\%=50\%\\ b,n_{H_2}=n_{Cu}=a=0,15\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,15.22,4=3,36\left(l\right)\)
Đúng 3
Bình luận (0)
Cho luồng khì H2 đi qua ống thủy tinh chứa 20 g CUO ở 400 độ C .Sau PƯ thu đc 16,8 g chất rắn
a, Tính hiệu suất PƯ ??
b, Tih thể tích H2 đã tham gia PƯ ở đktc
Gọi số mol CuO phản ứng là x mol.
PTHH: CuO + H2 \(\underrightarrow{t^o}\) Cu + H2O
mol:.......x.........x.........x.........x
Áp dụng bảo toàn khối lượng ta có
mCuO + mH2 = mCu + mH2O
<=> 20 + 2x = 16,8 + 18x
<=> x = 0,2 mol.
Nếu lượng CuO phản ứng hoàn toàn thì số mol phản ứng bằng nCuO = 20/80 = 0,25
=> H = \(\dfrac{n_{CuO\left(thực\right)}}{n_{CuO\left(líthuyết\right)}}.100=\dfrac{0,2}{0,25}.100=80\%\)
nH2 = x => VH2 = 4,48 lít
Đúng 0
Bình luận (2)
Bài 1:
1/Cho một lượng nhôm dư vào 500ml dung dịch HCl 0,5M đến khi PƯ hoàn toàn thu được V l khí H2.
a/Tính V?
b/Dẫn từ từ khí H2 thu được ở trên qua ống sứ có chứa 21,6g FeO đun nóng,sau PƯ chất rắn còn lại trong ống có khối lượng là 18,4g.Tính hiệu suất PƯ của FeO?
2/Cho hỗn hợp X gồm Cu,Fe và Al.Cho 57,2g X vào dung dịch HCl dư đến PƯ hoàn toàn thu được 26,88l khí H2 (đktc).Oử nhiệt độ cao 1,2 mol X phản ứng vừa đủ với 25,6g O2.Viết các PTHH của các PƯ xảy ra,tính Thành phần phần trăm về...
Đọc tiếp
Bài 1:
1/Cho một lượng nhôm dư vào 500ml dung dịch HCl 0,5M đến khi PƯ hoàn toàn thu được V l khí H2.
a/Tính V?
b/Dẫn từ từ khí H2 thu được ở trên qua ống sứ có chứa 21,6g FeO đun nóng,sau PƯ chất rắn còn lại trong ống có khối lượng là 18,4g.Tính hiệu suất PƯ của FeO?
2/Cho hỗn hợp X gồm Cu,Fe và Al.Cho 57,2g X vào dung dịch HCl dư đến PƯ hoàn toàn thu được 26,88l khí H2 (đktc).Oử nhiệt độ cao 1,2 mol X phản ứng vừa đủ với 25,6g O2.Viết các PTHH của các PƯ xảy ra,tính Thành phần phần trăm về khối lượng mỗi chất trong X
Nung 30g CaCO3 ở nhiệt độ cao sau 1 thgi thu đc 23,4g chất rắn. Dẫn toàn bộ khí vào V lít dd Ba(OH)2 2M sau khi pư kết thúc thì thu đc 17,73g kết tủa. Tính V kết tủa
\(CaCO_3\rightarrow\left(t^o\right)CaO+CO_2\\ CO_2+Ba\left(OH\right)_2\rightarrow BaCO_3+H_2O\\ m_{BaCO_3}=17,73\left(g\right)\Rightarrow n_{BaCO_3}=0,09\left(mol\right)\\ n_{Ba\left(OH\right)_2}=n_{BaCO_3}=0,09\left(mol\right)\\ V=V_{ddBa\left(OH\right)_2}=\dfrac{0,09}{2}=0,045\left(l\right)\)
Đúng 2
Bình luận (0)