Bài 3: Biết chất Pederine có công thức hóa học là C24H43O9N.
a)Neu y nghĩa của công thức hóa học trên ?
b)Tinh thành phần phần trăm theo khối lượng của nguyên tổ Nitrogen trong Pederine.
Bài 3: Biết chất phèn chua có công thức hóa học là Al2(SO4)3.
a) Nêu ý nghĩa của công thức hóa học trên ?
b)Tính thành phần phần trăm theo khối lượng của các nguyên tố trong phèn chua.
a) Có 2 nguyên tử nhôm , 3 nguyên tử lưu huỳnh , 12 nguyên tử Oxi
b) \(M_{Al_2\left(SO_4\right)_3}=27.2+\left(32+16.4\right).3=342\left(DvC\right)\\ \%Al=\dfrac{27.2}{342}.100\%=15\%\\ \%S=\dfrac{32.3}{342}.100\%=28\%\\ \%O=100\%-15\%-28\%=57\%\)
a) ý nghĩa:
Được tạo bởi 2 nguyên tử Al, 3 nguyên tử S và 12 nguyên tử O
Được tạo bởi 3 nguyên tố là: Al, S và O
Có PTK là: 27. 2 + (32 + 16 . 4) . 3 = 342 (đvC)
b) Thành phần % của các nguyên tố trong h/c là:
\(\%Al=\dfrac{54}{342}=15,78\%\\ \%S=\dfrac{96}{342}=28,07\%\\ \%O=100\%-15,78\%-28,07\%=56,15\%\)
Bài 3: Biết đường saccarozơ có công thức hóa học là C12H22O11.
a) Công thức hóa học trên cho em biết điều gì ?
b)Tính thành phần phần trăm theo khối lượng của các nguyên tố trong đường.
a, - Đường saccarozo do nguyên tố C, H, O tạo ra
- Có 12 nguyên tử C, 22 nguyên tử H và 11 nguyên tử O
- PTK = \(12.12+1.22+16.11=342đvC\)
b, \(\%m_C=\dfrac{144.100\%}{342}=42,1\%\\ \%m_H=\dfrac{22.100\%}{342}=6,43\%\)
\(\%m_O=100\%-42,1\%-6,43\%=51,47\%\)
Một hợp chất có công thức hóa học là K2CO3. Em hãy cho biết:
a) Khối lượng mol của chất đã cho.
b) Thành phần phần trăm (theo khối lượng) của các nguyên tố có trong hợp chất.
a) MK2CO3 = 39.2 + 12 + 16.3 = 138 (g)
b)
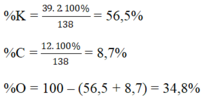
Một hợp chất có công thức hóa học là CaCo3 . Hãy tính thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất trên
Bài làm
Khối lượng mol của chất đã cho là:
MCaCO3 = 40 . 1 + 12 + 16 . 3 = 100 ( g )
Thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất trên là:
%Ca = ( 40 . 100 ) / 100 = 40%
%C = ( 12 . 100 ) / 100 = 12%
%O = 100% - 40% - 12% = 48%
# Chúc bạn học tốt #
A/LẠC LONG QUÂN :DÒNG DÕI NGUỒN GỐC NÒI RỒNG LÀ CON TRAI CỦA THẦN LONG NỮ
TÀI NĂNG: CÓ NHIỀU PHÉP LẠ
ÂU CƠ :LA TIÊN NỮ DONG HO THẦN NONG
Calcium carbonate là thành phần chính của đá vôi, có công thức hóa học là CaCO3. Tính phần trăm khối lượng của mỗi nguyên tố trong hợp chất trên
\(PTK_{CaCO_3}=NTK_{Ca}+NTK_C+3.NTK_O=40+12+3.16=100\left(đ.v.C\right)\\ \%m_{Ca}=\dfrac{NTK_{Ca}}{PTK_{CaCO_3}}.100\%=\dfrac{40}{100}.100=40\%\\ \%m_C=\dfrac{NTK_C}{PTK_{CaCO_3}}.100\%=\dfrac{12}{100}.100=12\%\\ \%m_O=100\%-\left(\%m_{Ca}+\%m_C\right)=100\%-\left(40\%+12\%\right)=48\%\)
Một hợp chất có công thức hóa học là K2CO3. Em hãy cho biết;
a) Khối lượng mol của chất đã cho
b) Thành phần phần trăm (theo khối lượng) của các nguyên tố có trong hợp chất.
a) Khối lượng mol của chất đã cho: MK2CO3= 39 . 2 + 16 . 3 = 138g
b) Thành phần phần trăm (theo khối lượng) của các nguyên tố có trong hợp chất
%K = (39,2 .100)/138 = 56,5 %
%C = (12.100)/138 = 8,7%
%O = (16,3 . 100)/138 = 34,8%
a) khối lượng mọi mol k2co3=39.2+12=16.3=138g
b)trong 1 mol k2co3 có: 2 mol nguyên tử k ->78g
1 mol nguyên tử c-> 12g
3 mol nguyên tử o->48g
thành phần các nguyên tố trong hơp chất:
%mk=\(\frac{78x100\%}{138}=56,5\%\) %mc=\(\frac{12x100\%}{138}=8,7\%\)
\(\%m_o=\frac{48x100\%}{138}=34,8\%\)
1.Tính thành phần phần trăm (theo khối lượng) của các nguyên tố hóa học có mặt trong các hợp chất sau:
a) Fe(NO3)2, Fe(NO3)2
b) N2O, NO, NO2
2.Hãy tìm công thức hóa học của chất X có khối lượng mol MX = 170 (g/mol), thành phần các nguyên tố theo khối lượng: 63,53% Ag; 8,23% N, còn lại O.
3.Lập công thức hóa học của hợp chất A biết:
- Phân khối của hợp chất là 160 đvC
-Trong hợp chất có 70% theo khối lượng sắt, còn lại là oxi.
Câu 2:
Trong 1 mol X: \(\left\{{}\begin{matrix}n_{Ag}=\dfrac{170.63,53\%}{108}=1\left(mol\right)\\n_N=\dfrac{170.8,23\%}{14}=1\left(mol\right)\\n_O=\dfrac{170\left(100\%-63,53\%-8,23\%\right)}{16}=3\left(mol\right)\end{matrix}\right.\)
Vậy CTHH của X là \(AgNO_3\)
Câu 1:
\(a,\%_{Fe}=\dfrac{56}{180}\cdot100\%=31,11\%\\ \%_N=\dfrac{14\cdot2}{180}\cdot10\%=15,56\%\\ \%_O=100\%-31,11\%-15,56\%=53,33\%\\ b,\%_{N\left(N_2O\right)}=\dfrac{14\cdot2}{44}\cdot100\%=63,63\%\\ \%_{O\left(N_2O\right)}=100\%-63,63\%=36,37\%\\ \%_{N\left(NO\right)}=\dfrac{14}{30}\cdot100\%=46,67\%\\ \%_{O\left(NO\right)}=100\%-46,67\%=53,33\%\\ \%_{O\left(NO_2\right)}=\dfrac{16\cdot2}{46}\cdot100\%=69,57\%\\ \%_{N\left(NO_2\right)}=100\%-69,57\%=30,43\%\)
Một hợp chất hóa học có công thức là CaCO3 Em hãy xác định thành phần phần trăm theo khối lượng của nguyên tố
\(\%Ca=\dfrac{1.40}{100}.100\%=40\%\\\%C=\dfrac{1.12}{100}.100\%=12\%\\ \%O=100\%-\left(40\%+12\%\right)=48\% \)
MCaCO3 = 100 g/mol
%Ca = \(\dfrac{40}{100}.100\)= 40%
%C = \(\dfrac{12}{100}.100\)= 12%
%O3= \(\dfrac{48}{100}.100\)=48%
Nêu các bước giải bài toán xác định thành phần phần trăm theo khối lượng của các nguyên tố tron hợp chất khi biết công thức hóa học của hợp chất.
Các bước giải :
B1 : Tính khối lượng mol của hợp chất.
B2 : Tính số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất.
B3 : Tính khối lượng của mỗi nguyên tố có trong 1 mol hợp chất.
B4 : Tính thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất.
Các bước giải:
Bước 1:Tính khối lượng M của hợp chất.
Bước 2 :Tính số M nguyên tử của mỗi nguyên tố có trong 1 M hợp chất.
Bước 4:Tính phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất.
☆♡CHÚC BẠN HỌC TỐT♡☆
Bước 1 : tính khối lượng của hợp chất (đvC)
Bước 2 : tính khối lượng các nguyên tố trong hợp chất(đvC)
Bước 3 : tính % khối lượng của nguyên tố trong hợp chất theo công thức :
%mnguyên tố = (NTKnguyên tố * số nguyên tử nguyên tố đó trong hợp chất) : PTKhợp chất