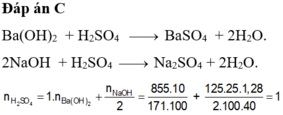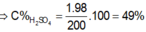Để trung hòa hết 40,5 gam dung dịch HX (X: F, Cl, Br, I) nồng độ 10% người ta phải dùng dung dịch AgNO3 dư thu được 8,5 gam kết tủa. Dung dịch axit ở trên là dung dịch

Những câu hỏi liên quan
Để trung hòa hết 40,5 gam dung dịch HX (X:F, Cl, Br, I) nồng độ 10% người ta phải dùng dung dịch AgNO3 dư thu được 8,5 gam kết tủa. Dung dịch axit ở trên là dung dịch gì ?
A:HF B:HI C:HBr D:HCl
giải thích giải dùm mình cần gấp tối nay lúc 8h
PTHH: \(HX+AgNO_3\rightarrow HNO_3+AgX\downarrow\)
Theo PTHH: \(n_{HX}=n_{AgX}\)
\(\Rightarrow\dfrac{40,5\cdot10\%}{M_X+1}=\dfrac{8,5}{108+M_X}\) \(\Rightarrow M_X\approx96,38\)
*Bạn xem lại đề
Đúng 2
Bình luận (0)
Để trung hòa hết 200g dung dịch HX ( X là halogen) nồng độ 14,6% người ta phải dùng 250 ml dung dịch NaOH 3,2M. Dung dịch axit trên là dung dịch nào ?
PTHH: \(HX+NaOH\rightarrow NaX+H_2O\)
Theo PTHH: \(n_{NaOH}=n_{HX}\)
\(\Rightarrow\dfrac{200\cdot14,6\%}{1+M_X}=0,25\cdot3,2\) \(\Leftrightarrow M_X=35,5\) (Clo)
Vậy HX là HCl
Đúng 0
Bình luận (0)
Cho 855 gam dung dịch Ba(OH)2 10% vào 200 gam dung dịch H2SO4 thu được kết tủa và dung dịch X. Để trung hoà dung dịch X người ta phải dùng 125ml dung dịch NaOH 25% (d 1,28). Nồng độ phần trăm của dung dịch H2SO4 là: A. 98% B. 25% C. 49% D. 50%
Đọc tiếp
Cho 855 gam dung dịch Ba(OH)2 10% vào 200 gam dung dịch H2SO4 thu được kết tủa và dung dịch X. Để trung hoà dung dịch X người ta phải dùng 125ml dung dịch NaOH 25% (d= 1,28). Nồng độ phần trăm của dung dịch H2SO4 là:
A. 98%
B. 25%
C. 49%
D. 50%
Hòa tan 5,94 gam hỗn hợp 2 muối clorua của 2 kim loại A, B (đều có hoá trị II) vào nước được dung dịch X. Để làm kết tủa hết ion Cl- có trong dung dịch X người ta cho dung dịch X tác dụng với dung dịch AgNO3 thu được 17,22 gam kết tủa. Lọc bỏ kết tủa, thu được dung dịch Y. Cô cạn Y được m gam hỗn hợp muối khan. Giá trị m là A. 6,36 g. B. 63,6 g. C. 9,12g. D. 91,2g.
Đọc tiếp
Hòa tan 5,94 gam hỗn hợp 2 muối clorua của 2 kim loại A, B (đều có hoá trị II) vào nước được dung dịch X. Để làm kết tủa hết ion Cl- có trong dung dịch X người ta cho dung dịch X tác dụng với dung dịch AgNO3 thu được 17,22 gam kết tủa. Lọc bỏ kết tủa, thu được dung dịch Y. Cô cạn Y được m gam hỗn hợp muối khan. Giá trị m là
A. 6,36 g.
B. 63,6 g.
C. 9,12g.
D. 91,2g.
Áp dụng phương pháp tăng giảm khối lượng:
Cứ 1 mol MCl2 → 1 mol M(NO3)2 và 2 mol AgCl thì m tăng 2.62 - 2.35,5 = 53 gam
Phản ứng tạo 0,12 mol AgCl có khối lượng muối tăng 3,18 gam
mmuối nitrat = mmuối clorua + mtăng = 5,94 + 3,18 = 9,12 (gam)
Đáp án C
Đúng 0
Bình luận (0)
Tính nồng độ của hai dung dịch axit clohiđric trong các trường hợp sau:
a) Cần phải dùng 150ml dung dịch HCl để kết tủa hoàn toàn 200g dung dịch AgNO3 8,5%.
b) Khi cho 50g dung dịch HCl vào một cốc đựng NaHCO3 (dư) thì thu được 2,24 lít khí ở đktc.
a) 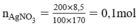
Phương trình hóa học của phản ứng:
HCl + AgNO3 → AgCl + HNO3
Theo pt nHCl = nAgCl = 0,1 mol
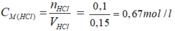
b) 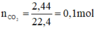
Phương trình hóa học của phản ứng:
HCl + NaHCO3 → NaCl + CO2↑ + H2O
Theo pt: nHCl = nCO2 = 0,1 mol ⇒ mHCl = 0,1. 36,5 = 3,65 g
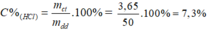
Đúng 0
Bình luận (0)
Hòa tan 5,94 gam hỗn hợp 2 muối clorua của 2 kim loại A, B (đều có hoá trị II) vào nước được dung dịch X. Để làm kết tủa hết ion Cl- có trong dung dịch X người ta cho dung dịch X tác dụng với dung dịch AgNO3 thu được 17,22 gam kết tủa. Xác định công thức hóa học của 2 muối chloride
Đọc tiếp
Hòa tan 5,94 gam hỗn hợp 2 muối clorua của 2 kim loại A, B (đều có hoá trị II) vào nước được dung dịch X. Để làm kết tủa hết ion Cl- có trong dung dịch X người ta cho dung dịch X tác dụng với dung dịch AgNO3 thu được 17,22 gam kết tủa. Xác định công thức hóa học của 2 muối chloride
Bài 2: Đổ dung dịch chứa 1g HBr vào dung dịch chứa 1g NaOH. Nhúng miếng giấy quỳ vào dung dịch thu được thì giấy quỳ sẽ đổi màu như thế nào?
Bài 3: Cho lượng dư dung dịch AgNO3 tác dụng với hỗn hợp gồm 0,1 mol NaF và 0,1 mol NaCl. Tính khối lượng kết tủa tạo thành?
Bài 4: Để trung hòa hết 200g dung dịch HX (F, Cl, Br, I) nồng độ nồng độ 14,6%. Người ta phải dùng 250 ml dung dịch NaOH 3,2M. Xác định CTHH của HX
Bài 5: Cho m gam hỗn hợp A gồm Fe và Mg vào dung dịch HCl dư thu được 5,6 lít khí (...
Đọc tiếp
Bài 2: Đổ dung dịch chứa 1g HBr vào dung dịch chứa 1g NaOH. Nhúng miếng giấy quỳ vào dung dịch thu được thì giấy quỳ sẽ đổi màu như thế nào?
Bài 3: Cho lượng dư dung dịch AgNO3 tác dụng với hỗn hợp gồm 0,1 mol NaF và 0,1 mol NaCl. Tính khối lượng kết tủa tạo thành?
Bài 4: Để trung hòa hết 200g dung dịch HX (F, Cl, Br, I) nồng độ nồng độ 14,6%. Người ta phải dùng 250 ml dung dịch NaOH 3,2M. Xác định CTHH của HX
Bài 5: Cho m gam hỗn hợp A gồm Fe và Mg vào dung dịch HCl dư thu được 5,6 lít khí (ở đktc) và dung dịch B. Cho dung dịch B tác dụng hết với dung dịch NaOH thu được 17,7 gam kết tủa.
a. Xác định khối lượng các kim loại trong hỗn hợp A.
b. Tính thể tích khí Cl2 (ở đktc) cần dùng để tác dụng hết với m gam hỗn hợp A.
Bài 6: Cho m gam hỗn hợp A gồm Fe và Mg vào dung dịch HCl dư thu được 5,6 lít khí (ở đktc) và dung dịch B. Cho dung dịch B tác dụng hết với dung dịch NaOH thu được 17,7 gam kết tủa.
a. Xác định khối lượng các kim loại trong hỗn hợp A.
b. Tính thể tích khí Cl2 (ở đktc) cần dùng để tác dụng hết với m gam hỗn hợp A.
Mn giúp em với
Bài 6 :
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
x ___________x _______x
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
y ____________y_______ y
\(n_{H2}=\frac{5,6}{22,4}=0,25\left(mol\right)\)
\(\rightarrow x+y=0,25\left(1\right)\)
\(2NaOH+FeCl_2\rightarrow Fe\left(OH\right)_2+2NaCl\)
__________ x ______ x
\(2NaOH+MgCl_2\rightarrow Mg\left(OH\right)_2+2NaCl\)
__________y _________ y
Ta có mFe(OH)2+mMg(OH)2=17,7
\(\rightarrow90x+58y=17,1\left(2\right)\)
(1)(2)\(\rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,15\end{matrix}\right.\)
\(\rightarrow m_{Fe}=0,1.56=5,6\left(g\right);m_{Al}=0,15.27=4,05\left(g\right)\)
\(2Fe+3Cl_2\rightarrow2FeCl_3\)
0,1____0,15
\(Mg+Cl_2\rightarrow MgCl_2\)
0,15__0,15
\(V_{Cl2}=0,3.22,4=6,72\left(l\right)\)
Bài 2 :
\(n_{HBr}=\frac{1}{81},n_{NaOH}=\frac{1}{40}\)
\(n_{NaOH}>n_{HBr}\rightarrow\) Chuyển xanh
Bài 3 :
\(m\downarrow=m_{AgCl}=0,1.143,5=14,35\left(g\right)\)
Bài 4 :
\(m_{HX}=29,2\left(g\right)\rightarrow n_{HX}=\frac{29,2}{X+1}\left(mol\right)\)
\(n_{NaOH}=0,8\left(mol\right)=n_{HX}\)
\(\rightarrow\frac{29,2}{X+1}=0,8\Leftrightarrow X=35,5\left(Cl\right)\)
Vậy HX là HCl
Bài 5 :
a, \(Fe+2HCl\rightarrow FeCl_2+H_2\)
__a____________a________a
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
b_____________b_________b
\(\rightarrow a+b=0,25\left(1\right)\)
\(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2\downarrow+2NaCl\)
a_________________a____________________
\(MgCl_2+2NaOH\rightarrow Mg\left(OH\right)_2+2NaCl\)
b___________________b_________________
\(m_{kettua}=17,7\left(g\right)\rightarrow90a+58b=17,7\left(2\right)\)
(1);(2) \(\rightarrow\left\{{}\begin{matrix}a=0,1\\b=0,15\end{matrix}\right.\)
\(n_{Fe}=0,1\left(mol\right)\rightarrow m_{Fe}=0,1.56=5,6\left(g\right)\)
\(n_{Mg}=0,15\left(mol\right)\rightarrow m_{Mg}=0,15.24=3,6\left(g\right)\)
b, \(2Fe+3Cl_2\underrightarrow{^{to}}2FeCl_3\)
0,1_____0,15_____________
\(Mg+Cl_2\underrightarrow{^{to}}MgCl_2\)
0,1___0,1__________
\(\rightarrow n_{Cl2}=0,15+0,1=0,25\left(mol\right)\)
\(\rightarrow V_{Cl2}=0,25.22,4=5,6\left(l\right)\)
Dung dịch A chứa các ion Cu2+, Fe3+, Cl-. Để kết tủa hết ion Cl- trong 10ml dung dịch A phải dùng hết 70ml dung dịch AgNO3 1M. Cô cạn 100ml dung dịch A thu được 43,25g hỗn hợp muối khan. Tính nồng độ mol các ion Cu2+, Fe3+, Cl- A. 2M; 1M; 7M B. 2M; 1M; 0,7M C. 0,2M; 0,1M; 7M D. 0,2M; 0,1M; 0,7M
Đọc tiếp
Dung dịch A chứa các ion Cu2+, Fe3+, Cl-. Để kết tủa hết ion Cl- trong 10ml dung dịch A phải dùng hết 70ml dung dịch AgNO3 1M. Cô cạn 100ml dung dịch A thu được 43,25g hỗn hợp muối khan. Tính nồng độ mol các ion Cu2+, Fe3+, Cl-
A. 2M; 1M; 7M
B. 2M; 1M; 0,7M
C. 0,2M; 0,1M; 7M
D. 0,2M; 0,1M; 0,7M
Đáp án A
Ag++ Cl- →AgCl
nCl- = nAg+ = 0,07 mol (trong 10 ml A)
Gọi số mol Cu2+; Fe3+ có trong 100 ml A là x, y mol
Theo ĐLBT ĐT thì: 2x+ 3y = 0,7
64x+ 56y+ 0,7.35,5 = 43,25 gam
Suy ra x = 0,2; y = 0,1
Suy ra nồng độ mol các ion Cu2+,Fe3+,Cl- lần lượt là 2M; 1M; 7M
Đúng 0
Bình luận (0)
Bài 10: Hòa tan hết m gam Na2CO3 trong dung dịch HCl 20% (dư 25% so với ban đầu), thu được khí X và dung dịch Y. Dẫn khí X qua dung dịch Ba(OH)2 dư thu được 27,58 gam kết tủa. Tính nồng độ % của chất tan trong dung dịch Y.