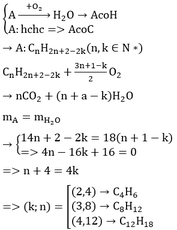đốt cháy hoàn toàn 3 gam hợp chất hữu cơ X ( gồm 2 nguyên tố) sinh ra 5,4 gam nước. Xác định công thức phân tử của X . Biết X nặng hơn khí hidro 15 lần

Những câu hỏi liên quan
Đốt hoàn toàn 1 dung lượng hợp chất hữu cơ AC gồm 2 nguyên tố, thu được 8,8 gam khí CO2 và 5,4 gam h2O. Hãy xác định công thức phân tử của A biết PTK của A bằng 30
Đốt cháy hoàn toàn 9 gam một hh chất hữu cơ A thì thu được 13,2 gam khí cacboic và 5,4 gam nước .Phân tử khối của hợp chất hữu cơ là 180.Hãy xác định công thức phân tử của hợp chất hữu cơ đó
Xem chi tiết
Ta có: \(n_{CO_2}=\dfrac{13,2}{44}=0,3\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\Rightarrow n_H=0,3.2=0,6\left(mol\right)\)
⇒ mC + mH = 0,3.12 + 0,6.1 = 4,2 (g) < mA
⇒ A có các nguyên tố C, H và O.
⇒ mO = 9 - 4,2 = 4,8 (g)
\(\Rightarrow n_O=\dfrac{4,8}{16}=0,3\left(mol\right)\)
Giả sử CTPT của A là CxHyOz. (x, y, z nguyên dương)
⇒ x : y : z = 0,3 : 0,6 : 0,3 = 1: 2 : 1
⇒ CTĐGN của A là (CH2O)n (n nguyên dương)
Mà: MA = 180 (g/mol)
\(\Rightarrow n=\dfrac{180}{12+2+16}=6\left(tm\right)\)
Vậy: A là C6H12O6.
Bạn tham khảo nhé!
Đúng 1
Bình luận (0)
Phân tử hợp chất hữu cơ A có 2 nguyên tố. Đốt cháy hoàn toàn 3 gam chất A thu được 5,4 gam nước. Biết khối lượng mol của A là 30 gam. Công thức phân tử của A là
A
.
C
2
H
6
B
.
C
3
H
8
C
.
C
2
H...
Đọc tiếp
Phân tử hợp chất hữu cơ A có 2 nguyên tố. Đốt cháy hoàn toàn 3 gam chất A thu được 5,4 gam nước. Biết khối lượng mol của A là 30 gam. Công thức phân tử của A là
A . C 2 H 6
B . C 3 H 8
C . C 2 H 4
D . C H 3
Đốt cháy hoàn toàn 3,75 gam một chất hữu cơ A, thu được 11 gam CO2 và 6,75 gam H2O. Biết khối lượng mol của A là 30 gam. Xác định công thức phân tử của A.
a) A hợp chất hữu cơ A gồm những nguyên tố nào ?
b) xác định công thức phân tử của hợp chất hữu cơ A
c) Dẫn toàn bộ khí sinh đi qua bình đựng dung dịch NaOH dư. Tính khối lượng muối tạo thành.
a, có nCO2=11/44=0,25 mol
có nC=nCO2=0,25mol=>mC=12.0,25=3(g)
có nH2O=6,75/18=0,375mol
có nH=2nH2O=2.0,375=0,75mol=>mH=0,75(g)
=>mH+mC=0,75+3=3,75=mA
=> A gồm nguyên tố C và H
b, gọi CTPT A là CxHy
có x/y=nC/nH=0,25/0,75=1/3
=> công thức thực nghiệm (CH3)n<=>CnH3n
có MA=30 gam/mol<=>12n+3n=30<=>n=2
vậy CTPT của A là C2H6
c;PTHH: CO2+2NaOH->Na2CO3+H2O
=> nNa2CO3=nCO2=0,25mol=>mNa2CO3=0,25.106=26,5 gam
Đúng 0
Bình luận (2)
Hợp chất hữu cơ A chỉ chứa 2 nguyên tố X và Y. Đốt cháy hoàn toàn m gam A sinh ra m gam H2O. Biết phân tử khối của A nằm trong khoảng từ 150 đvC đến 170 đvC. a. Hãy cho biết X và Y là những nguyên tố gì? b. Xác định công thức đơn giản nhất (công thức trong đó tỉ lệ số nguyên tử của các nguyên tố là tối giản) và công thức phân tử của A.
Đọc tiếp
Hợp chất hữu cơ A chỉ chứa 2 nguyên tố X và Y. Đốt cháy hoàn toàn m gam A sinh ra m gam H2O. Biết phân tử khối của A nằm trong khoảng từ 150 đvC đến 170 đvC.
a. Hãy cho biết X và Y là những nguyên tố gì?
b. Xác định công thức đơn giản nhất (công thức trong đó tỉ lệ số nguyên tử của các nguyên tố là tối giản) và công thức phân tử của A.
Đốt cháy hoàn toàn 4,8 gam một hợp chất hữu cơ A sau phản ứng thu được 6,6 gam CO2 và 5,4 gam H2O. Biết rằng khi hóa hơi ở điều kiện tiêu chuẩn 2,24 lít khí A nặng 3,2 gam. a) Xác định công thức phân tử của hợp chất hữu cơ A. b) Biết rằng A có phản ứng với Na. Tính thể tích khí hidro (đktc) thoát ra khi cho lượng chất A ở trên phản ứng hoàn toàn với Na dư. (Na = 23, O = 16, C = 16, H = 1)
a)
n CO2 = 6,6/44 = 0,15(mol) => n C = n CO2 = 0,15(mol)
n H2O = 5,4/18 = 0,3(mol) => n H = 2n H2O = 0,6(mol)
=> n O = (4,8 - 0,15.12 - 0,6)/16 = 0,15(mol)
Ta có :
n C : n H : n O = 0,15: 0,6 : 0,15 = 1 : 4 : 1
=> CTP của A là (CH4O)n
M A = (12 + 4 + 16)n = 3,2/(2,24/22,4) = 32
=> n = 1
Vậy CTPT của A là CH4O
b)
$2CH_3OH + 2Na \to 2CH_3ONa + H_2$
n CH3OH = n CO2 = 0,15(mol)
=> n H2 = 1/2 n CH3OH = 0,075(mol)
=> V H2 = 0,075.22,4 = 1,68(lít)
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 23 gam hợp chất hữu cơ A thu được sản phẩm gồm 44 gam CO2 và 27 gam H2O.
a) Hỏi trong A có những nguyên tố nào?
b) Xác định công thức phân tử của A, biết tỉ khối của A so với hidro bằng 23.
Đốt cháy A thu được CO2 và H2O.
Vậy A chứa cacbon, hidro và có thể có oxi.
mC = 44/44 x 12 = 12 (gam)
mH = 27/18 x 2 = 3 (gam)
Theo đề bài, ta có mO = mA – mC – mH => mO = 23 – 12 – 3 = 8 (gam) Trong A có 3 nguyên tố C,H,O và có công thức CxHyOz
Theo đề bài ta có: MA/2 = 23, vậy mA = 46
Cứ 23 gam A có 12 gam cacbon 46 gam A có 12x gam cacbon
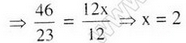
Tương tự ta có y = 6, z = 1
Vậy công thức của A là C2H6O
Đúng 5
Bình luận (0)
Đốt cháy hoàn toàn 1,52 gam một hợp chất hữu cơ X thu được 1,344 lit khí CO2 (đktc) và 1,44 gam nước. Xác định công thức phân tử của X. Biết rằng 22,8 gam X có số phân tử bằng số phân tử của 19,2 gam SO2 ở cùng điều kiện.
$M_X = \dfrac{22,8}{ \dfrac{19,2}{64} } = 76$
Ta có :
$n_C = n_{CO_2} = \dfrac{1,344}{22,4} = 0,06(mol)$
$n_H = 2n_{H_2O} = 2.\dfrac{1,44}{18} = 0,16(mol)$
$\Rightarrow n_O = \dfrac{1,52 -0,06.12 -0,16}{16} = 0,04(mol)$
$n_C : n_H :n_O =0,06 : 0,16 : 0,04 = 3 : 8 : 2$
Vậy CTPT có dạng : $(C_3H_8O_2)_n$
Suy ra: $76n = 76 \Rightarrow n =1 $
Vậy CTPT là $C_3H_8O_2$
Đúng 2
Bình luận (0)
phân tử chất hữu cơ A có 2 nguyên tố.Đốt cháy hoàn toàn chất A thu được 8,8 gam CO2 và 5,4 game nước. Hãy xác định công thức phân tử của A. Biết tỉ khối của A so với khí hirđrô là 15
Theo gt ta có: $n_{CO_2}=0,2(mol);n_{H_2O}=0,3(mol)$
Chất A có CTTQ là $C_xH_y$ (vì có 2 nguyên tố)
Ta có: $x:y=0,2:0,6=1:3$
Vậy CTĐGN của A là $(CH_3)_n$
Mà $M_A=30\Rightarrow A=C_2H_6$
Đúng 2
Bình luận (0)
\(n_{CO_2}=\dfrac{8.8}{44}=0.2\left(mol\right)\)
\(n_{H_2O}=\dfrac{5.4}{18}=0.3\left(mol\right)\)
\(\Rightarrow n_A=0.3-0.2=0.1\left(mol\right)\)
Số nguyên tử C \(\dfrac{0.2}{0.1}=2\)
\(\)Số nguyên tử H : \(\dfrac{0.3\cdot2}{0.1}=6\)
\(CTPT:C_2H_6\)
Đúng 1
Bình luận (0)